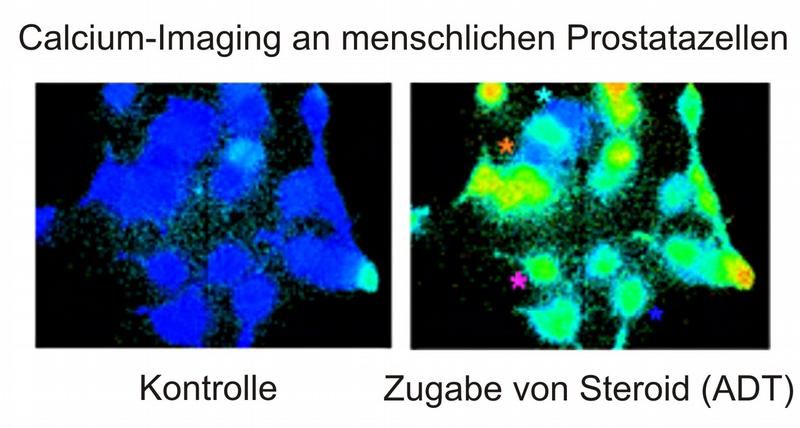
"Druggable" Krebsziel, das in einem Signalweg zur Regulierung der Organgröße gefunden wurde
Mehr als ein Jahrzehnt lang Forschung über den "Hippo"-Signalweg
Es ist bekannt, dass Krebs ungehindertes Zellwachstum bedeutet und dass ein biologischer Weg, der die Größe der Organe reguliert, der auf dem Hippo-Signalweg bekannt ist, auch an Krebs beteiligt ist. Es ist weiter bekannt, dass ein wichtiger Akteur auf diesem Weg, YAP, viele Arten von Tumoren anregt. Jetzt haben die Forscher des Boston Children's Hospital ein anhaltendes Problem gelöst: Wie kann dieses Wissen in ein praktisches Ziel für Medikamente umgesetzt werden? In einer Studie zeigen sie, dass YAP weitgehend über einen anderen Downstream-Player namens NUAK2 wirkt, der leicht mit einem kleinen Molekül inaktiviert werden kann.
"Der Hippo-Signalweg, und insbesondere YAP, war schwer mit Medikamenten zu bekämpfen", sagt Fernando Camargo, Senior Study Author und PhD des Boston Children's Stem Cell Research Program. "Dies ist die erste Demonstration eines "druggable"-Moleküls, das bei jeder Art von Tumor, der von YAP angetrieben wird, angesteuert werden könnte."
Obwohl die Studie Leberkrebs betraf, könnten die Ergebnisse für viele YAP-getriebene Mundkrebsarten, Kopf- und Halskrebs, Bauchspeicheldrüsenkrebs, Eierstockkrebs und Plattenepithelkarzinome relevant sein, fügt Camargo hinzu. Das Team hofft, das in zukünftigen Studien zu testen.
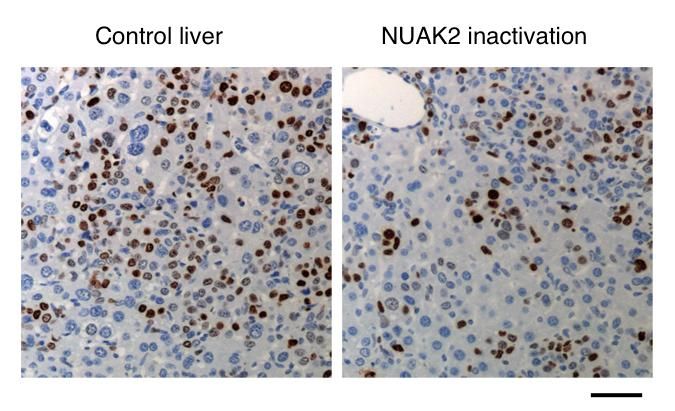
Ein kleines Molekül, das NUAK2 inaktiviert, reduziert die Anzahl der Krebszellen in der Mausleber
Wei-Chien Yuan/Boston Children's Hospital
Finden eines medikamentösen Krebsziels
YAP ist ein Transkriptionsfaktor, eine Art von Ziel, das als "unmedikamentabel" gilt, da es den Transkriptionsfaktoren an strukturellen Merkmalen fehlt, die es einem Medikament ermöglichen, sich an sie zu binden. Aber YAP wiederum reguliert die Aktivität vieler anderer Gene, und Wei-Chien Yuan, PhD, im Camargo-Labor wollte diese Gene identifizieren, in der Hoffnung, etwas anderes zu finden.
Mit menschlichen Leberkrebs-Zelllinien und einem Mausmodell von Leberkrebs kombinierte Yuan mehrere Assays, um herauszufinden, welche nachgelagerten Gene YAP beeinflusst. Sie fand 14, dann schränkte sie ihre Suche auf Kinasen ein, Enzyme, die besonders geeignet sind, mit Medikamenten angesteuert zu werden. Nur einer tauchte auf: NUAK2.
Weitere Experimente zeigten, dass NUAK2 (auch bekannt als nicht-fermentierende[SNF1]-ähnliche Kinase oder SNARK) für das YAP-gesteuerte Wachstum in menschlichen Krebszelllinien und für die Proliferation von Leberkrebs in Mausmodellen entscheidend ist.
Schließlich zeigten sie, dass eine niedermolekulare Verbindung, die NUAK2 inaktiviert, die YAP-getriebene Krebszellproliferation und Leberentstehung stark dämpfte.
Die gezielte Anwendung von NUAK2 hat einen zusätzlichen Nutzen, sagt Camargo, der auch mit dem Dana-Farber/Boston Children's Cancer and Blood Disorders Center verbunden ist. "Es wird zurückgemeldet, um YAP selbst weiter zu aktivieren, so dass die Hemmung von NUAK2 die Aktivität von YAP weiter verringert, was genau das ist, was Sie wollen."
Zukunftspläne
Yuan und ihre Kollegen hoffen nun, ihre Ergebnisse zu erweitern.
"Wir wissen, dass die Hemmung von NUAK2 bei Leberkrebs funktioniert. Wir müssen jetzt sehen, ob der gleiche Mechanismus bei anderen Krebsarten im Spiel ist", sagt Camargo.
Sie planen auch, ihr kleines Molekül zu modifizieren, das ursprünglich im Labor von Nathanael Gray, PhD, am Dana-Farber Cancer Institute synthetisiert wurde.
"Wir wollen sehen, ob wir die Verbindung selektiver machen können", sagt Yuan, Erstautor auf dem Papier. "Es hat andere unspezifische Ziele, also müssen wir es modifizieren, um es nutzbar zu machen."
Eine Wachstumsmentalität
Die Geschichte von YAP begann vor über einem Jahrzehnt mit der Entdeckung des Größenkontrollpfades Hippo - so genannt, weil die Manipulation in Fruchtfliegen zum Wachstum von riesigen Tumoren, übergroßen Augen und Flügeln führte, die achtmal so groß waren wie die normale Größe. Größere Tiere mit Defekten in Flusspferden wurden auch mit überwucherten Körperteilen gefunden, und Camargo zeigte, dass die Aktivierung von YAP die Größe einer Mausleber vervierfachen kann. Hippo und YAP wurden später für die Krebsforschung interessant.