Bakterien-Gen sorgt für Balance
Gezielter Angriff auf Speicherproteine reguliert Eisenhaushalt in Bakterien
Verschiedene Bakterienarten enthalten eine Art "Marker-Gen". Damit wird eine komplexe Zell-Maschinerie gestartet, die Proteine verdaut und recycled. Jülicher Wissenschaftler fanden heraus, dass das Marker-Gen auch für den Eisenhaushalt und damit das Wachstum der Zelle eine wichtige Rolle spielt. Die neuen Erkenntnisse könnten beim Kampf gegen Infektionskrankheiten wie Tuberkulose helfen.
Das Corynebacterium glutamicum dient als ungefährlicher Modellorganismus für den eng verwandten Erreger der Tuberkulose, mit dem es viele Gemeinsamkeiten hat.
Forschungszentrum Jülich
Die Biotechnologen des Jülicher Instituts für Bio- und Geowissenschaften studieren seit Jahren das Corynebacterium glutamicum. Mit dem Bodenbakterium werden jährlich mehrere Millionen Tonnen Aminosäuren produziert, zum Beispiel der Futtermittelzusatz L-Lysin. Das Bakterium dient aber auch als ungefährlicher Modellorganismus für den eng verwandten Erreger der Tuberkulose, mit dem es viele Gemeinsamkeiten hat. Eine davon ist ein Marker-Gen, das als Matrize für ein "prokaryotisches Ubiquitin-artiges Protein" dient – ein Marker-Protein. Im Tuberkuloseerreger ist es die erste Komponente in einer komplexen Zell-Maschinerie, die Proteine erst entfaltet und dann abbaut, sodass ihre Aminosäure-Bausteine wiederverwendet werden können. "Das Marker-Protein wird mit ausgewählten anderen Proteinen verbunden und markiert sie auf diese Weise für den schrittweisen Abbau", erklärt Michael Bott, Leiter des Forschungsbereichs Systemische Mikrobiologie. "Die letzte Komponente dieser Demontage-Maschinerie ist das Proteasom, eine Art Proteinhäcksler der Zelle." Dieses Element existiert jedoch nicht im Corynebacterium glutamicum. Doch was ist dann dort die Aufgabe des Marker-Gens?
Um diese Frage zu beantworten, entfernten die Jülicher Wissenschaftler das Marker-Gen aus dem Genom von Corynebakterien und verfolgten ihr Wachstum unter unterschiedlichen äußeren Bedingungen. Nur in einer der über zwanzig Testreihen zeigte sich ein messbarer Effekt: Eine mangelhafte Versorgung mit Eisen führte zu stark verringertem Wachstum der genetisch veränderten Bakterien.
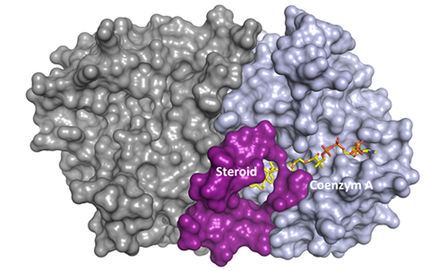
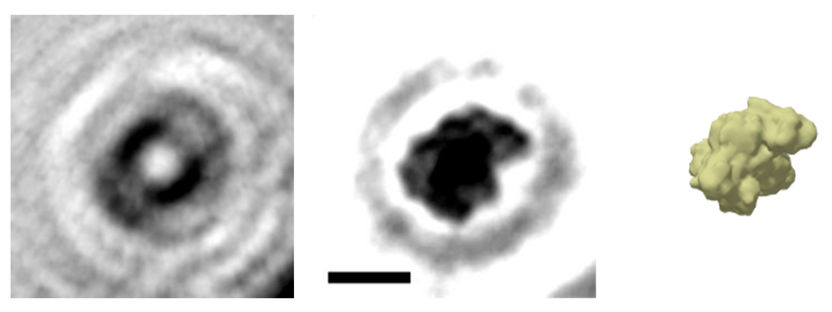
"Eisen ist ein Spurenelement, das von Bakterienzellen in relativ großen Mengen gebraucht wird", erklärt Bott. "Viele essenzielle Proteine sind eisenhaltig, für ihre Herstellung wird deshalb Eisen benötigt. Andererseits darf eine Zelle auch nicht zu viel freies Eisen enthalten, denn in Verbindung mit Sauerstoff kann es zu einem Zellgift werden." Deshalb verfügen Zellen über Eisenspeicher, die sogenannten Ferritine. Diese Proteinkomplexe haben die Form einer Hohlkugel und können Eisen in einer ungefährlichen Form einkapseln, sodass es bei Bedarf zur Verfügung steht.
Eingeschlossenes Eisen
Die Bakterienzellen ohne das Marker-Gen zeigten typische Anzeichen einer unzureichenden Eisenversorgung. Als die Wissenschaftler jedoch daraufhin den Eisengehalt der Zellen bestimmten, zeigte sich, dass er dem in der Normalform – dem sogenannten Wildtyp – des Bakteriums entsprach. Wieso also die Mangelerscheinungen? Michael Bott hat eine Erklärung: "Das Eisen wird nach wie vor in den zelleigenen Speichern gesammelt und eingekapselt. Es kann jedoch nicht mehr herausgelöst werden." Die Zelle kann also nicht mehr auf ihre Eisenvorräte zurückgreifen.
Die Ergebnisse der Jülicher Studie legen nahe, dass das Marker-Protein eine entscheidende Rolle dabei spielt, das gespeicherte Eisen aus der Einkapselung wieder herauszulösen. "Wir wissen, dass das Protein an den Eisenspeicher gebunden wird – nicht nur im Corynebakterium, sondern auch im Tuberkulose-Erreger. Möglicherweise ist es auch dort für die Freigabe des gespeicherten Eisens verantwortlich", so Bott. "Und Eisen ist für viele bakterielle Krankheitserreger essenziell. Ein erzwungener Mangel könnte das Wachstum dieser Erreger aufhalten, oder zumindest verlangsamen." Ein Antibiotikum, das das Marker-Protein angreift, könnte damit in der Zukunft bei der Tuberkulose-Bekämpfung helfen. "Wir denken auch über mögliche Anwendungen in der Biotechnologie nach, zum Beispiel bei der Entwicklung von bakteriellen Produktionsstämmen", erklärt Bott. "Doch noch befinden wir uns in der Grundlagenforschung. Erst wenn wir die Mechanismen in den Bakterienzellen im Einzelnen verstehen, können wir den nächsten Schritt tun."