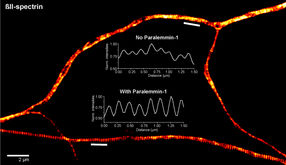
Leuchtsignale aus der lebenden Zelle
Forscher der Goethe-Universität und des MIT, Cambridge (USA) berichten über ein Verfahren, mit dem sie fluoreszierende Proteinmarker unter Druck und fein dosiert in lebende Zellen einschleusen können. Das Verfahren liefert zeitlich und räumlich hoch aufgelöste Bilder und lässt sich mit anderen Markierungsmethoden kombinieren.
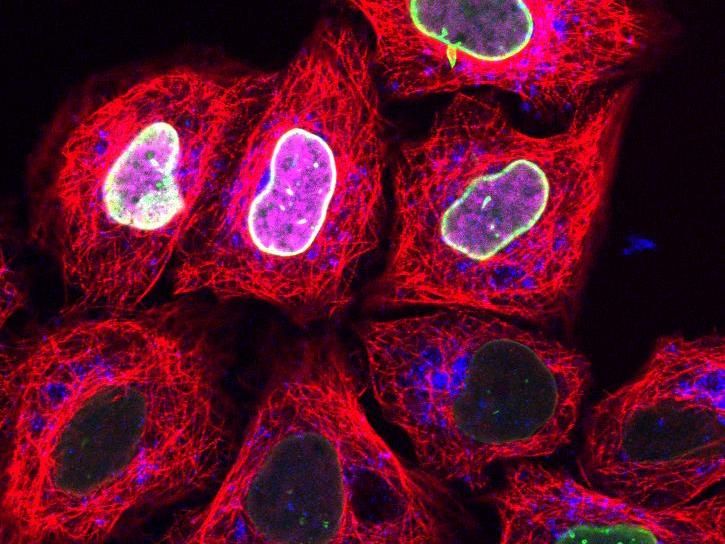
Mit Hilfe des Schlüssel-Schloss-Prinzips lässt sich selektiv das Kernhüllenprotein Lamin A mit der fluoreszenzmarkierten Sonde trisNTA (grün) anfärben. Simultan können in der gleichen Zelle durch orthogonale Markierungsmethoden weitere Proteine visualisiert werden (Histon2B in mangenta; Lysosomen in blau; Mikrotubuli in rot).
Ak Tampe, Goethe-Universität
Bestimmte Proteine in der Zelle aufzuspüren, gleicht der Suche nach einer Nadel im Heuhaufen. Um Proteine orten und ihre Funktion in der lebenden Zelle entschlüsseln zu können, versuchen Forscher, sie mit fluoreszierenden Molekülen zu markieren. Doch diese lassen sich oft nicht in genügender Anzahl einschleusen. Eine Forschergruppe der Goethe Universität fand jetzt in Kooperation mit amerikanischen Kollegen eine Lösung für dieses Problem.
„Obwohl immer mehr Proteinmarkierungsmethoden synthetische Fluoreszenzfarbstoffe nutzen, leiden diese oft unter Problemen wie Zellpermeabilität und geringer Markierungseffizienz. Auch kann man sie nur eingeschränkt mit anderen Proteinmarkierungsmethoden verwenden“, erklärt Dr. Ralph Wieneke vom Institut für Biochemie der Goethe-Universität.
Die Arbeitsgruppe um Wieneke und Prof. Robert Tampé hat schon vor längerer Zeit einen Marker entwickelt, der ausgewählte Proteine mit einer Präzision von wenigen Nanometern in der Zelle lokalisiert. Es handelt sich um ein hochspezifisches Schlüssel-Schloss-Paar, bestehend aus dem kleinen synthetischen Molekül trisNTA und einem genetisch codierten His-tag.
Um diesen Proteinmarker in die Zellen zu schleusen, verwendeten die Frankfurter Forscher zusammen mit Kollegen des Massachussetts Institute of Technology (MIT), Cambridge, USA, ein Verfahren, bei dem der Marker zusammen mit den Zellen in Lösung schwimmt. Diese wird dann durch verengte Kanäle gepresst (cell squeezing). Unter dem Druck nehmen die Zellen die fluoreszierenden Sonden mit einer Effizienz von über 80 Prozent auf. Das Hochdurchsatz-Verfahren erlaubt es, eine Million Zellen pro Sekunde durch die künstliche Kapillare zu pressen.
Da der Marker in hohem Maße spezifisch an die gewünschten Proteine bindet und sich seine Konzentration in der Zelle präzise regulieren ließ, konnten die Forscher hochauflösende mikroskopische Bilder von lebenden Zellen aufnehmen. Zudem konnten sie den Marker erst an sein Zielmolekül binden lassen, wenn es durch Licht aktiviert wurde. So lassen sich zelluläre Prozesse nicht nur räumlich, sondern auch zeitlich präzise verfolgen.
Die Forscher konnten ihre Markierungsmethode in lebenden Zellen sogar mit anderen Proteinmarkierungsmethoden kombinieren. So wird es möglich, gleichzeitig mehrere Proteine in Echtzeit zu beobachten. „Wir konnten eine Vielzahl an fluoreszenzmarkierten trisNTAs mittels cell squeezing in Zellen einschleusen. Damit erweitern sich die Möglichkeiten der konventionellen und der hochauflösenden Lebendzellmikroskopie ungemein“, erklärt Prof. Robert Tampé. Zukünftig wird man dynamische Prozesse in lebenden Zellen mit höchster Auslösung in Zeit und Raum verfolgen können.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Fluoreszenzmikroskopie
Die Fluoreszenzmikroskopie hat die Life Sciences, Biotechnologie und Pharmazie revolutioniert. Mit ihrer Fähigkeit, spezifische Moleküle und Strukturen in Zellen und Geweben durch fluoreszierende Marker sichtbar zu machen, bietet sie einzigartige Einblicke auf molekularer und zellulärer Ebene. Durch ihre hohe Sensitivität und Auflösung erleichtert die Fluoreszenzmikroskopie das Verständnis komplexer biologischer Prozesse und treibt Innovationen in Therapie und Diagnostik voran.
Themenwelt Fluoreszenzmikroskopie
Die Fluoreszenzmikroskopie hat die Life Sciences, Biotechnologie und Pharmazie revolutioniert. Mit ihrer Fähigkeit, spezifische Moleküle und Strukturen in Zellen und Geweben durch fluoreszierende Marker sichtbar zu machen, bietet sie einzigartige Einblicke auf molekularer und zellulärer Ebene. Durch ihre hohe Sensitivität und Auflösung erleichtert die Fluoreszenzmikroskopie das Verständnis komplexer biologischer Prozesse und treibt Innovationen in Therapie und Diagnostik voran.