Identifizierung eines für die Regeneration nach einem Schlaganfall entscheidenden Gehirnproteins
Alle 40 Sekunden erleidet jemand in den Vereinigten Staaten einen Schlaganfall und die verfügbaren Therapien, wie z.B. Gerinnungshemmer oder Gerinnungsentferner, konzentrieren sich darauf, das Ausmaß der Hirnschäden zu begrenzen. Jetzt zeigt die Forschung der University of Pittsburgh School of Medicine und des VA Pittsburgh Healthcare System, dass ein Gehirnprotein namens UCHL1 entscheidend dafür sein kann, wie sich Nervenzellen nach Schlaganfall reparieren. Die Forschung, die in Tiermodellen durchgeführt wird, könnte bei der Entwicklung von Therapien helfen, die die Schlaganfallregeneration durch Verbesserung des zugrunde liegenden biologischen Reparaturprozesses verbessern.
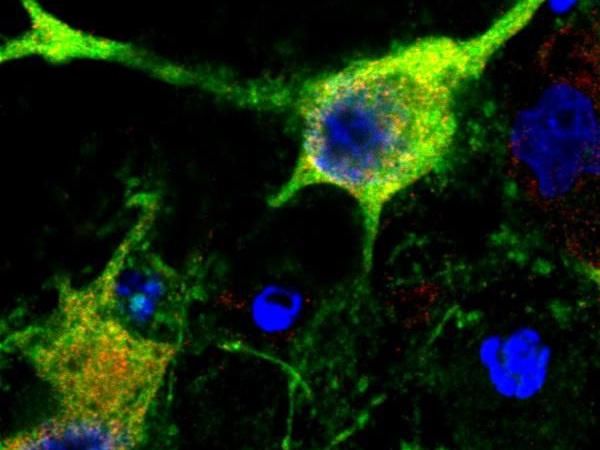
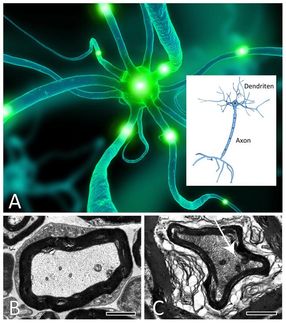
Mausnervenzelle mit teilweise geschädigten Axonen (grün), die aus dem Zellkern nach außen ragen
Steven Graham/University of Pittsburgh
"Auch wenn traditionelle Schlaganfalltherapien sehr effektiv sind, wenn sie verfügbar sind, muss die Behandlung in den ersten Stunden nach einem Schlaganfall beginnen und die meisten Patienten sind nicht in der Lage, diese Behandlungen zu erhalten. Es besteht also ein klarer Bedarf an neuen Ansätzen, die die Genesungstage nach einem Schlaganfall eines Patienten verbessern können", sagte Co-Seniorautor Dr. Steven Graham, Professor für Neurologie an der Pitt's School of Medicine und Associate Chief of Staff for Research an der VA Pittsburgh. "Wir denken, dass wir ein Protein identifiziert haben, das die Ursache dafür ist, wie sich das Gehirn nach einem Schlaganfall erholt, was es zu einem attraktiven Ziel für die Entwicklung von Medikamenten macht, die zur Verbesserung der Regeneration beitragen."
UCHL1 ist ein Enzym, das im Gehirn hochaktiv ist und eine Rolle bei der Beseitigung abnormaler Proteine spielt. Mutationen im Gen, das für UCHL1 kodiert, sollen motorische Funktionsdefizite beim Menschen verursachen. Frühere Forschungen aus Grahams Labor hatten einige Hinweise auf die Funktion von UCHL1 gegeben und gezeigt, dass Cyclopentenon-Prostaglandine (CyPgs) - Fettsäuremoleküle -, die nach einem Schlaganfall in Nervenzellen freigesetzt werden, an UCHL1 binden und dessen Funktion beeinträchtigen.
Graham arbeitete mit Feng Zhang, Ph.D., einem Assistenzprofessor für Neurologie an der Pitt's School of Medicine und Mitautor der aktuellen Studie, die in den Proceedings of the National Academy of Sciences veröffentlicht wurde, zusammen, um die genaue Rolle von UCHL1 bei Schlaganfällen herauszufinden und festzustellen, ob es sich um ein lebensfähiges Ziel für Medikamente handeln könnte.
Die Forscher erstellten ein Mausmodell, in das sie eine veränderte Version des UCHL1-Gens einführten, die gegen die Auswirkungen der CyPgs resistent war. Anschließend modellierten sie operativ die Wirkung eines Schlaganfalls sowohl bei gentechnisch veränderten als auch bei normalen Mäusen, um zu vergleichen, wie sich die Nervenzellen erholt haben.
Das Verhindern, dass CyPgs die Hemmung von UCHL1 verhinderten, verringerte die Anzahl der Verletzungen der Axone nach einem Schlaganfall im Vergleich zu normalen Mäusen. Axone - die langen Kabel, die aus der Mitte der Nervenzelle nach außen ragen - werden benötigt, um elektrische Signale zu übertragen und sich mit anderen Neuronen zu verbinden und den Großteil der "weißen Substanz" im Gehirn ausmachen.
Weitere Experimente zeigten, dass das Halten von UCHL1 nach einem Schlaganfall dazu beiträgt, die Funktion von Neuronen und Hirngewebe zu erhalten, indem es zelluläre Reparaturmechanismen aktiviert, die beschädigte Proteine schnell aufräumten und so den Verlust weiterer Nervenzellen verhindern. Die Mäuse mit der resistenten Form von UCHL1 hatten auch die Erholung von Wach-, Gleichgewichts- und anderen motorischen Funktionen verbessert.
"Während sich die meisten Schlaganfalltherapien darauf konzentrieren, den neuronalen Tod zu verhindern, könnten die Erhaltung der axonalen Integrität und die Verringerung von Verletzungen der weißen Substanz ebenso wichtig für eine verbesserte Genesung sein", sagt Graham, der auch Neurologe am UPMC Stroke Institute ist. "UCHL1 ist ein zentraler Akteur in diesem Prozess."
Graham und seine Kollegen arbeiten nun daran, neue Medikamente zu identifizieren, die verhindern könnten, dass CyPgs an UCHL1 binden, oder beschädigte UCHL1-Proteine durch ein Derivat zu ersetzen, das intravenös verabreicht werden kann.
Originalveröffentlichung
Hao Liu el al.; "Role of UCHL1 in axonal injury and functional recovery after cerebral ischemia"; PNAS; 2019.