Entzündungsforschung: Riesenzellen räumen auf
Kampf der Giganten: Das Ganze ist mehr als die Summe seiner Teile
Immunforscher konnten jetzt erstmalig Mehrkernigen Riesenzellen klare funktionelle Eigenschaften zuweisen. Der Lübecker Wissenschaftler Prof. Admar Verschoor konnte zusammen mit Forschern um Prof. Mark Pepys in London und Dr. Laura Helming in München zeigen, dass Riesenzellen besonders für die Aufnahme von großen und Komplement-beschichteten Partikeln sowie pathogenen Ablagerungen im Gewebe gerüstet sind. Die einzelnen Fresszellen (Makrophagen), aus denen sie durch Zell-Fusion entstehen, sind dazu aufgrund ihrer begrenzten Zellmembran und Aktivierung nur bedingt fähig.
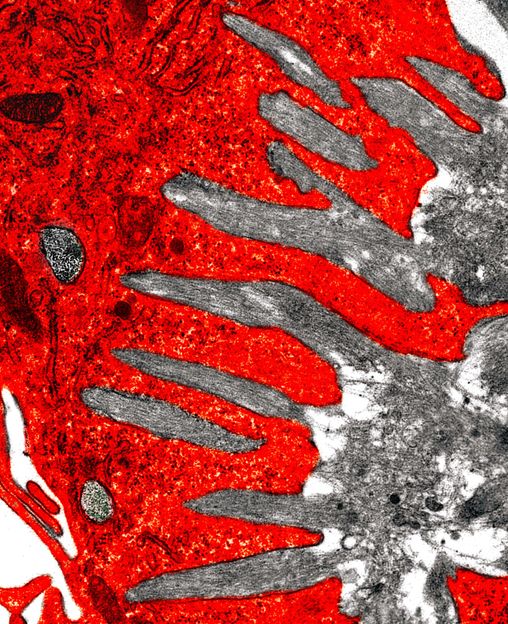
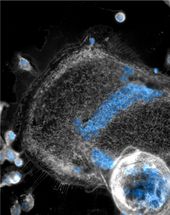
Gewaltige Zellen für schwere Brocken: Mehrkernige Riesenzelle (rot) bei der Aufnahme von Amyloidablagerungen im Gewebe.
Andrzej Loesch, UCL
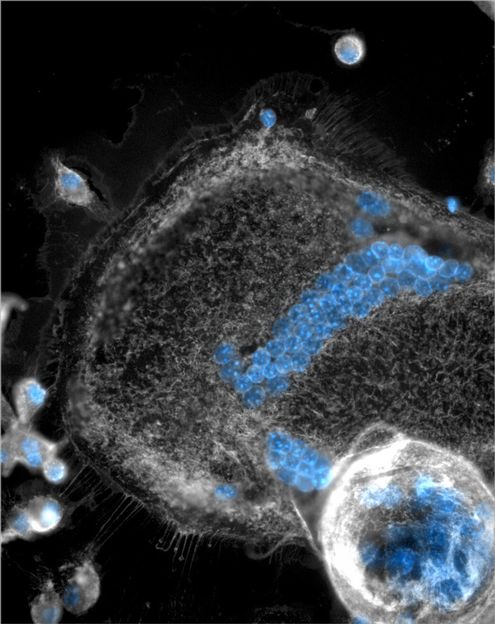
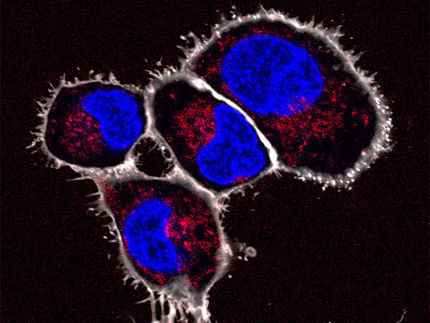
Spezialisten für die Aufnahme großer Partikel: Mit bis zu über 100 Kernen (blau) können Riesenzellen ein Vielfaches der Größe normaler Immunzellen annehmen
Ronny Milde, TUM
Mehrkernige Riesenzellen (Multinucleated Giant Cells, MGCs) wurden zwar schon vor fast 150 Jahren von dem deutschen Mediziner Theodor Langhans in knotigen Schwellungen, sogenannten Tuberkeln, detailgenau beschrieben. Sie dienen Pathologen als Marker für verschiedene chronisch-entzündliche Erkrankungen. Dennoch war ihre Funktion im Körper bisher weitestgehend unbekannt.
Neben einer klaren Spezialisierung von MGCs zur Aufnahme besonders großer Partikel zeigten die von Erstautor Ronny Milde durchgeführten Experimente, dass die Aufnahme von solchen Partikeln deutlich gesteigert war, die durch Proteine des körpereigenen Komplementsystems gebunden wurden. Hauptaufgabe des Komplementsystems ist es, die Zerstörung von Krankheitserregern durch die Fresszellen zu koordinieren und zu verstärken.
Die veröffentlichten Beobachtungen erklären zudem Behandlungserfolge einer neuartigen Therapie für Systemische Amyloidose, einer seltenen, aber sehr schweren Erkrankung, die durch die Fehlfaltung von Eiweißen (Proteinen) verursacht wird: Der von Mark Pepys entwickelte und derzeit in klinischen Studien getestete Therapieansatz führte im Tiermodell nicht nur zur Bildung von MGCs, sondern ebenfalls zur Aktivierung des Komplementsystems an den pathogenen Proteinablagerungen. Die resultierende effektive Entfernung dieser Ablagerungen mittels Komplement und MGCs bietet Patienten mit Systemischer Amyloidose somit eine hoffnungsvolle Aussicht auf Besserung des Verlaufes ihrer Erkrankung.
Zusammenfassung der Studie
Im Einzelnen zeigt die in „Cell Reports“ veröffentlichte Arbeit auf der Grundlage einer systematischen in vitro-Analyse, dass IL-4-induzierte MGCs große und Komplement-opsonisierte Partikel besser phagozytieren können als deren unfusionierte M2-Makrophagen-Vorläufer. Die Expression von Komplement-Rezeptor CR4 war erhöht in MGCs, dieser fungierte jedoch vorwiegend als Adhäsionsintegrin. Im Gegensatz dazu und trotz unveränderter Expression stieg die funktionelle Aktivierung des Komplement-Rezeptors CR3 während der Fusion, und dieses lokalisierte auf den extensiven Membranfalten, welche aus der Fusion resultierten. Die Kombination von erhöhter Membranfläche und aktiviertem CR3 rüstet MGCs somit optimal für die Phagozytose von Komplement-opsonisierten großen Partikeln und deren Beseitigung aus dem Gewebe. Zudem finden sich diese Eigenschaften ebenso in MGCs in vivo in der kürzlich beschriebenen Komplement-abhängigen therapeutischen Beseitigung von Ablagerungen in Systemischer Amyloidose. Riesenzellen sind mehr als die Summe ihrer Teile.