Struktur des Eisen-Transportproteins entschlüsselt
Erstmals kann die komplexe Struktur des Proteins, das die lebenswichtigen Eisen-Ionen in die Zelle schleust, beschrieben werden. Die Biochemiker der Universität Zürich schaffen so die Grundlage für das bessere Verständnis des Eisen-Stoffwechsels. Die Resultate können für die künftige Therapie von Eisen-Stoffwechselkrankheiten wichtig sein.
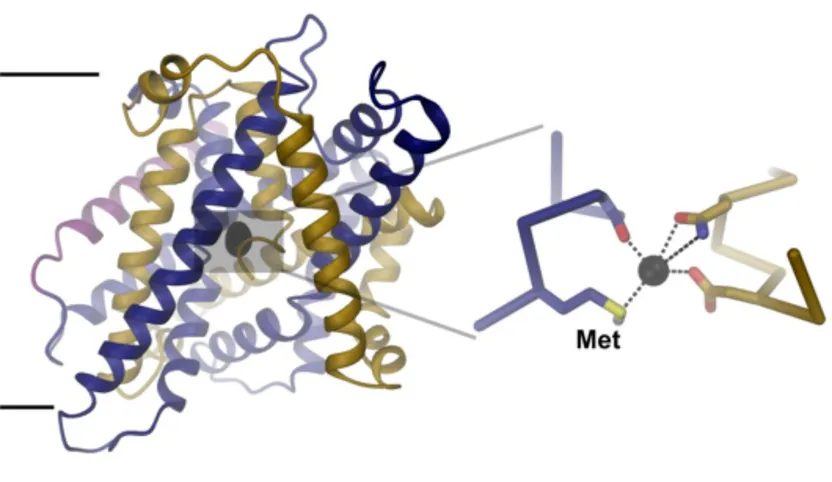
Struktur des Eisentransportproteins: Der Blick ist parallell zur Membran (schwarze Linie). Eine vergrösserte Ansicht der Ionenbindungsstelle mit gebundenem Fe2+ Ion (rechts) zeigt die Interaktion des Ions mit konservierten Proteinresten. Die Methionin-Seitenkette, die entscheidend zur Selektivität der Bindungsstelle beiträgt, ist markiert (Met).
UZH
Eisen ist das häufigste Spurenelement im Menschen. Als Ko-Faktor bestimmter Proteine spielt es eine zentrale Rolle beim Transport von Sauerstoff und bei wichtigen Stoffwechselprozessen – wie Elektronentransport und Energiestoffwechsel – in der Zelle. Aufgrund seiner einerseits wichtigen Bedeutung in vielfältigen Zellabläufen, aber andererseits seiner Toxizität bei übermässiger Anhäufung im Körper, wird die Aufnahme und Speicherung von Eisen im Körper strikt reguliert. Bei Säugetieren wird Eisen mit Hilfe des Membranproteins DMT1 in die Zellen hineingeschleust. Fehlerhafte Veränderungen in der Proteinstruktur beeinträchtigen diesen Transport. Die Folge können schliesslich Eisenstoffwechselkrankheiten wie Blutarmut (Anämie) und Hämochromatose, die Eisenspeicherkrankheit, sein.
Im Wissenschaftsjournal «Nature Structural and Molecular Biology» beschreibt nun Ines Ehrnstorfer, Doktorandin in der Arbeitsgruppe von Prof. Raimund Dutzler am Biochemischen Institut der Universität Zürich, gemeinsam mit Kollegen, erstmals präzise den Aufbau des Transportproteins. Anhand der Struktur der Ionen-Bindungsstelle können die Forscher erklären, warum DMT1 die zweiwertigen Metallionen von Eisen und Mangan (Fe2+ und Mn2+), nicht aber das gleich geladene Calcium-Ion (Ca2+) in die Zelle transportiert – dies obwohl Calcium in viel höherer Konzentration vorliegt.
Die Bindungsstelle für Ionen aufgeschlüsselt
Um die strukturelle Basis für die Selektivität des Transports der sogenannten zweiwertigen Metall-Ionen – insbesondere des Transports von Eisen (Fe2+) – zu verstehen, hat Ines Ehrnstorfer die Struktur eines nahen bakteriellen Verwandten von DMT1 mit Hilfe der Röntgenstrukturanalyse bestimmt. Die Untersuchung macht Folgendes sichtbar: Die Struktur des Proteins enthält eine Ionen-Bindungsstelle im Zentrum des Proteins. Diese Andockstelle ist aus konservierten Aminosäuren aufgebaut. «Eine dieser Aminosäuren, das Methionin, kann nur mit den Übergangs-Metallionen, nicht aber mit Ca2+, interagieren», führt Ehrnstorfer weiter aus. Die Studie zeige auch, dass Mutationen in der Bindungsstelle die Interaktion mit Ionen und die Transporteigenschaften sowohl im bakteriellen wie auch im humanen Transporter schwäche.
«Die Resultate legen damit die Basis für das Verständnis des selektiven Transports von Metall-Ionen insbesondere von Eisen. Sie sind damit Voraussetzung für die gezielte Entwicklung von Medikamenten zur Behandlung von Eisenspeicherkrankheiten», so die Biochermikerin.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren

Antibody Stabilizer von CANDOR Bioscience
Protein- und Antikörperstabilisierung leicht gemacht
Langzeitlagerung ohne Einfrieren – Einfache Anwendung, zuverlässiger Schutz

DynaPro NanoStar II von Wyatt Technology
NanoStar II: DLS und SLS mit Touch-Bedienung
Größe, Partikelkonzentration und mehr für Proteine, Viren und andere Biomoleküle

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte

Nuvisan GmbH - Neu-Ulm, Deutschland

Mensch oder ChatGPT? - Unterschiede zwischen tiermedizinischen Fachartikeln schwer feststellbar

Ethris und Spin-off Heqet Therapeutics kooperieren bei der Entwicklung von RNA-basierten Therapeutika für Herzinfarkt und Herzversagen - Zusammenarbeit soll das Potenzial von nicht kodierenden RNAs (ncRNAs) bei der Regeneration von Herzgewebe nutzen
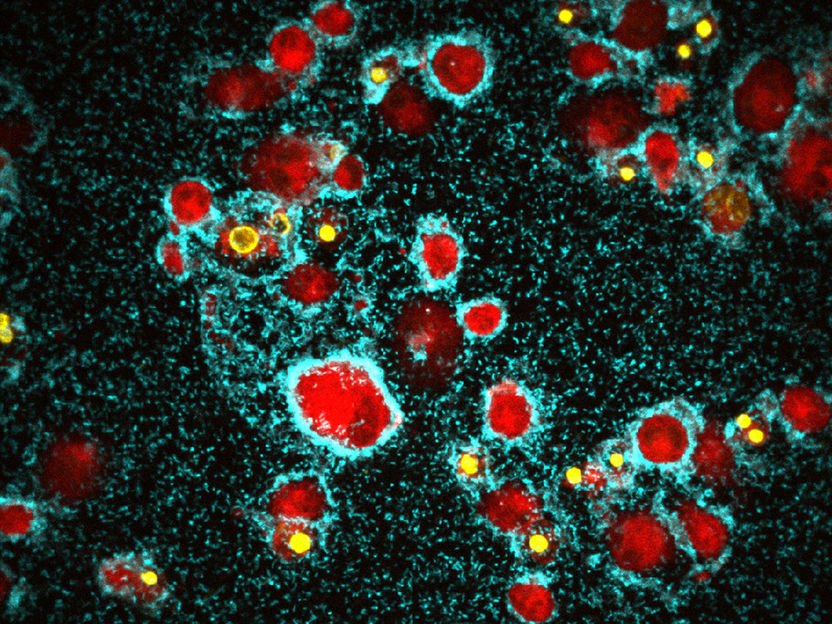
Cholera-Erreger töten Immunzellen mit aggressivem Biofilm - Studie liefert neue Erkenntnisse über Angriffsstrategien von Krankheitserregern

Ein „Chamäleon“ im Magen - Wissenschaftler haben schnelle Anpassungsfähigkeit des Magenkrebserregers Helicobacter pylori ergründet
Analytica 2020 mit sehr guten Ergebnissen im digitalen Format - Größte virtuelle Plattform der Laborbranche
Kategorie:Schädel

Sichtbar mehr Bewegung: Forschende aus dem Ruhrgebiet entwickeln neues Mikroskop für Immunzellen - Hochdurchsatzanalyse von Arzneimittelsubstanzen: 60-mal schneller als herkömmliche Mikroskope

Zellen passen sich ultraschnell an die Schwerelosigkeit an
Kategorie:Dermatologe
Ultradünnschichtverfahren





















































