Zielgenau gegen Autoimmunkrankheiten und chronische Entzündungen
Neuer Mechanismus zur Hemmung des Immunoproteasoms aufgeklärt
Multiple Sklerose, Diabetes Typ I und Lupus haben eines gemeinsam: Es handelt sich um Autoimmunerkrankungen, bei denen die Abwehrzellen nicht mehr zwischen Freund und Feind unterscheiden können und körpereigenes Gewebe angreifen. Eine Schlüsselrolle spielt dabei das Immunoproteasom, das dem Abwehrsystem Informationen über die Vorgänge in der Zelle liefert. Chemikerinnen und Chemiker der Technischen Universität München (TUM) haben nun einen Weg entdeckt, dessen Funktion mithilfe eines neuartigen Mechanismus zu hemmen und legen damit die Grundlage für die mögliche Optimierung bestehender Wirkstoffe.
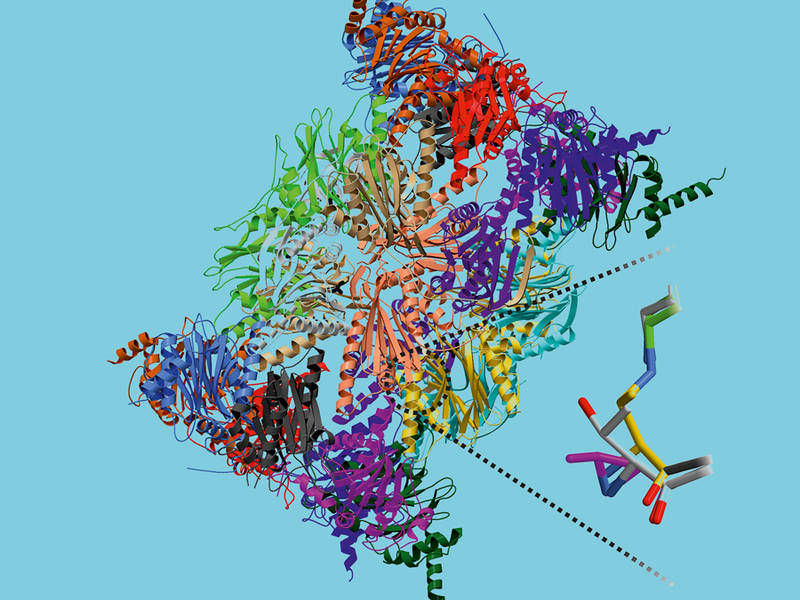
Die Kristallstruktur des Immunoproteasoms. Rechts ein Schema des durch den Inhibitor zerstörten aktiven Zentrums.
Lehrstuhl für Biochemie / TUM
Das Immunsystem fungiert als Polizei des Körpers und schützt uns vor Eindringlingen wie Bakterien und Viren. Um zu erfahren, was in der Zelle vor sich geht, benötigt es aber Informationen über den Fremdkörper. Diese Aufgabe übernimmt das sogenannte Immunoproteasom. Es handelt sich dabei um einen zylinderförmigen Proteinkomplex, der Eiweißstrukturen des Eindringlings in Bruchstücke zerlegt und diese dem Abwehrsystem zur Verfügung stellt.
"Bei Autoimmunerkrankungen wie Rheuma, Diabetes Typ I und Multipler Sklerose oder schweren Entzündungen ist oftmals eine deutlich erhöhte Konzentration des Immunoproteasoms in der Zelle messbar", erklärt Prof. Michael Groll vom Lehrstuhl für Biochemie der TUM. "Eine Inaktivierung dieser Abbaumaschinerie unterdrückt die Neubildung von Immunbotenstoffen, was wiederum eine übermäßige Immunreaktion verhindert."
Feine, aber wesentliche Unterschiede
Bereits seit Längerem sind Wissenschaftler auf der Suche nach neuen Wirkstoffen, die das Immunoproteasom gezielt hemmen, ohne das ebenfalls in der Zelle vorkommende konstitutive Proteasom zu beeinträchtigen. Das konstitutive Proteasom baut gezielt fehlerhafte oder nicht mehr benötigte Eiweiße ab und übernimmt damit das zelluläre Recycling. Werden sowohl das konstitutive Proteasom als auch das Immunoproteasom gehemmt, führt dies zum Tod der Zelle.
Eine Voraussetzung für das Design eines spezifischen Wirkstoffs schuf die Forschergruppe um Groll Anfang 2012: Sie entschlüsselte die Kristallstruktur des Immunoproteasoms. So war es möglich, die feinen, aber wesentlichen Unterschiede zwischen den nahezu identisch aufgebauten Strukturen zu erkennen.
Besonderer Wirkmechanismus
Der potenzielle Wirkstoff, den die Wissenschaftler nun entwickelten, basiert auf dem Epoxyketon ONX 0914, einem Immunoproteasom-Hemmer, der in klinischer Phase getestet wurde. Die Forscher ersetzten das Epoxyketon durch eine Sulfonylfluorid-Gruppe und veränderten deren Positionierung am Inhibitor. Als Ergebnis erhielten die Forscher eine neue Verbindung, die speziell das Immunoproteasom hemmt und auf das konstitutive Proteasom kaum Einfluss hat.
Die Besonderheit des entdeckten Mechanismus erklärt Erstautor Christian Dubiella: "Normalerweise verstopfen Inhibitoren das aktive Zentrum des Enzyms und legen somit dessen Funktion lahm. Die von uns synthetisierte Substanz jedoch bindet an ihr Ziel, veranlasst das aktive Zentrum, sich selbst zu zerstören, und spaltet sich nach verrichteter Arbeit wieder ab." Vor allem Einblicke in den atomaren Mechanismus, welcher mittels Röntgenstrukturanalyse aufgeklärt wurde, ermöglicht die maßgeschneiderte Entwicklung von neuen Immunoproteasom-Inhibitoren. Damit könnte der Weg für eine zukünftige Generation an Wirkstoffen offen stehen.