Neues Wirkprinzip für Kaliumkanäle entdeckt
Nervenzellen übertragen Informationen mithilfe von speziell für Kaliumionen durchlässigen Kanälen. Defekte Kaliumkanäle sind für Epilepsie und Depression mitverantwortlich. Die Forscher um Prof. Henning Stahlberg vom Biozentrum der Universität Basel ermittelten nun erstmals die vollständige 3-D-Struktur eines Kaliumkanals des Typs HCN. Daraus konnten sie Rückschlüsse über den Wirkungsmechanismus gewinnen, welchen sie in der aktuellen Ausgabe von «Nature Communications» beschreiben.

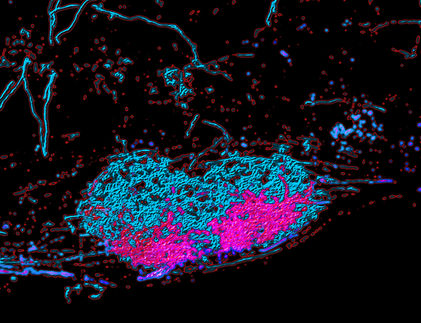
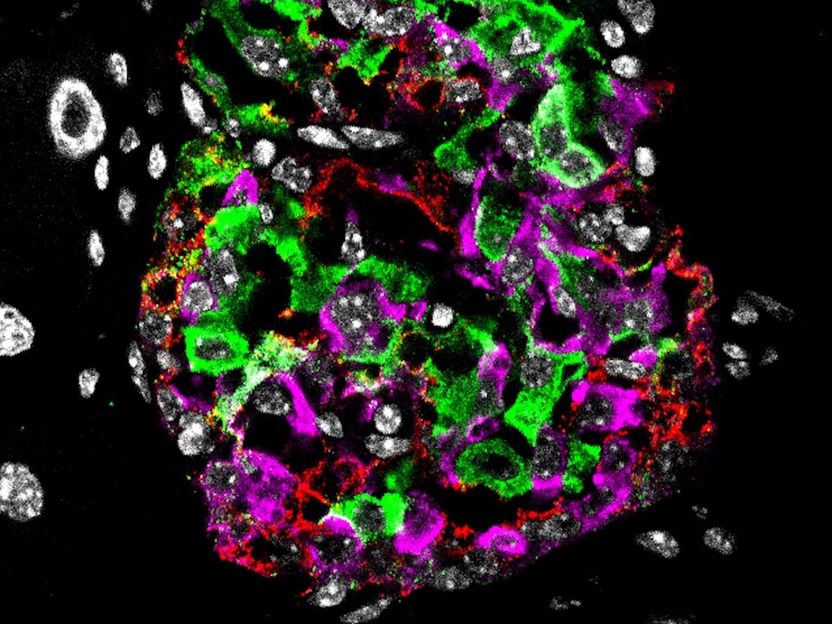
3-D-Modell von mehreren nebeneinander angeordneten HCN-Kaliumkanälen.
University of Basel
Nervenzellen leiten Informationen über elektrische Impulse durch unseren Körper. Ein zentrales Bauelement dieses elektrischen Schaltkreises sind Kaliumkanäle, die entweder durch einen Impuls oder auch durch Signalmoleküle gesteuert werden. Beim Menschen werden Fehlfunktionen solcher sogenannter HCN-Kaliumkanäle mit neuronalen Erkrankungen wie Epilepsie und Depression in Verbindung gebracht. Die Forschungsgruppe um Prof. Henning Stahlberg vom Biozentrum der Universität Basel hat nun erstmals die komplette Struktur eines bakteriellen Pendants dieser Art von Kaliumkanälen aufgeklärt und neue Hinweise auf deren Funktionsweise erhalten.
Neues Wirkprinzip dank 3-D-Struktur
Kaliumkanäle sind in der Membran von Zellen verankert. Sie bilden eine Pore mit einem Filter, der ausschliesslich für Kaliumionen durchlässig ist und durch das Signalmolekül cAMP gesteuert wird. Bisher ging man davon aus, dass sich die Pore öffnen und schliessen kann und so den Fluss der Kaliumionen reguliert. Stahlbergs Team fand nun Anhaltspunkte für ein anderes Wirkprinzip. Die Forscher rekonstruierten mithilfe von Kristallisationstechniken und der Elektronenmikroskopie die intakte dreidimensionale Struktur des bakteriellen Kaliumkanals in seiner natürlichen Umgebung in An- und Abwesenheit von cAMP.
Anhand dieser Strukturanalysen konnten sie feststellen, dass die Pore entgegen der landläufigen Meinung immer geöffnet ist. «Wenn das Signalmolekül cAMP an den Kaliumkanal andockt, kommt es zu Umlagerungen und Verschiebungen im Proteingerüst», erläutert Julia Kowal, Erstautorin der Studie. «Wir vermuten, dass cAMP stattdessen den Filter etwas weitet und damit den Durchfluss der Kaliumionen regelt.» Die neuen strukturellen Details ermöglichten den Forschern, die Funktionsweise dieser Kanäle aus einem anderen Blickwinkel zu betrachten.
Mechanismus relevant für neue Wirkstoffe
Stahlberg möchte nun die Filterregion mit einer extrem hoch auflösenden Kamera genauer untersuchen, um auch die letzten Fragen über den Mechanismus zu klären. Signalgesteuerte Kaliumkanäle werden auch als «Schrittmacher-Kanäle» bezeichnet. Sie steuern den Herzrhythmus sowie die rhythmische Erregbarkeit von Neuronen. Das genaue Verständnis des Wirkmechanismus ist daher die Grundlage für die Entwicklung spezifischer Arzneistoffe zur Behandlung von Epilepsie oder Herzrhythmusstörungen.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.