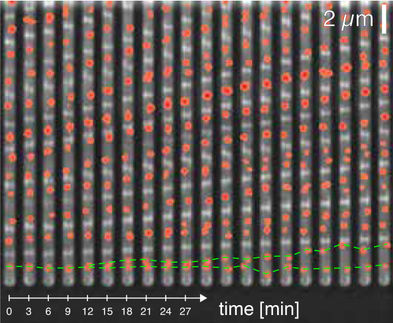
Neue Methode zur Visualisierung bakterieller Kommunikation
Forschende der Universität Basel haben eine Fluoreszenzmarkierung entwickelt, mit der sich bakterielle Kommunikationswege in lebenden Zellen darstellen lassen. Die Kommunikation zwischen Bakterienzellen ist wesentlich für die Steuerung von Prozessen innerhalb von Bakterienpopulationen, wie zum Beispiel der Bildung von Biofilmen.
An «Quorum Sensing» beteiligt: Selektive Markierung des Rezeptors CepR im Bakterium Burholdedia cenocepacia.
Illustration aus José Gomes et al., «Fluorescent Labeling Agents for Quorum-Sensing Receptors (FLAQS) in Live Cells» Chem. Eur. J. 2013, 19. Copyright Wiley-VCH Verlag GmbH & Co. KGaA. Reproduced with permission.
Die meisten Bakterien können miteinander kommunizieren, indem sie Signalmoleküle absondern. Übersteigt die Konzentration der Signale eine bestimmte Schwelle («ein Quorum»), erkennen die Bakterien, dass sich in der Nähe genügend Artgenossen befinden, um eine koordinierte Aktion auszulösen. Erst dann werden die Gene aktiviert, welche etwa zur Bildung von Biofilmen führen oder krank machende Virulenzfaktoren freisetzen. Über dieses sogenannte «Quorum Sensing» (QS) stimmen Bakterien ihr Verhalten ab und steuern Prozesse, von denen die gesamte Population profitiert.
Bei vielen Bakterienarten erfolgt die Verständigung über kleine Signalmoleküle, meist N-Acyl-L-homoserinlactone (AHL), welche die Bakterienzellen in die Umgebung abgeben. Dort können sie von anderen Zellen leicht aufgenommen werden und bei einer gewissen Konzentration innerhalb der Zelle an spezifische QS-Rezeptoren binden.
Nachweis des Rezeptors durch Fluoreszenzmarkierung des Signalstoffs
Den Forschungsgruppen um Prof. Karl Gademann (Universität Basel) und Prof. Leo Eberl (Universität Zürich) ist es nun gelungen, die Zell-Zell-Kommunikation an lebenden Zellen sichtbar zu machen. Dazu hängten die Forscher an den natürlichen AHL-Signalstoff einen fluoreszierenden Baustein an. In Tests an Bakterienkulturen konnten sie zeigen, dass das modifizierte Signalmolekül spezifisch an einen QS-Rezeptor aus dem Bakterium Burkholderia cenocepacia bindet.
Dieses Bakterium ist Teil einer Bakteriengruppe, die Biofilme innerhalb der Lunge bildet und so vor allem bei immungeschwächten oder an zystischer Fibrose erkrankten Patienten schwere Komplikationen wie zum Beispiel eine Lungenentzündung hervorrufen kann.
Die Forscher konnten den Rezeptor auch in einer natürlichen Population von B. cenocepacia nachweisen. Hier konkurriert der natürliche AHL-Botenstoff mit dem künstlichen Gegenstück um die Bindung am Rezeptor. Die Fluoreszenzmarkierung war gleichmässig über die ganze lebende Zelle verteilt, wodurch der Rezeptor erstmals im Cytoplasma lokalisiert werden konnte.
Breite Anwendungsmöglichkeiten
Mithilfe des fluoreszenzmarkierten AHL-Analogons ist ein einfacher Nachweis der QS-Rezeptoren in lebenden Zellen möglich. Insofern ist für diese neue Methode eine breite Anwendung denkbar, etwa als schneller Test, mit dem sich Quorum Sensing in verschiedenen Milieus oder in klinischen Proben nachweisen lässt. Zudem eröffnen sich neue Wege für ein tieferes Verständnis der Kommunikation innerhalb einer Bakterienpopulation oder zwischen einem Bakterium und seinem Wirt.