Tanz der Wassermoleküle macht Feuerkäfer zum Frostschutzkünstler
Wasserdynamik vermittelt Interaktion zwischen Proteinen und Eiskristallen
Bestimmte Pflanzen und Tiere schützen sich mit Frostschutzproteinen vor Temperaturen unter dem Gefrierpunkt. Wie die Larve des Käfers Dendroides Canadensis es schafft, Temperaturen bis zu -30 Grad Celsius zu trotzen, berichtet ein internationales Forschungsteam um Prof. Dr. Martina Havenith vom Lehrstuhl für Physikalische Chemie II der Ruhr-Universität. Gemeinsam mit amerikanischen Kollegen zeigten die RUB-Wissenschaftler, dass Interaktionen zwischen den Frostschutzproteinen und Wassermolekülen entscheidend zum Kälteschutz beitragen. Bislang ging man davon aus, dass der Effekt nur über den direkten Kontakt der Proteine mit Eiskristallen erreicht wird. Die Ergebnisse erzielte das Team mit einer Kombination von Terahertz-Spektroskopie und molekulardynamischen Simulationen.
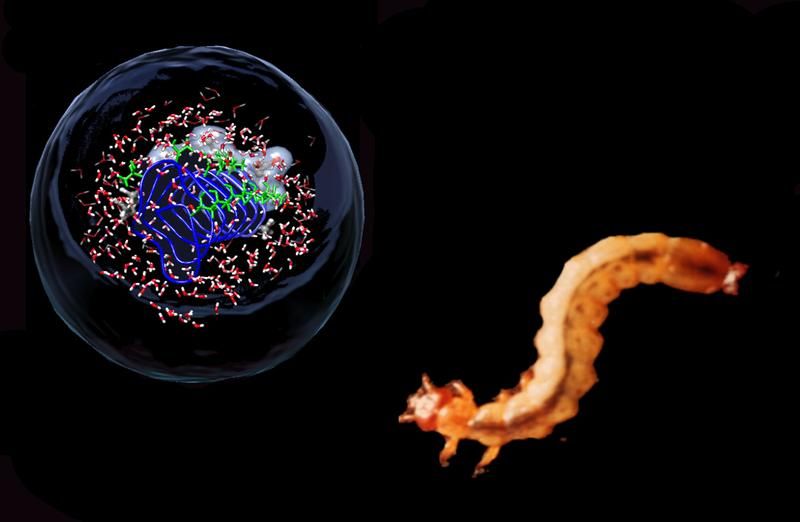
Wasserdynamik gezielt verändern: Das Antifreeze-Protein (blau) der Feuerkäfer-Larve verändert an der Eisbindungsfläche mit Threonin-Seitenketten (grün) die Dynamik des Wassers.
Grafik: Konrad Meister

Antifreeze-Proteine gewinnen: Um in Zukunft weitere Antifreeze-Proteine untersuchen zu können, ist Erstautor Konrad Meister (rechts) in der Antarktis auf Fischfang-Expedition unterwegs.
Foto: Konrad Meister

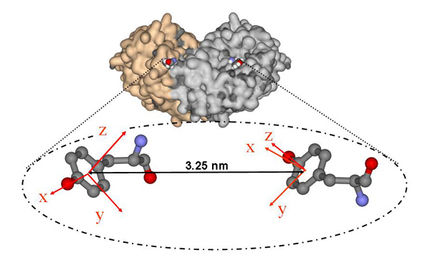
Protein-Eis-Interaktion: lokal und über größere Distanz
Die Struktur der Feuerkäfer-Frostschutzproteine ähnelt einem dreieckigen Prisma. Die Eisbindungsfläche des "Prismas" enthält viele exponierte Seitenketten, da die Reste der Aminosäure Threonin hier aus der Oberfläche ragen. An diese Reste binden Eiskristalle. Bislang ging man davon aus, dass die "Antifreeze"-Proteine nur lokal mit Nanoeiskristallen interagieren und so verhindern, dass sich größere Eiskristalle bilden. Die internationale Forschergruppe zeigte jedoch, dass über die Wassermoleküle zwischen Proteinen und Eiskristallen auch eine Interaktion über größere Distanzerfolgt, die zum Gefrierschutz beiträgt.
Die Dynamik der Wassermoleküle ist für den Gefrierschutz wichtig
In der Nähe der Eisbindungsfläche beobachteten die Wissenschaftlerinnen und Wissenschaftler eine deutlich verlangsamte Bewegung der Wassermoleküle, welche sich signifikant von den Wasserbewegungen an den nicht-eisbindenden Seiten des Proteins sowie des freien Wassers unterschied. Je tiefer die Temperatur, desto langsamer war die Wasserbewegung. "Wir vermuten, dass die beruhigte Wasserbewegung an der Bindungsfläche des Proteins das Andocken der Nanoeiskristalle erleichtert", spekuliert Martina Havenith. Dazu passt, dass die Forscher in einer inaktiven Mutante des Antifreeze-Proteins kaum verlangsamte Wasserbewegung fanden.
Effizienter als bei Fischen
Die Gefrierschutzproteine des Feuerkäfers sind zehn bis hundert Mal aktiver als die von arktischen und antarktischen Fischen, die sich gegen Temperaturen von -1,9 Grad Celsius schützen müssen. Diese hohe Gefrierschutzaktivität erreichen die Insekten durch die Kombination der zwei Strategien: direkte Interaktion zwischen Proteinen und Eis und Interaktion über Wassermoleküle.
Rolle der Lösungsmittel beachten
"Die besondere Rolle des Wassers beim natürlichen Frostschutz ist ein exzellentes Beispiel dafür, dass man bei der Betrachtung der Funktion eines Biomoleküls nicht nur seine 3D-Struktur, sondern seine gesamte Umgebung berücksichtigen muss - insbesondere das Lösungsmittel, in diesem Fall Wasser", sagt Prof. Havenith.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!

Themenwelt Spektroskopie
Durch die Untersuchung mit Spektroskopie ermöglicht uns einzigartige Einblicke in die Zusammensetzung und Struktur von Materialien. Von der UV-Vis-Spektroskopie über die Infrarot- und Raman-Spektroskopie bis hin zur Fluoreszenz- und Atomabsorptionsspektroskopie - die Spektroskopie bietet uns ein breites Spektrum an analytischen Techniken, um Substanzen präzise zu charakterisieren. Tauchen Sie ein in die faszinierende Welt der Spektroskopie!