Gefährliches Bakterium bekommt kalte Füße
Helmholtz-Forscher entwaffnen den nächsten Verwandten des Pesterregers
In Europa entvölkerte die Pest einst ganze Landstriche, in Afrika, Südamerika und Indien tritt sie noch heute immer wieder auf. Die Erreger der Seuche sind Bakterien der Gattung Yersinia. Etwas weniger aggressive Verwandte dieses Erregers lösen auch in Deutschland jedes Jahr mehrere Tausend Fälle von Durchfallerkrankungen mit teilweise schweren Folgeerscheinungen aus. Wissenschaftler des Braunschweiger Helmholtz-Zentrums für Infektionsforschung (HZI) haben gemeinsam mit Kollegen der Ruhr-Universität Bochum einen Mechanismus entdeckt, wie diese Bakterien ihre Waffen im Wirt anschalten. Der Trick: Yersinien besitzen ein molekulares Thermometer, das nur bei 37 Grad Celsius das krankmachende Programm der Bakterien startet.
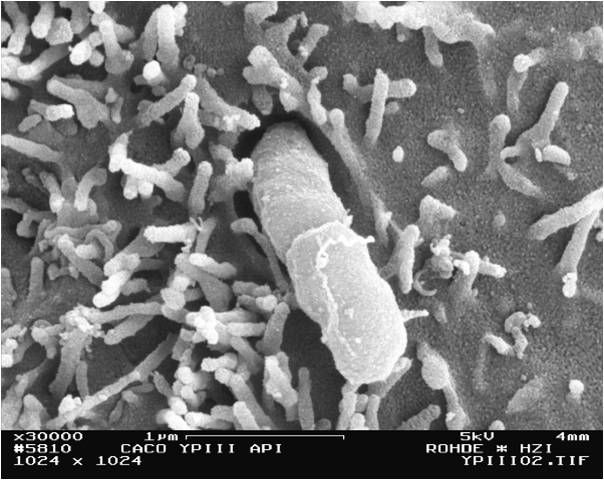
Yersinia pseudotuberculosis auf einer eukaryotischen Zelle
HZI / Manfred Rohde
Den HZI-Forschern gelang es nun, erstmals über genetische Veränderungen das Thermometer dauerhaft auf eine zu niedrige Temperatur einzustellen, bei der die Bakterien inaktiv bleiben. Das nächste Ziel ist es, einen Wirkstoff zu entwickeln, der genau diese Funktion erfüllt und als alternatives Medikament zu den gängigen, jedoch immer häufiger wirkungslosen Antibiotika eingesetzt werden kann.
Als Modellorganismus diente den HZI-Forschern Yersinia pseudotuberculosis, der nächste Verwandte des Pesterregers. In Deutschland werden vor allem Kleinkinder mit diesem Bakterium infiziert – meist durch den Verzehr von rohem oder nicht ausreichend gegartem Schweinefleisch. „Nach der Aufnahme merkt der Erreger durch den Temperaturwechsel, dass er jetzt im Menschen ist“, erklärt Dr. Katja Böhme aus der Abteilung „Molekulare Infektionsbiologie“ am HZI. „Im Dünndarm finden die Yersinien dann bestimmte Andockzellen, an die sie mit Rezeptoren binden und so eine Aufnahme ins Gewebe erzwingen,“ ergänzt Böhmes Kollegin Rebekka Steinmann. Ist den Bakterien der Eintritt ins Gewebe gelungen, schalten sie ihr Programm um: Nun produzieren sie Faktoren, mit denen sie die Angriffe des menschlichen Immunsystems abwehren und sogar Immunzellen töten können. Als Schalter dient dabei das erwähnte molekulare Thermometer. Außerhalb des Körpers blockiert der Regulator YmoA das Anti-Immunprogramm von Yersinia. Bei Körpertemperatur wird YmoA jedoch inaktiviert: Dies sorgt dafür, dass Yersinia „auf Angriff schaltet“. Als Teil des erwähnten Anti-Immunprogramms wird das Gen des Hauptregulators LcrF angeschaltet: Dieser wiederum löst die Produktion einer ganzen Reihe von krankmachenden Faktoren von Yersinia aus.
Auf dem Weg zu jedem Genprodukt, also auch der bakteriellen Vielzweckwaffe LcrF, entsteht immer zuerst eine sogenannte mRNA: Sie ist eine molekulare Matrize, eine mobile Abschrift des Gens, an die sich die Maschinerie der Proteinproduktion anheften kann. Bei LcrF muss jedoch auch hierfür erst die Temperatur stimmen: Ist die Umgebung kälter als 37 Grad, faltet sich die mRNA-Matrize zusammen, bildet eine Art Knäuel und ist für die Proteinproduktion unzugänglich – das Abwehrprogramm der Bakterien bleibt ausgeschaltet.
„Wir konnten die Temperaturkontrolle von LcrF gleich auf zwei Ebenen beeinflussen“, sagt Böhme. „Zunächst haben wir die Menge von YmoA künstlich gesteigert und so auch das Gen für den Regulator LcrF inaktiviert.“ Das allein reicht allerdings nicht aus, um den Erreger unschädlich zu machen: Die Wissenschaftler konnten trotzdem noch eine Rest-Aktivität von LcrF nachweisen, die auf bereits vorher gebildete mRNAs zurückging. Computersimulationen der mRNA-Moleküle zeigten den Forschern, welche Bereiche für die Faltung und Entfaltung besonders wichtig sind. „Wir haben dann einzelne Bausteine der LcrF-Matrize ausgetauscht, sodass sie sich auch bei 37 Grad nicht mehr entfalten konnte. Die Bakterien waren dadurch nicht mehr in der Lage, ihr Abwehrprogramm zu starten und konnten vom Immunsystem beseitigt werden“, erklärt Steinmann.
Bisher waren molekulare Thermometer nur bei der Anpassung an Hitzestress bekannt. Bei der Kontrolle wichtiger Gene von Krankheitserregern sind sie jedoch eine Neuentdeckung. „Hier eröffnet sich eine ganz neue Möglichkeit, um Infektionen zu bekämpfen“, sagt Prof. Petra Dersch, Leiterin der Abteilung „Molekulare Infektionsbiologie“ am HZI. „Ein Molekül, das die mRNA von LcrF wie eine Klammer zusammenhält, würde die Yersinien inaktivieren und sie so dem Immunsystem ausliefern. Außerdem würde ein solcher Wirkstoff ausschließlich die krankmachenden Yersinien treffen, da nur sie das Waffensystem kontrollieren – es wäre also auch ein geeigneter Wirkstoff zur Bekämpfung der Pest.“
Ein generelles Problem in der Bekämpfung von Infektionen ist die ständige Veränderung der Krankheitserreger. Daher suchen die Infektionsforscher heute nach universellen Schwachstellen, also nach Eigenschaften oder Mechanismen, die für die Erreger grundlegend und unverzichtbar sind. „Unser Ziel ist es, Krankheitserreger zu entschärfen, ohne wie die gängigen Antibiotika gleichzeitig auch nützliche Bakterien zu beseitigen. Molekulare Thermometer, die die Virulenz von krankmachenden Bakterien kontrollieren, sind dafür ein geeigneter Angriffspunkt“, sagt Dersch.
Originalveröffentlichung
Böhme K, Steinmann R, Kortmann J, Seekircher S, Heroven AK, Berger E, Pisano F, Thiermann T, Wolf-Watz H, Narberhaus F, and Dersch P: Concerted actions of a thermo-labile regulator and a unique intergenic RNA thermosensor control Yersinia virulence. PLoS Pathogens, February 2012, Volume 8, Issue 2.