Forschung ohne Tierversuche
Die Krebsforscherin Dr. Irina Nazarenko und der Ingenieur Dr. Stefan Giselbrecht vom KIT erhalten vom Verein Ärzte gegen Tierversuche einen Wissenschaftspreis für tierversuchsfreie Krebsforschung. Ausgezeichnet werden die beiden Forscher für ihre Modellierung des Wachstums menschlicher Zellen auf mikrostrukturierten Biochips, mit der sie die Abläufe bei der Metastasierung von Brustkrebs in Knochengewebe untersuchen. Die Ergebnisse des Projekts im Rahmen des BioGrenzflächen (BioInterfaces) Programms sollen neue Ansätze für die Steuerung des Stammzellverhaltens und für innovative Krebstherapien ermöglichen.
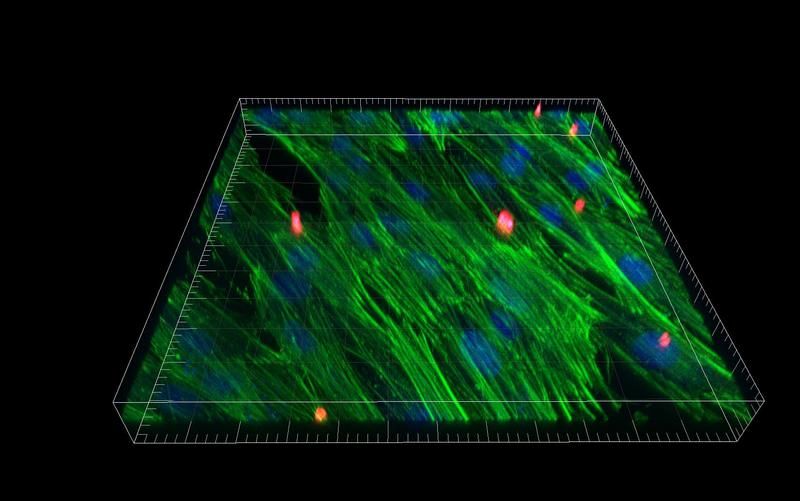
Zellwachstum in folienbasierten Mikrochips.
Jochen Dindorf, Alexandra Baumann und Maximilian Preissler
Mit dem Preis zeichnet der Verein Ärzte gegen Tierversuche Arbeiten zur Krebsforschung aus, die ganz auf die Verwendung von Tieren und tierischem Material verzichten – auch Nährmedien für Zellkulturen und Antikörper sind synthetisch hergestellt. Der Preis ist mit 10 000 Euro dotiert. „Es freut uns, Wissenschaftler zu fördern, deren Forschungsarbeiten auf den Menschen bezogene tumorspezifische Untersuchungen ermöglichen und die ohne jedes Tierleid auskommen“, sagt die Biologin Silke Bitz von der Ärztevereinigung.
Die KIT-Wissenschaftler Dr. Irina Nazarenko vom Institut für Toxikologie und Genetik (ITG) und Dr. Stefan Giselbrecht vom Institut für Biologische Grenzflächen (IBG 1) verbinden in ihrem interdisziplinären Projekt des Programms BioGrenzflächen Methoden der Zellforschung und der Ingenieurwissenschaften. Sie erforschen, wie
Metastasen eines Tumors entstehen, indem sie die Kommunikation zwischen Zellen untersuchen. Bei der Metastasierung spielt die Bildung sogenannter prä-metastatischer Nischen eine entscheidende Rolle: Tumorzellen können offenbar normale Zellen des Körpers so verändern, dass in bestimmten Organen, wie in der Lunge, in der Leber und in den Knochen, sozusagen ein fruchtbarer Boden vorbereitet wird. In diesen prä-metastatischen Nischen können sich zirkulierende Tumorzellen ansiedeln, um Metastasen zu bilden.
Die Forschungsteams von Nazarenko und Giselbrecht untersuchen die noch unbekannten molekularen Mechanismen der Kommunikation zwischen Tumorzellen und zwischen dem Tumor und dem Körper des Patienten, speziell den adulten Stammzellen. Dabei geht es vor allem um die gezielte Steuerung des Stammzellvehaltens mithilfe von zellulärer Kommunikation. Die Forscher entwickeln dafür ein Modell der prä-metastatischen Nische des Brustkrebses (Mammakarzinom) im Knochengewebe Sie kultivieren menschliche Zellen auf mikrostrukturierten Biochips in Bioreaktoren. So stellen sie die Abläufe bei der Interaktion zwischen Zellen und der Nische in Knochengewebe lebensecht dar.
Um ein Modell des Knochenmarks zu entwickeln, setzen die beiden KIT-Forscher neue folienbasierte mikrostrukturierte Zellkulturmatrizen und miniaturisierte Bioreaktoren ein und verwenden Ko-Kulturen aus menschlichen Zellen. Mithilfe von Chips bilden sie die Architektur des Knochens möglichst wirklichkeitsgetreu nach. Die Chips stellen sie über den von ihnen entwickelten SMART-Prozess (Substrate Modification And Replication by Thermoforming) her. Um die Aktivierung von Stammzellen des Knochenmarks durch von Tumorzellen produzierte Botenstoffe, wie lösliche Moleküle oder Membranbläschen, zu untersuchen, werden Nazarenko und Giselbrecht Bioreaktoren mit zwei integrierten Chips verwenden, die durch eine poröse Membran getrennt sind. Im ersten Chip kultivieren sie die Modelle des Knochenmarks, im zweiten Chip Tumorzellen des menschlichen Mammakarzinoms.
Diese Arbeiten im interdisziplinären Umfeld des KIT und des Programms BioInterfaces ermöglichen erstmals, das natürliche Interface der prä-metastatischen Nische unter kontrollierten Bedingungen in vitro zu beobachten und zu steuern. Nazarenko und Giselbrecht entwickeln ihr Modell als Vorreiter im Bereich der anwendungsorientierten Mikro- und Nanotechnologien. Darauf basierend soll künftig auch die Modellierung von Nischen in anderen Organen und für verschiedene Tumorarten möglich sein. Erkenntnisse über die Abläufe bei der Bildung der prä-metastasischen Nische und deren gezielte Steuerung sind wesentlich für die Entwicklung neuer Therapien gegen Metastasen.
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
 Neu
Neu
Flexcell Zelldehnungsbioreaktoren für zelluläre Biomechanik-Anwendungen von Dunn
Flexcell Zelldehnungsbioreaktoren für zelluläre Biomechanik-Anwendungen
Wurde in über 1300 Labors weltweit verwendet und in über 9000 Forschungspublikationen zitiert.

Biostat STR von Sartorius
Biostat STR Bioreaktoren der Generation 3
Entwickelt für ultimative Upstream-Leistung

Ambr® 250 Modular von Sartorius
Mini-Bioreaktoren für Zell- und Gentherapien mit hoher Skalierbarkeit
Maximieren Sie Ihre Prozessentwicklung mit zuverlässigen Einweg-Gefäßen

Ambr® 250 HT Consumables von Sartorius
Effiziente Bioprozesse mit Einweg-Bioreaktoren
Minimieren Sie Reinigungsaufwand und maximieren Sie Flexibilität für Zell- und Mikrobiolkulturen

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte
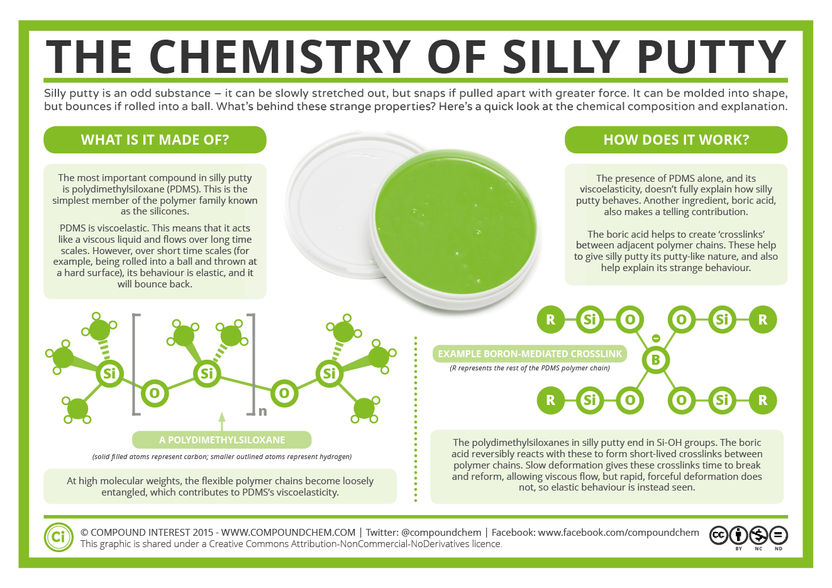
The Chemistry of Silly Putty
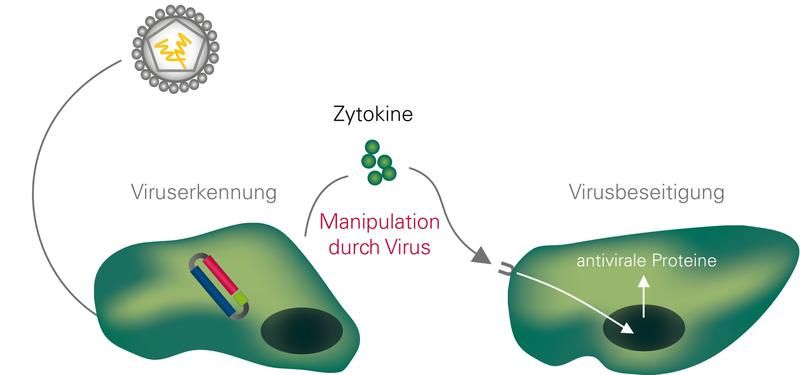
Schwachstellen der menschlichen Abwehr - Max-Planck-Forscher untersuchen Angriffsstrategien von Viren
Studie: Deutsche Forscher kehren in ihr Heimatland zurück - Nur 36 von 548 Wissenschaftlern blieben in den USA

IMGM Laboratories GmbH - Martinsried, Deutschland
Hochleistungsbakterium für die weiße Biotechnologie - Studie über Pseudomonas putida erhält BMBF-Förderung

Sevion Therapeutics - San Diego, USA

Wenn runzlige Falten gut sind: Schrumpelig aussehende Bakterien sind am besten an ihren Wirtsorganismus angepasst

Primm GmbH - Dübendorf, Schweiz

Eppendorf Austria GmbH - Wien, Österreich

Chemiker nutzen Treibhausgas zur Herstellung eines Wirkstoffs gegen Schlafkrankheit - Mit Flow-Chemie Fluoroform sinnvoll nutzen





















































