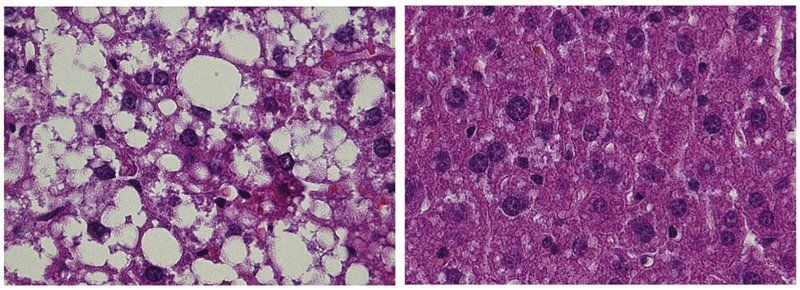
Warum Sichelzellenanämie vor Malaria schützt - Mechanismus aufgeklärt
Eine Mutation ist nicht zwangsweise schlecht, sie kann auch Leben retten. So schützt eine Mutation der roten Blutkörperchen, die sogenannte Sichelzellenanämie, sogar vor Malaria und den schwerwiegenden Folgen. Wie das funktioniert war unklar. Die molekularen Mechanismen wurden jetzt erst aufgedeckt, von einem Forscherteam der Universitäten in Oeiras (Portugal), Leipzig und Paris. Malaria fordert weltweit jährlich über eine Million Todesopfer. Die neuen Erkenntnisse bringen erste Ansätze für eine Therapie der lebensgefährlichen Malariafolgen, wie Malariaencephalitis, an der besonders häufig Kinder sterben.
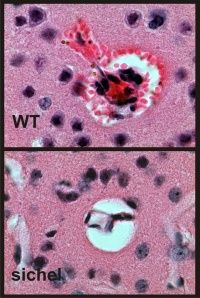
Schädigung der Blut-Hirn-Schranke bei Malaria. (Sichtbar sind Erythrozyten, die durch geschädigte Gefäßwände gedrückt wurden. Das bei ihrem Abbau entstehende Eisen sieht man als braune Pünktchen in Fresszellen.)
Die Sichelzellenanämie ist eine Erbkrankheit. Durch einen Gendefekt wird bei den Betroffenen ein abnormales Hämoglobin, bestehend aus dem Farbstoff Häm und einem Eiweißmolekül, als Bestandteil der roten Blutkörperchen gebildet. Das führt dazu, dass sich die Blutzellen verändern und sichelförmig werden. Das kann bei einer schweren Ausprägung zur gefährlichen Verstopfung von Blutgefäßen führen, bei leichter Ausprägung aber interessanterweise auch gegen Malaria helfen. Besonders in Gebieten in denen Malaria epidemieartig auftritt, gibt es daher evolutionär bedingt vermehrt Menschen die genau diese Mutation und damit eine Sichelzellenanämie aufweisen, besonders viele in Afrika.
Gewebeschutz statt direkter Erregerbekämpfung
Bis jetzt gab es verschiedene Theorien darüber, wie diese Resistenz gegen Malariaerreger – Einzeller, genannt Plasmodien, die durch Stiche der Anophelesmücke übertragen werden – zu Stande kommen könnte. "Man hatte vermutet, dass die Erreger im Blut von Sichelzellträgern stärker und damit erfolgreicher bekämpft werden", erklärt Professor Ingo Bechmann, beteiligt an der Veröffentlichung und Direktor des Instituts für Anatomie an der Medizinischen Fakultät der Universität Leipzig. "Das stimmt aber so nicht. Das Geheimnis liegt eher in einer Malaria-Toleranz des Immunsystems von Sichelzellträgern – ein völlig unerwartetes Ergebnis. Die Erreger werden zwar erstens vom Immunsystem bekämpft, wie beim Gesunden auch, aber zweitens gibt es bei Sichelzellträgern einen zusätzlichen Mechanismus der den Körper vor den entzündlichen Prozessen schützt, die das Immunsystem automatisch bei einer Malariainfektion mit auslöst. Eine gefährliche Malariaencephalitis, eine schwere Entzündung im Gehirn, wird beispielsweise gar nicht erst in Gang gesetzt."
Kohlenstoffmonoxid verhindert entzündliche Immunreaktionen
Das Gefährliche an der Malariaerkrankung sind genau diese entzündlichen Prozesse. Denn die Erreger befallen rote Blutkörperchen, vermehren sich in ihnen und bringen sie anschließend zum platzen. Dabei werden massenweise neue Erregerzellen freigesetzt aber auch massenweise Abbauprodukte der roten Blutkörperchens. Darunter ist auch der Stoff Häm der den roten Blutzellen ihre rote Farbe verleiht, der aber, einmal freigesetzt, im Organismus toxisch wirkt und die typischen Fieberschübe und Entzündungsprozesse auslöst. Das Immunsystem läuft Sturm. Hier greift der Schutzmechanismus von Sichelzellträgern: Denn das mutierte Sichelzell-Hämoglobin bewirkt die pausenlose Produktion eines Enzyms, der Hämoxidase1. Dieses Enzym zerstört den giftigen Farbstoff Häm, sobald der frei im Blut zirkuliert und spaltet ihn in ungiftige Bestandteile, darunter der gasförmige Transmitter Kohlenstoffmonoxid (CO). Dieses Gas wiederum wirkt zurück auf die Stellen im Hämoglobinmolekül der roten Blutkörperchen an der der Farbstoff Häm sitzt und verhindert dort, dass er sich ablösen kann. Er wird also nicht mehr übermäßig ins Blut freigesetzt, kann seine giftige Wirkung nicht mehr entfalten, also auch keine Entzündungsreaktionen wie die Malariaencephalitis auslösen.
Schutzeffekt via Rückenmark und Blutzellen
Ihre Ergebnisse erzielten die Wissenschaftler durch umfassende Experimentalreihen mit verschiedenen Blutmutanten-Stämmen von Mäusen. Sie verglichen den Krankheitsverlauf der unterschiedlichen Tiere, schwer (homozygot) und leicht (heterozygot) an Sichelzellanämie erkrankte Mäuse und gesunde Tiere, nach einer Infektion mit dem Malariaerreger Plasmodium falciparum. "Unsere Aufgabe in Leipzig war es, alle Mäuse pathologisch zu analysieren. Wir haben also geschaut ob und wo genau, und bei welcher Maus-Mutante Entzündungsreaktionen und damit Gewebeschädigungen auftraten."
Interessant war dabei, dass die Bildung des Enzyms Hämoxidase1 auch bei nicht sichelzellerkrankten Mäusen stattfindet, aber dort eben nur minimal und nicht fortwährend. Außerdem findet bei den Sichelzell-Mäusen die Bildung des Enzyms und damit des Kohlenstoffmonoxid besonders in blutbildenden Geweben statt, im Rückenmark und in den Blutzellen selbst.
Behandlungsmöglichkeiten in Sicht
"Weil nun klar ist, wie die Sichelzellenanämie natürlich gegen Malaria schützt, können wir uns diese Erkenntnisse für die Therapie von Malaria zunutze machen. Wir wollen den natürlichen Gewebeschutzmechanismus durch Kohlenstoffmonoxid künstlich nachahmen", erklärt Professor Bechmann. "Das würde besonders Kindern das Leben retten. Sie erkranken häufig an den schlimmsten Begleiterscheinungen von Malaria, auch an Malariaencephalitis." Wie die Erkenntnisse klinisch umgesetzt, die Erkrankten also behandelt werden können, soll nun in Anschlussprojekten herausgefunden werden.
Originalveröffentlichung
Ferreira, A., et al. Sickle Hemoglobin Confers Tolerance to Plasmodium Infection. Cell 2011.