Alzheimer-Mäuse: Gedächtnisverlust durch Tau-Proteine ist umkehrbar
Max-Planck-Studie macht Hoffnung auf wirksame Therapien
Ablagerungen des Amyloid-beta- und des Tau-Proteins im Gehirn sind das charakteristische Merkmal von Morbus Alzheimer. Vor allem der Hippocampus ist davon betroffen, eine für Lernen und Gedächtnis zentrale Region. Offenbar verschwindet aber die giftige Wirkung des Tau-Proteins wieder weitgehend, wenn das entsprechende Tau-Gen abgeschaltet wird. Forscher von den Max-Planck Arbeitsgruppen für Strukturelle Molekularbiologie am DESY in Hamburg konnten zeigen, dass bei vormals „dementen“ Mäusen mit einem menschlichen Tau-Gen die Lernfähigkeit und Erinnerung zurückkehrt und sich Synapsen teilweise neu bilden, sobald das Gen inaktiv ist. Die Wissenschaftler testen nun Wirkstoffe gegen die Tau-Ablagerungen an Mäusen. Möglicherweise könnte damit der Gedächtnisverlust bei Alzheimer im frühen Stadium zumindest teilweise wieder rückgängig gemacht werden.
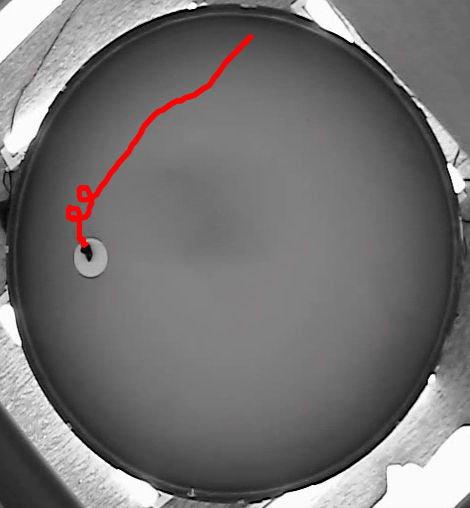
Maus mit abgeschalteter tau-Variante im Gedächtnistest.
© Max Planck-ASMB/Mandelkow
Während verklumptes Amyloid-beta zwischen den Nervenzellen unlösliche Knäuel bildet, verklumpt das Tau-Protein innerhalb der Neuronen. Das Protein stabilisiert röhrenförmige Proteine des Zellskeletts, die so genannten Mikrotubuli. Sie sind die "Schienen" für den Transport in Zellen. Bei Alzheimer wird Tau durch zu viele Phosphatgruppen funktionsunfähig und verklumpt. Dadurch bricht der Nährstofftransport zusammen, die Nervenzellen und ihre Synapsen sterben ab. Dies ist der Beginn des Gedächtnisverlustes.
Das Team von Eva und Eckhard Mandelkow von den Max-Planck Arbeitsgruppen für Strukturelle Molekularbiologie haben - zusammen mit Kollegen aus Leuven, Hamburg und Erlangen - Mäuse mit zwei verschiedenen menschlichen Tau-Genvarianten ausgestattet: Die eine Gruppe mit einer Form, die nicht verknäulen kann (anti-aggregant), und eine zweite mit dem Bauplan für die stark aggregierende Proteinvariante (pro-aggregant). Mäuse mit der ersten Form entwickelten keinerlei Alzheimer-Symptome. Nager mit pro-aggregant Tau wurden hingegen „dement“.
Die Wissenschaftler maßen diesen Gedächtnisverlust mit Hilfe eines Schwimmtests: Gesunde Mäuse lernen schnell in einem Wasserbassin die rettende, unter der Oberfläche liegende Plattform zu finden. Die transgenen Tiere dagegen, die ein zusätzliches Gen für die Bildung schnell aggregierenden menschlichen Tau-Proteins besitzen, paddeln dagegen ziellos durch das Bassin, ehe sie eher zufällig auf die kleine Insel treffen. Sie benötigen mehr als viermal so viel Zeit wie ihre gesunden Artgenossen. Doch schaltet man bei ihnen das mutierte toxische Gen wieder ab, schaffen sie es bereits ein paar Wochen später fast spielend, ihr Fell rasch ins Trockene zu bringen.
Überraschende Gewebsresultate
Gewebeuntersuchungen zeigten, dass bei der ersten Gruppe erwartungsgemäß keinerlei Tau-Klumpen entstanden waren. In der zweiten Gruppe – den „dementen“ Mäusen – bildeten sich hingegen Co-Aggregate aus menschlichem Tau und „Maus-Tau“. Normalerweise verklumpt das arteigene Tau-Protein von Mäusen aber gar nicht. „Noch erstaunlicher ist aber: Wochen nachdem das zusätzliche Gen abgeschaltet worden war, hatte sich das verklumpte menschliche Tau wieder aufgelöst – das „Maus-Tau“ blieb jedoch weiterhin verknäult. Trotzdem waren die Mäuse wieder fähig zu lernen und sich zu erinnern“, sagt Eckhard Mandelkow. Genauere Untersuchungen zeigten, dass sich bei ihnen sogar neue Synapsen gebildet hatten.
Die Wissenschaftler schließen daraus, dass mutiertes, also krank machendes Tau, gesundes Tau verändern kann. Offenbar wirkt es wie ein Kristallisationskeim – und das machte es so giftig für die Nervenzellen. „Die eigentliche Sensation ist jedoch, dass der Verlauf von Alzheimer umgekehrt werden kann. Zumindest in einem frühen Stadium der Erkrankung, noch bevor zu viele Neuronen zerstört sind“, sagt Eva Mandelkow, die zusammen mit ihrem Mann in diesem Jahr mit dem Potamkin-Preis 2011 für Alzheimer-Forschung der American Academy of Neurology ausgezeichnet wird.
Beim Menschen lässt sich das Verklumpen von Tau jedoch nicht einfach ausschalten wie bei den transgenen Mäusen. Aber spezielle Wirkstoffe könnten die Tau-Aggregate wieder auflösen. Die Hamburger Forscher haben bereits durch Screening von 200.000 Substanzen zwei Wirkstoffklassen gefunden, die Tau-Aggregate wieder in lösliches Tau verwandeln können. Sie werden nun im Tierversuch getestet.
Originalveröffentlichung
A. Sydow, A. Van der Jeugd, F. Zheng, T. Ahmed, D. Balschun, O. Petrova, D. Drexler, L. Zhou, G. Rune, E. Mandelkow, et al.; "Tau-induced Defects in Synaptic Plasticity, Learning and Memory are reversible in Transgenic Mice after Switching off the Toxic Tau Mutant"; Journal of Neuroscience.