Leberregeneration im "Trickfilm" - Forscher sind den Mechanismen der Leberregeneration auf der Spur
Wie die Leber es schafft, sich auch nach massiven Schäden wieder zu regenerieren, ist eine bedeutende Frage in der Medizin. Wissenschaftler von HepatoSys/GermanVirtual Liver Network sind den zugrunde liegenden Mechanismen auf die Spur gekommen. Es ist ihnen gelungen, die Regeneration von Leberläppchen in der Computersimulation zu verfolgen und die so erarbeiteten zentralen Prinzipien im Experiment zu bestätigen.
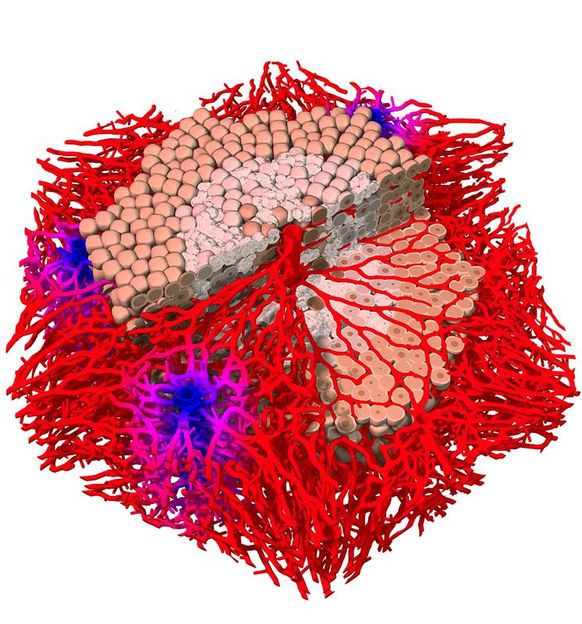
Computermodell eines Leberläppchens im Querschnitt Die Abbildung zeigt das dreidimensionale Lebermodell im Computer einige Stunden nach Vergiftung mit Tetrachlorkohlenstoff. Immer mehr Zellen im Zentrum des Läppchens sterben auf Grund der Vergiftung ab (dargestellt durch hellere Farbe). Ebenso zu sehen sind die sinusoidalen Blutgefäße (in rot) und die Portalgefäße (in blau).
Drasdo/Hoehme
Die neuen Einblicke in die Leberregeneration erlauben ein besseres Verständnis des Vorgangs - und öffnen die Tür für die Entwicklung neuer Therapie-Ansätze bei Leberzirrhose und anderen Schädigungen dieses lebenswichtigen Organs.
Einzigartig: die Leberregeneration
Die Leber ist ein ganz besonderes Organ: Selbst wenn sie - etwa nach Vergiftungen - zu mehr als fünfzig Prozent ihrer Gesamtmasse beschädigt ist, kann sie sich beinahe vollständig regenerieren. Diese Fähigkeit ist ebenso lebenswichtig wie erstaunlich. Die Leber ist das bedeutendste Stoffwechselorgan und hat unter anderem zur Aufgabe, das Blut zu entgiften. Damit sie dies leisten kann, ist sie mit einer höchst aufwändigen Anatomie ausgestattet: Beim Menschen setzten sich die beiden Leberlappen aus rund einer Million kleiner Leberläppchen von maximal einem bis zwei Millimetern Größe zusammen. Das in die Leber einströmende Blut tritt über das sogenannte Portalfeld, das benachbarte Leberläppchen voneinander trennt, in die Läppchen ein und fließt durch winzige Blutgefäße, die von Hepatozyten, dem häufigsten Zelltyp in der Leber, umgeben sind, zu einer zentral liegenden Vene, die das Blut wieder abführt. Diese spezielle Architektur stellt sicher, dass das Blut optimalen Kontakt zu den Hepatozyten hat, wenn es durch das Organ fließt.
Erholt sich die Leber nach einer Schädigung durch Medikamente, Alkohol oder einer Virusinfektion, gilt es, diesen komplexen Aufbau wieder herzustellen. Wie das gelingt ist noch weitgehend unverstanden. HepatoSys-Forscher um Dirk Drasdo, der am Interdisziplinären Zentrum für Bioinformatik in Leipzig (IZBI) und im nationalen französischen Institut für Forschung in Informatik und Automatisierung (INRIA) in Le Chesnay bei Paris arbeitet, haben es sich zur Aufgabe gemacht, der Leberregeneration mit computerbasierten systembiologischen Methoden auf den Grund zu gehen. Dazu simulierten sie im Computer das Szenario nach einer Vergiftung mit Tetrachlor-Kohlenstoff (CCl4) in der Mausleber - ein typisches Tiermodell für eine Paracetamolvergiftung beim Menschen.
Vom Gewebeschnitt in den Computer
Zunächst galt es, das Modell eines durchschnittlichen Leberläppchens im Computer darzustellen. In enger Zusammenarbeit mit den experimentell arbeitenden Kollegen um Jan Hengstler, Leibniz Institut und Universität Dortmund, erfassten die Wissenschaftler die notwendigen Parameter, die etwa Ausrichtung und Form der Blutgefäße beschreiben, sowie die Anordnung der Hepatozyten. Dazu nutzten sie Bildverarbeitungsmethoden, die es erlauben, Mikroskopiebilder von speziell präparierten Gewebeschnitten im Computer dreidimensional zusammenzusetzen und durch Kennzahlen zu beschreiben.
Im nächsten Schritt galt es, den Regenerationsprozess innerhalb der Leberläppchen von Mäusen zu erfassen. Den Tieren wurde zuvor die leberschädigende Substanz Tetrachlorkohlenstoff gespritzt, was - ähnlich einer Paracetamolvergiftung - zur Folge hat, dass Hepatozyten nahe der Zentralvene des Leberläppchens absterben. Dazu führten die Wissenschaftler sogenannte Prozessparameter ein. Sie erfassen wann und wo neue Hepatozyten entstehen, wohin sie im Organ wandern und wie sie sich anordnen, um die ursprüngliche Architektur des Leberläppchens wieder herzustellen. Schließlich entwickelten sie auf Basis sämtlicher Parameter des Leberläppchens ein mathematisches Modell, mit dem sich die räumliche Dynamik der einzelnen Hepatozyten und der Blutgefäße simulieren lässt. Damit gelang es den Wissenschaftlern, zentrale, bisher unbekannte Mechanismen während des Regenerationsvorgangs im Leberläppchen zu identifizieren. Wie sich herausstellte, entstehen die neuen Leberzellen nämlich nicht einfach irgendwo. "Vielmehr zeigte sich schnell, dass der Prozess in seiner räumlich-zeitlichen Dynamik nur dann funktionieren kann, wenn sich die neuen Hepatozyten entlang der Sinusoide orientieren, feinen Blutgefäßen, die das Leberläppchen durchziehen", erklärt Drasdos Mitarbeiter Stefan Höhme. Diese Beobachtung im Computermodell ließ sich anschließend auch im Laborexperiment mit echten Leberläppchen bestätigen. "Das bringt uns in unserem Verständnis der komplexen Vorgänge bei der Leberregeneration ein ganzes Stück weiter", so Höhme.
Nicht nur für die Leber
Ein derartiges dynamisches Modell eines Zellverbandes, das auch in der Lage ist, Vorhersagen zu treffen, sei bislang noch eine absolute Seltenheit, hebt Drasdo die Bedeutung der Arbeit hervor. "Es erfasst gleichzeitig einzelne Zellen, aber auch den gesamten Gewebeverband," sagt er. "Und das schafft die Grundlage, um nun auch die Signalprozesse innerhalb und zwischen den Zellen, die den Regenerationsprozess steuern, genauer zu untersuchen." Der Clou an der Sache: Nach dem selben Prinzip lassen sich auch Modelle für andere medizinisch relevante Fragestellungen erstellen, zum Beispiel um zu klären, wie sich ein Tumor im Körper ausbreitet. Ein Verständnis dieser dynamischen Vorgänge ebnet den Weg für neue, effektivere Therapieansätze, etwa um die Leber bei ihrer Regeneration zu unterstützen, oder Tumore am Wachstum zu hindern. "Unsere Arbeit war so nur möglich, weil wir mit den experimentell arbeitenden Kollegen um Jan Hengstler in Dortmund Hand in Hand arbeiten konnten," betont Drasdo, der sich schon seit vielen Jahren dem Modellieren von Zellen und Zellverbänden widmet. "Erst dadurch können wir unsere Erkenntnisse aus der Computersimulation direkt im Experiment prüfen und umgekehrt - und genau das macht Systembiologie aus."