Durchbruch in der Methan-Forschung: Aktivierungsmechanismus des Methan-produzierenden Enzyms entschlüsselt
„Nature“-Publikation offenbart die evolutionäre Verbindung zwischen zwei fundamentalen biologischen Prozessen
Forschende am Zentrum für Synthetische Mikrobiologie (SYNMIKRO) der Philipps-Universität Marburg und der TU Berlin haben einen bedeutenden Durchbruch im Verständnis der Aktivierung von Methyl-Coenzym-M-Reduktase (MCR) erzielt – dem Enzym, das für nahezu die gesamte biologische Methanproduktion verantwortlich ist und eines der am häufigsten vorkommenden Enzyme der Erde darstellt. Ihre Ergebnisse wurden nun in „Nature“ publiziert und werfen nicht nur ein neues Licht auf einen der ältesten Prozesse der Energiegewinnung in der Natur, sondern offenbaren auch eine unerwartete evolutionäre Verbindung zur sogenannten Stickstofffixierung.
In diesem ersten Schritt des globalen Stickstoffkreislaufs nehmen Mikroorganismen Stickstoff aus der Luft auf und wandeln ihn so um, dass Lebewesen ihn verwerten können. „Grundlagenforschung im Bereich der biologischen Energie- und Stoffumwandlung birgt ein erhebliches Potenzial, aktuelle Herausforderungen wie dem stetig wachsenden Energiebedarf der Menschheit und dem fortschreitenden Klimawandel zu begegnen“, erklärt Dr. Christian Lorent, Mitautor der „Nature“-Publikation und wissenschaftlicher Mitarbeiter des an der TU Berlin beheimateten Exzellenzclusters Unifying Systems in Catalysis (UniSysCat).
Die zwei Seiten des Treibhausgases
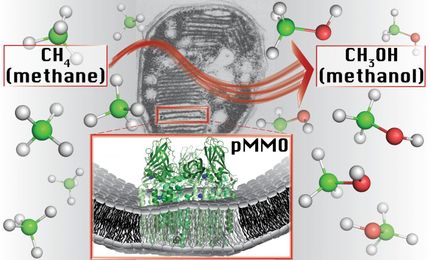
Methanogene Archaeen sind Mikroorganismen, die seit Milliarden von Jahren existieren und jährlich bis zu eine Milliarde Tonnen Methan zum Beispiel im Magen von Wiederkäuern oder in Feuchtgebieten produzieren. Obwohl Methan ein starkes Treibhausgas ist, das zur Erderwärmung beiträgt, birgt die biologische Methanproduktion auch großes Potenzial als erneuerbare Energiequelle durch die Gewinnung von Biogas in der Landwirtschaft. Ein tieferes Verständnis der grundlegenden Mechanismen der Methanbildung kann zu Fortschritten in nachhaltigen Energietechnologien und im Klimaschutz führen.
Eine der anspruchsvollsten Redoxreaktionen
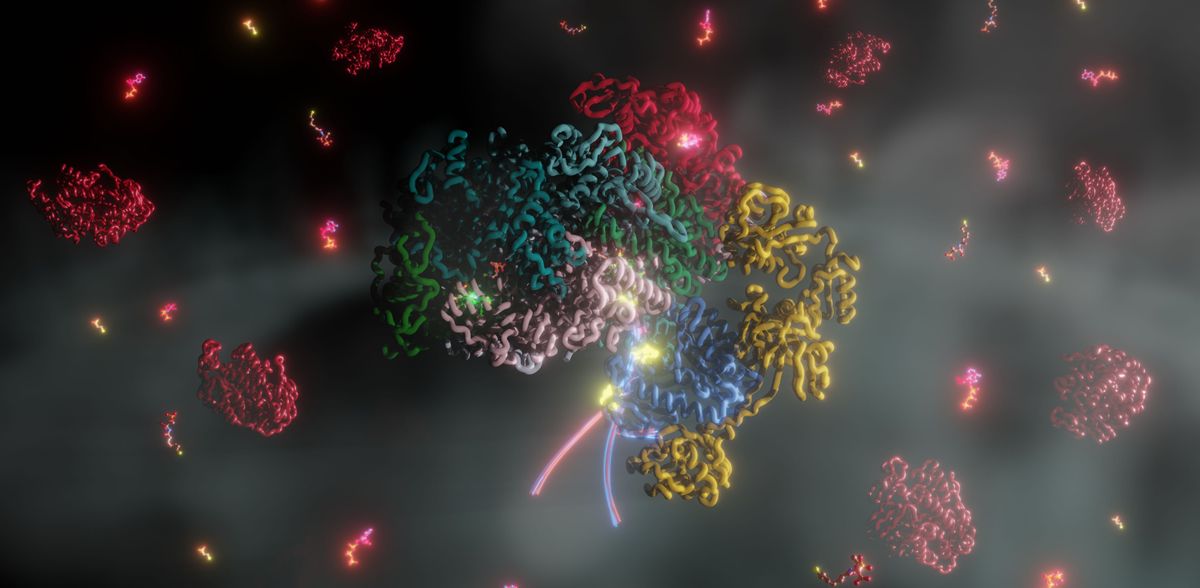
Im Zentrum der biologischen Methanproduktion steht MCR, ein hochspezialisiertes Enzym, dessen aktives Zentrum das einzigartige Coenzym F430 enthält. Die Funktion dieses Kofaktors hängt entscheidend von einem zentralen Nickelion ab, das sich im Oxidationszustand Ni(1+) befinden muss, um die Methanproduktion zu katalysieren. Die Aktivierung von Nickel in diesen Zustand erfordert jedoch das Überwinden einer beträchtlichen energetischen Hürde – eine der anspruchsvollsten Redoxreaktionen in der Natur. Wie frühe Lebensformen diese Aktivierung bewältigten, war lange Zeit ungeklärt.
In ihrer Studie gelang es dem Forschungsteam, den MCR-Aktivierungskomplex aus dem Modellorganismus Methanococcus maripaludis zu isolieren und zu charakterisieren. „Wir haben festgestellt, dass ein kleines Protein namens McrC zusammen mit weiteren methanogenen Markerproteinen das MCR in einem ATP-abhängigen Prozess aktiviert und so die notwendige Energie für die Methanproduktion aufbringt“, erklärt Fidel Ramírez-Amador von der Philipps-Universität Marburg, einer der Hauptautoren der Studie.
Spektroskopische Untersuchungen lieferten den fehlenden Beweis
Bemerkenswerterweise konnten die Forschenden zeigen, dass der Aktivierungsmechanismus drei einzigartig aufgebaute und hochspezialisierte Metallkomplexe benötigt, die bislang ausschließlich in der Nitrogenase, dem einzigen Enzym, das atmosphärischen Stickstoff in biologisch verfügbare Formen umwandeln kann, bekannt waren. „Die spektroskopischen Untersuchungen lieferten den fehlenden Beweis dafür, dass diese Kofaktoren aus Eisen und Schwefel bestehen und wahrscheinlich für den Elektronentransfer entscheidend sind“, erläutert Dr. Christian Lorent. Dr. Jan Schuller von der Philipps-Universität Marburg, Seniorautor der Studie, ergänzt: „Diese auffällige Ähnlichkeit legt nahe, dass diese Systeme trotz völlig unterschiedlicher Funktionen einen gemeinsamen evolutionären Ursprung haben. Unsere Studie etabliert eine beispiellose evolutionäre Verbindung zwischen zwei fundamentalen biologischen Prozessen: der Methanogenese und der Stickstofffixierung.“
„Die elegantesten Lösungen zur Energieerzeugung und die effizientesten Katalysatoren wurden in der Natur über Jahrmillionen evolutionär optimiert. Es ist unsere Aufgabe als Wissenschaftler diese zu finden, zu verstehen und anzuwenden“, resümiert Dr. Christian Lorent. Im Exzellenzcluster UniSysCat forscht er an der Aufklärung der Reaktionsmechanismen und Kopplung verschiedener Metalloenzyme, die zum Beispiel auch Wasserstoff produzieren oder das Klimagas Kohlenstoffdioxid binden können.
Originalveröffentlichung
Fidel Ramírez-Amador, Sophia Paul, Anuj Kumar, Christian Lorent, Sebastian Keller, Stefan Bohn, Thinh Nguyen, Stefano Lometto, Dennis Vlegels, Jörg Kahnt, Darja Deobald, Frank Abendroth, Olalla Vázquez, Georg Hochberg, Silvan Scheller, Sven T. Stripp, Jan Michael Schuller; "Structure of the ATP-driven methyl-coenzyme M reductase activation complex"; Nature, 2025-4-16