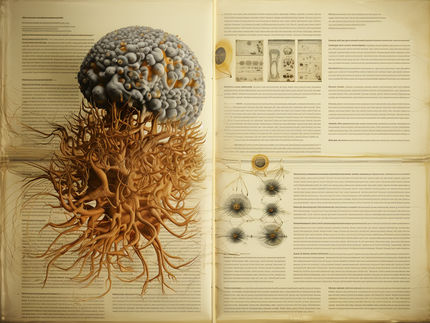
Forschende können Moleküle optisch vermessen
Mit der MINFLUX-Mikroskopie lassen sich Abstände innerhalb von Biomolekülen mit einem Lichtmikroskop bestimmen
Einem Team um die Physiker Steffen Sahl und Stefan Hell vom Göttinger Max-Planck-Institut für Multidisziplinäre Naturwissenschaften und vom Heidelberger Max-Planck-Institut für medizinische Forschung ist es gelungen, mit einem Lichtmikroskop Abstände innerhalb von Biomolekülen bis hinunter zu 1 Nanometer zu messen, und zwar mit Ångström-Präzision. Die mit der MINFLUX-Mikroskopie erreichte intra-molekulare Auflösung ermöglicht es, die räumlichen Abstände von Untereinheiten in Makromolekülen optisch zu erfassen und damit unterschiedliche Konformationen einzelner Proteine im Lichtmikroskop nachzuweisen.

Verschieden lange Polyproline, relativ steife Polypeptide, dienen als intramolekulare „Nanometer-Zollstöcke“ zur Demonstration höchster MINFLUX-Auflösungen im Förster Resonanzenergietransfer (FRET)-Abstandsbereich. Die 2-Sigma-Ellipsen zeigen die Messunsicherheit der einzelnen Positionen.
© MPI f. Multidisziplinäre Naturwissenschaften/ Steffen J. Sahl

Zwei identische Untereinheiten des bakteriellen Zitrat-Sensors in antiparalleler (oben) und paralleler (unten) Anordnung. Optische 3D-Positionsmessungen mit MINFLUX detektieren die beiden Zustände des von den Untereinheiten gebildeten Dimers, indem sie Abstände zwischen den Fluoreszenzmolekülen an den Protein-Enden sehr präzise vermessen. Die Ellipsen zeigen die Messunsicherheit der beiden Positionen (1, 2 und 3 sigma).
© MPI f. Multidisziplinäre Naturwissenschaften/ Steffen J. Sahl


Mit der Fluoreszenzmikroskopie können Forschende spezifische Moleküle in Zellen oder Geweben sichtbar machen. Die Technik ist aus der biologischen und medizinischen Forschung nicht mehr wegzudenken. Mithilfe neuer höchstauflösender Nanoskopie-Konzepte wie der MINFLUX-Mikroskopie lassen sich sogar eng benachbarte Biomoleküle lichtmikroskopisch voneinander trennen. Das Innere von Zellen genau abzubilden ist das eine, aber kann man optische Mikroskopie auch auf die Vermessung einzelner Proteine oder anderer Makromoleküle anwenden?
Wie die Forschenden um Steffen Sahl und Stefan Hell nun demonstrierten, geht das. Und zwar erstaunlich gut. In ihrer jüngsten Arbeit zeigte das Team, dass sich mit der MINFLUX-Methode auch der dreidimensionale Abstand zwischen zwei Fluoreszenzmarkern, die jeweils an einer spezifischen Stelle im Makromolekül angebracht sind, optisch vermessen lässt – und zwar mit Ångström-Präzision.
Abstände zwischen zwei räumlich verankerten Fluoreszenzmolekülen von ein paar Nanometern zu vermessen, war mit MINFLUX zwar denkbar, aber experimentell nicht so einfach umzusetzen oder nachzuweisen. „Bei Abständen kleiner als 5 bis 10 Nanometer wechselwirken die rund 1 Nanometer kleinen Fluoreszenzmoleküle häufig miteinander. Dadurch können sie ihr Fluoreszenzlicht nicht unabhängig voneinander aussenden – die Voraussetzung für eine zuverlässige Abstandsmessung“, erklärt Sahl, Erstautor der Studie. „Wie viele andere war auch ich fasziniert von der hohen Ortsauflösung und Präzision, die mit der von Stefan Hell vorgeschlagenen und entwickelten MINFLUX-Methode möglich ist“, sagt der Physiker. „Am Beginn unserer Arbeit stand daher eine Abschätzung: so klein sind Proteine, und so genau können wir prinzipiell werden. Warum realisieren wir nicht Auflösungen innerhalb eines Biomoleküls?“ Denn Nanometerabstände zwischen zwei Proteinen, oder deren Untereinheiten zu erfassen, war bislang der sogenannten Förster-Resonanzenergietransfer-Methode, kurz FRET, vorbehalten, einer Standardmethode in der Struktur- und Molekularbiologie.
Vorstoß in den FRET-Bereich
In diesen Auflösungsbereich sind Sahl, Hell und ihre Kolleg*innen nun auch mit der MINFLUX-Mikroskopie vorgestoßen. Zum Einsatz kamen eigens dafür am Max-Planck-Institut für Multidisziplinäre Naturwissenschaften entwickelte fotoaktivierbare Fluoreszenzmoleküle, die mit einer geringen Dosis UV-Licht nacheinander „angeschaltet“ werden können, aber nicht miteinander wechselwirken. So ließen sich die zu vermessenden Positionen im Makromolekül mit einem einzelnen Fluoreszenzmolekül markieren und unabhängig voneinander Ångström-genau erfassen.
„Wir haben gezeigt, dass mit MINFLUX alle Abstände – bis hin zum unmittelbaren Kontakt der Fluoreszenzmoleküle – gemessen werden können. Dafür reicht es, die direkte Position der Moleküle in zwei oder drei Dimensionen, also 2D oder 3D, zu bestimmen“, so Sahl. „Mit unseren Experimenten erreichen wir damit den Abstandsbereich von FRET und gehen sogar darüber hinaus.“
FRET dagegen schätzt den Abstand zwischen zwei Farbstoffmolekülen indirekt über den Energieübertrag von einem Farbstoff zum anderen ab. Dabei beeinflussen nicht nur der Abstand, sondern auch die Orientierung der Farbstoffmoleküle das Messergebnis. Dies kann zu Unsicherheiten führen, wenn es darum geht, den intra-molekularen Abstand präzise zu vermessen. Auch ist das FRET-Verfahren in Studien von Proteinuntereinheiten bislang häufig limitiert, wenn sich diese aus dem messbaren Abstandsbereich herausbewegen. „Hier kann die MINFLUX-Methode ihre Stärke ausspielen, indem sie alle denkbaren Abstände lückenlos bis hinunter zu 1 Nanometer korrekt darstellt“, erklärt Max-Planck-Direktor Hell. „MINFLUX ist somit ein neues, sehr leistungsfähiges Werkzeug im Repertoire der Strukturbiologie, um Proteine und andere Biomoleküle und ihre Interaktionen zu untersuchen.“
Von molekularen Zollstöcken und kleinen Proteinmolekülen
Für den Nachweis der präzisen Abstandsmessung und Ortsgenauigkeit nutzte das Forschungsteam ein Molekül, mit dem auch die FRET-Methode in einem klassischen Experiment in den 1960er-Jahren ihren Anfang nahm. Damals gelang es Lubert Stryer und Richard Haugland, die von Theodor Förster 1948 publizierte Abstandsabhängigkeit zu bestätigen. Dazu nahmen sie molekulare „Zollstöcke“ von definierter mittlerer Länge, sogenannte Polyproline, zu Hilfe. Genau diese Zollstöcke nutzten nun auch die Max-Planck-Forscher in ihren Experimenten – und zeigten, dass sich die Methode prinzipiell sogar in Zellen anwenden lässt.
So ließen sich in Kooperation mit der Forschungsgruppe von Stefan Jakobs am Max-Planck-Institut für Multidisziplinäre Naturwissenschaften in menschlichen Zellen fluoreszenzmarkierte Lamin-Proteine, die etwa 3 Nanometer dünne Filamente an der Membran um den Zellkern ausbilden, mit der MINFLUX-Methode getrennt abbilden.
Darüber hinaus demonstrierten die Forschenden das Potenzial von MINFLUX anhand von präzisen Abstandsmessungen in weiteren kleinen Proteinen, sogenannten Nanobodies, und aus ihnen gebildeten Oligomeren. Am Beispiel von Antikörpermolekülen zeigten sie, wie mehrere Positionsmessungen es erlauben, die räumliche Lage der Proteinuntereinheiten zueinander aufzulösen. Mit zwei identischen Untereinheiten des bakteriellen Zitratsensors demonstrierte das Team in Kooperation mit der Abteilung von Christian Griesinger am Max-Planck-Institut für Multidisziplinäre Naturwissenschaften, dass sogar Abstände von 1 Nanometer gemessen werden können. Die MINFLUX-Mikroskopie detektierte auch die beiden strukturellen Anordnungen der Untereinheiten eindeutig und mit einer Präzision im Bereich von 1 Ångström.
Hell, der im Jahr 2014 für die Entwicklung der superauflösenden Mikroskopie mit dem Chemie-Nobelpreis ausgezeichnet wurde, sagt: „Seitdem wir das MINFLUX-Konzept im Jahr 2016 erstmals vorgestellt haben, hat es die Grenzen der Lichtmikroskopie noch einmal radikal verschoben. Innerhalb von Makromolekülen auflösen zu können, war 2014 nicht absehbar.“