"Drastische und schnelle" Rückbildung von Hirntumoren nach CAR-T-Therapie der nächsten Generation
Forscher wählten einen neuen Ansatz für CAR-T, indem sie CAR-TEAM-Zellen zur Behandlung gemischter Zellpopulationen in Tumoren entwickelten
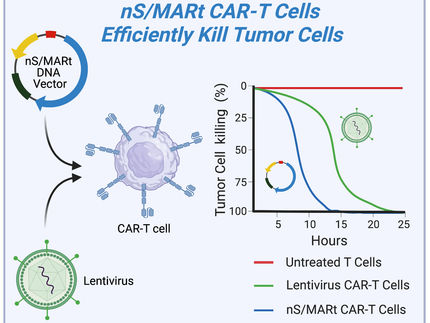
Ein gemeinsames Projekt, das Patienten mit einer tödlichen Form von Hirntumor eine vielversprechende Zelltherapie bieten soll, hat bei den ersten Patienten, die diese neuartige Behandlung erhalten haben, dramatische Ergebnisse gezeigt. In einer in der Fachzeitschrift The New England Journal of Medicine veröffentlichten Arbeit haben Forscher des Mass General Cancer Center, das zum Mass General Brigham Healthcare System gehört, die Ergebnisse der ersten drei Patientenfälle aus einer klinischen Phase-1-Studie vorgestellt, in der ein neuer Ansatz für die CAR-T-Therapie bei Glioblastom (GBM) untersucht wird. Die Studie mit der Bezeichnung INCIPIENT soll die Sicherheit von CARv3-TEAM-E T-Zellen bei Patienten mit rezidivierendem GBM untersuchen. Bereits wenige Tage nach einer einzigen Behandlung kam es bei den Patienten zu einer drastischen Verkleinerung ihrer Tumore, bei einem Patienten sogar zu einer fast vollständigen Rückbildung des Tumors. Mit der Zeit beobachteten die Forscher bei diesen Patienten ein Fortschreiten des Tumors, aber angesichts der vielversprechenden vorläufigen Ergebnisse der Strategie wird das Team Strategien verfolgen, um die Dauerhaftigkeit der Reaktion zu verlängern.

Mitglieder des INCIPIENT-Teams des Mass General Cancer Center (von links nach rechts): Elizabeth Gerstner, MD, William Curry, MD, Marcela Maus, MD, PhD, Bryan Choi, MD, PhD, Kathleen Gallagher, PhD und Matthew Frigault, MD.
Kate Flock/MGH
"Dies ist eine Geschichte von der Forschung zur Praxis, mit einer neuartigen Zelltherapie, die in den Labors des Massachusetts General Hospital entwickelt und innerhalb von fünf Jahren für den Einsatz bei Patienten umgesetzt wurde, um einen dringenden Bedarf zu decken", sagte Bryan Choi, MD, PhD, Neurochirurg und stellvertretender Direktor des Zentrums für Hirntumor-Immunologie und Immuntherapie, Zelluläre Immuntherapie-Programm, Mass General Cancer Center und Abteilung für Neurochirurgie. "Die CAR-T-Plattform hat die Art und Weise, wie wir über die Behandlung von Krebspatienten nachdenken, revolutioniert, aber solide Tumore wie das Glioblastom sind nach wie vor schwierig zu behandeln, da nicht alle Krebszellen genau gleich sind und die Zellen innerhalb des Tumors variieren. Unser Ansatz kombiniert zwei Therapieformen und ermöglicht es uns, das Glioblastom auf eine breitere und potenziell wirksamere Weise zu behandeln."
Der neue Ansatz ist das Ergebnis jahrelanger Zusammenarbeit und Innovation aus dem Labor von Dr. Marcela Maus, Direktorin des Zellularen Immuntherapieprogramms am Mass General Cancer Center, Paula O'Keeffe Lehrstuhl für Onkologie und Dozentin am Krantz Family Center for Cancer Research. Maus' Labor hat ein Team von kooperierenden Wissenschaftlern und Fachpersonal zusammengestellt, um genetisch veränderte T-Zellen der nächsten Generation rasch von der Forschung in die klinische Erprobung bei Krebspatienten zu bringen.
"Wir haben in den Aufbau des Teams investiert, um unsere Innovationen in der Immuntherapie aus dem Labor in die Klinik zu bringen und so die Versorgung von Krebspatienten zu verbessern", so Maus. "Diese Ergebnisse sind aufregend, aber sie sind auch erst der Anfang - sie zeigen uns, dass wir auf dem richtigen Weg sind, eine Therapie zu verfolgen, die das Potenzial hat, die Aussichten für diese hartnäckige Krankheit zu verändern. Wir haben die Patienten noch nicht geheilt, aber das ist unser kühnes Ziel".
Studien wie diese zeigen, wie vielversprechend die Zelltherapie für die Behandlung unheilbarer Krankheiten ist. Das Institut für Gen- und Zelltherapie am Mass General Brigham, wo Maus stellvertretender Leiter und Leiter der Abteilung für Zelltherapien ist, trägt dazu bei, wissenschaftliche Entdeckungen von Forschern in erste klinische Versuche am Menschen und schließlich in lebensverändernde Behandlungen für Patienten umzusetzen. Der multidisziplinäre Ansatz des Instituts hebt es von anderen in diesem Bereich ab und hilft den Forschern, neue Therapien schnell voranzutreiben und die technologischen und klinischen Grenzen dieses neuen Bereichs zu erweitern.
Bei der CAR-T-Therapie werden die eigenen Zellen des Patienten zur Krebsbekämpfung eingesetzt - sie gilt als die personalisierteste Art der Krebsbehandlung. Die Zellen eines Patienten werden entnommen, so modifiziert, dass sie Proteine auf ihrer Oberfläche produzieren, die als chimäre Antigenrezeptoren bezeichnet werden, und dann wieder in den Körper injiziert, um den Tumor direkt zu bekämpfen. Die in dieser Studie verwendeten Zellen wurden von der Connell and O'Reilly Families Cell Manipulation Core Facility des Dana-Farber/Harvard Cancer Center hergestellt.
CAR-T-Therapien sind für die Behandlung von Blutkrebs zugelassen, aber die Anwendung der Therapie bei soliden Tumoren ist begrenzt. Feste Tumore enthalten gemischte Zellpopulationen, die es einigen Krebszellen ermöglichen, sich auch nach einer Behandlung mit CAR-T der Erkennung durch das Immunsystem zu entziehen. Das Team von Maus arbeitet daran, diese Herausforderung der Tumorheterogenität mit einer innovativen Strategie zu bewältigen, die zwei bisher getrennte Strategien kombiniert: CAR-T und bispezifische Antikörper, so genannte T-cell engaging antibody molecules (TEAMs). Die Version von CAR-TEAM für das Glioblastom ist so konzipiert, dass sie direkt in das Gehirn eines Patienten injiziert werden kann.
Maus und Kollegen hatten zuvor CAR-T-Zellen entwickelt, die auf eine häufige Krebsmutation namens EGFRvIII abzielen. Als diese allein jedoch nur begrenzte Wirkung zeigte, entwickelte ihr Team diese CAR-T-Zellen so, dass sie TEAMs gegen Wildtyp-EGFR abgaben, der in normalem Hirngewebe nicht nachweisbar ist, aber in mehr als 80 Prozent der Fälle von GBM exprimiert wird.
Der Kombinationsansatz erwies sich in präklinischen Glioblastom-Modellen als vielversprechend, was das Forschungsteam ermutigte, die klinische Umsetzung zu verfolgen. In Zusammenarbeit mit den Neurochirurgen und Neuroonkologen des Mass General, darunter Dr. Elizabeth Gerstner und Dr. William Curry, sowie den Spezialisten für die Verabreichung von Zelltherapien, Dr. Matthew Frigault, und die Überwachung von Immuntherapien, Dr. Kathleen Gallagher, startete das Team INCIPIENT (ClinicalTrials.gov-Nummer NCT05660369), eine nicht-randomisierte, offene Phase-1-Studie an einem Standort.
Drei Patienten wurden zwischen März 2023 und Juli 2023 in die Studie aufgenommen. Die T-Zellen der Patienten wurden entnommen und in die neue Version der CAR-TEAM-Zellen umgewandelt, die dann jedem Patienten wieder infundiert wurden. Die Patienten wurden während der gesamten Studiendauer auf Toxizität überwacht.
Alle Patienten waren mit einer Standardbestrahlung und einer Temozolomid-Chemotherapie behandelt worden und wurden nach einem Wiederauftreten der Krankheit in die Studie aufgenommen:
- Bei einem 74-jährigen Mann bildete sich der Tumor nach einer einzigen Infusion der neuen CAR-TEAM-Zellen rasch, aber vorübergehend zurück. Blut und Liquor des Patienten zeigten einen Rückgang der EGFRvIII- und EGFR-Kopienzahlen, die schließlich nicht mehr nachweisbar waren.
- Ein 72-jähriger Mann wurde mit einer einzigen Infusion von CAR-TEAM-Zellen behandelt. Zwei Tage nach Erhalt der CAR-TEAM-Zellen zeigte eine MRT-Untersuchung einen Rückgang der Tumorgröße um 18,5 Prozent. Am 69. Tag war der Tumor um 60,7 Prozent geschrumpft, und das Ansprechen hielt über sechs Monate an.
- Eine 57-jährige Frau wurde mit CAR-TEAM-Zellen behandelt. Eine MRT-Untersuchung fünf Tage nach einer einzigen Infusion von CAR-TEAM-Zellen zeigte eine nahezu vollständige Rückbildung des Tumors.
Die Patienten haben die Infusionen gut vertragen, obwohl fast alle kurz nach der Infusion Fieber und einen veränderten Geisteszustand hatten, wie es bei einer aktiven CAR-T-Therapie, die in die Gehirnflüssigkeit verabreicht wird, zu erwarten war. Alle Patienten wurden vor ihrer Entlassung im Krankenhaus beobachtet.
Die Autoren stellen fest, dass trotz des bemerkenswerten Ansprechens bei den ersten drei Patienten in allen Fällen ein Fortschreiten des Tumors beobachtet wurde, obwohl in einem Fall über sechs Monate lang kein Fortschreiten zu verzeichnen war. Das Fortschreiten des Tumors hing zum Teil mit der begrenzten Persistenz der CAR-TEAM-Zellen in den Wochen nach der Infusion zusammen. Als nächsten Schritt erwägt das Team Serieninfusionen oder eine Vorkonditionierung mit Chemotherapie, um das Ansprechen zu verlängern.
"Wir berichten von einem dramatischen und schnellen Ansprechen bei diesen drei Patienten. Unsere bisherige Arbeit zeigt, dass wir Fortschritte machen, aber es gibt noch mehr zu tun", sagte Mitautorin Elizabeth Gerstner, MD, eine Neuroonkologin in der Abteilung für Neurologie am Massachusetts General Hospital.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.
Originalveröffentlichung
Bryan D. Choi, Elizabeth R. Gerstner, Matthew J. Frigault, Mark B. Leick, Christopher W. Mount, Leonora Balaj, Sarah Nikiforow, Bob S. Carter, William T. Curry, Kathleen Gallagher, Marcela V. Maus; "Intraventricular CARv3-TEAM-E T Cells in Recurrent Glioblastoma"; New England Journal of Medicine, 2024-3-13