Von Tausenden von Stunden hin zu wenigen Minuten: Software beschleunigt Entwicklung von Arzneistoffen
Forschende entwickeln neue Methode, um die Morphologie von Zuckerschichten auf klinisch relevanten Proteinen innerhalb von Minuten vorherzusagen
Zucker bedecken fast alle Proteine auf der Oberfläche unserer Körperzellen und bilden so einen Schutzschild um die Proteine. Somit beeinflussen diese Zucker, wie Zellen mit ihrer Umgebung, unter anderem mit Krankheitserregern, interagieren. Sie spielen daher eine wichtige Rolle bei der Entwicklung von Medikamenten. GlycoSHIELD, ein neuer computerbasierter Ansatz zur Untersuchung der Zuckerschilde von Proteinen, ist ressourcenschonend, zeiteffizient und benutzerfreundlich. Der Algorithmus wurde im Rahmen des Dioscuri-Programms der Max-Planck-Gesellschaft in einem polnisch-deutschen Kooperationsprojekt durch internationale Zusammenarbeit mit Forschungsteams in Frankreich, Taiwan und Deutschland entwickelt.
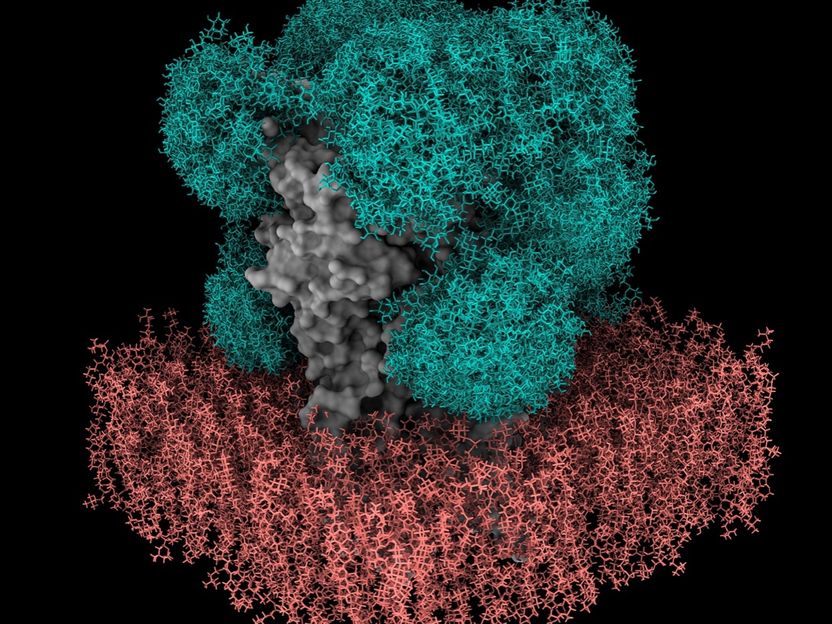
Modell des Zuckerschilds (grün) auf dem GABAA-Rezeptor (grau) in einer Membran (rot), erstellt von GlycoSHIELD.
© Dr. Cyril Hanus, Inserm, University Paris-Cité.
Die Proteine in unserem Körper übernehmen nicht nur wichtige Funktionen für das Überleben unserer Zellen, sondern beeinflussen auch die Entstehung und den Verlauf von Krankheiten. Um ihre Rolle im gesunden und erkrankten Organismus zu verstehen, untersuchen Forschende die atomare dreidimensionale Struktur von Proteinen sowohl mit experimentellen als auch mit computergestützten Methoden. Über 75% aller Proteine auf der Oberfläche unserer Zellen sind mit sogenannten Glykanen bedeckt. Diese Zuckermoleküle bilden sehr dynamische Schutzschilde um die Proteine. Weil die Zucker aber sehr mobil und variabel in ihrer Struktur sind, ist es schwierig zu bestimmen, wie die Schilde sich unter bestimmten Bedingungen verhalten oder wie sie die Wirkung von Arzneimittelmolekülen beeinflussen. Mateusz Sikora, Projektleiter und Leiter des Dioscuri Centre for Modelling of Posttranslational Modifications, und sein Team in Krakau sowie seine Partner am Max-Planck-Institut für Biophysik in Frankfurt am Main sind diese Herausforderung mit Hilfe von Computern angegangen. In ihrem Projekt haben sie mit Wissenschaftlern und Wissenschaftlerinnen des Inserm in Paris, der Academia Sinica in Tapei und der Universität Bremen zusammengearbeitet. Der von dem Team entwickelte neue leistungsstarke Algorithmus GlycoSHIELD ermöglicht eine schnelle, aber realistische Modellierung der Zuckerketten auf Proteinoberflächen. GlycoSHIELD reduziert die Rechenzeit und damit den Stromverbrauch im Vergleich zu herkömmlichen Simulationstools um mehrere Größenordnungen und ebnet so den Weg zum grüneren Rechnen. Die Forschenden haben ihre neue Methode und deren Validierung in der Fachzeitschrift Cell veröffentlicht.
Von Tausenden von Stunden hin zu wenigen Minuten
Die Zuckerschutzschilde beeinflussen stark, wie Proteine mit anderen Molekülen, zum Beispiel Medikamenten, wechselwirken. So versteckt die Zuckerschicht auf den Spike-Proteinen des Coronavirus beispielsweise das Virus vor dem Immunsystem, indem es natürlichen oder durch Impfstoffe gebildeten Antikörpern die Erkennung des Virus erschwert. Daher spielen Zuckerschilde eine wichtige Rolle bei der Entwicklung von Arznei- und Impfstoffen. Die pharmazeutische Forschung könnte stark von einer einfachen, routinemäßigen Vorhersage ihrer Morphologie und Dynamik profitieren. Bisher waren solche Vorhersagen über die Struktur der Zucker mithilfe von Computersimulationen jedoch nur mit Expertenwissen und auf speziellen Supercomputern möglich. In vielen Fällen waren dafür Tausende oder gar Millionen von Rechenstunden erforderlich. Mit GlycoSHIELD bietet Sikoras Team eine schnellere, umweltfreundliche Open-Source-Alternative. „Unser Ansatz reduziert Ressourcen, Rechenzeit und benötigtes technisches Know-how“, erklärt Sikora. „Jede*r kann jetzt die Anordnung und Dynamik von Zuckermolekülen auf Proteinen innerhalb von Minuten auf dem eigenen PC berechnen, auch ohne Expertenwissen und Hochleistungsrechner. Unsere neue Art der Berechnung ist außerdem sehr energieeffizient.“ Die Software kann nicht nur in der Forschung eingesetzt werden, sondern könnte auch bei der Entwicklung von Medikamenten oder Impfstoffen hilfreich sein, zum Beispiel bei der Immuntherapie gegen Krebs.
Ein Puzzle aus Zucker
Wie ist es dem Team gelungen, eine so hohe Effizienzsteigerung zu erzielen? Die Forschenden erstellten und analysierten eine Bibliothek mit Tausenden möglichen 3D-Anordnungen von solchen Zuckerketten, die am häufigsten im Menschen und in Mikroorganismen vorkommen. Mit langen Computersimulationen und Experimenten fanden sie Folgendes heraus: Es reicht aus zu beachten, dass die Zucker nicht mit Membranen oder Teilen des Proteins kollidieren, um die Schutzschilde zuverlässig vorherzusagen. Der Algorithmus basiert auf diesen Erkenntnissen. „GlyoSHIELD-Nutzer und ‑Nutzerinnen müssen nur das Protein und die Anknüpfpunkte der Zucker angeben. Unsere Software puzzelt die Zucker dann in der wahrscheinlichsten Anordnung auf die Proteinoberfläche“, erklärt Sikora. „Wir konnten die Zuckerschilde des Spike-Proteins exakt nachbilden: Sie sehen genauso aus, wie sie in Experimenten beobachtet werden!“ Mit GlycoSHIELD ist es nun möglich, sowohl neue als auch bereits bekannte Proteinstrukturen mit Informationen zu der Zuckerschicht zu ergänzen. Die Wissenschaftler und Wissenschaftlerinnen nutzten GlycoSHIELD beispielsweise auch, um das Muster der Zucker auf dem GABAA-Rezeptor zu entschlüsseln, einem wichtigen Angriffspunkt für Beruhigungs- und Narkosemittel.
Ein Erfolg für das Dioscuri Centre
Die von der Max-Planck-Gesellschaft initiierten Dioscuri Centres sollen helfen, exzellente Forschung in Mittel- und Osteuropa zu stärken und auszubauen. Seit Mai 2023 erhält Mateusz Sikora, ehemals Postdoktorand am Max-Planck-Institut für Biophysik, als Leiter des an der Jagiellonen-Universität in Krakau, Polen, eingerichteten Dioscuri Centres for Modelling of Posttranslational Modifications im Rahmen des bilateral geförderten Programms finanzielle Mittel. Gerhard Hummer, Leiter der Abteilung für Theoretische Biophysik am Max-Planck-Institut für Biophysik, unterstützt ihn als Partner aus Deutschland und hat ebenfalls zu dieser Arbeit beigetragen. Nach weniger als einem Jahr hat Sikora mit seinem grünen Algorithmus bereits einen großen Erfolg erzielt und trägt dazu bei, Polen als attraktiven und wettbewerbsfähigen Forschungsstandort zu repräsentieren.
Originalveröffentlichung
Yu-Xi Tsai, Ning-En Chang, Klaus Reuter, Hao-Ting Chang, Tzu-Jing Yang, Sören von Bülow, Vidhi Sehrawat, Noémie Zerrouki, Matthieu Tuffery, Michael Gecht, Isabell Louise Grothaus, Lucio Colombi Ciacchi, Yong-Sheng Wang, Min-Feng Hsu, Kay-Hooi Khoo, Gerhard Hummer, Shang-Te Danny Hsu, Cyril Hanus, Mateusz Sikora; "Rapid simulation of glycoprotein structures by grafting and steric exclusion of glycan conformer libraries"; Cell, Volume 187























































