Kidnapping im Immunsystem
Das humane Cytomegalievirus programmiert zelluläre Abwehrmechanismen um
Das humane Cytomegalievirus, kurz HCMV schlummert bei den meisten Menschen ein Leben lang unbemerkt im Körper. In immungeschwächten Individuen kann das Virus allerdings lebensgefährliche Infektionen verursachen. Es befällt dendritische Zellen, einen bestimmten Typ Zellen im Immunsystem. Die Mehrzahl von ihnen wird zwar infiziert, aber nur in wenigen wird das genetische Programm der Viren sofort ausgeführt. Forscherinnen und Forscher am TWINCORE, Zentrum für Experimentelle und Klinische Infektionsforschung, konnten jetzt zeigen, welche Signalwege des angeborenen Immunsystems das Virus angreift, um sich selbst von den Wirtszellen produzieren zu lassen. Diese Ergebnisse veröffentlichen sie in der Fachzeitschrift Nature Communications.

Dr. Bibiana Costa, Erstautorin der Studie, im Labor.
©TWINCORE/Grabowski
Bis zu 90% der Weltbevölkerung tragen HCMV in sich. Bei Menschen mit regulärem Immunsystem verläuft die Infektion in der Regel subklinisch, sie ruft also keine ausgeprägten Symptome hervor. In immunsupprimierten Patienten, beispielweise Empfängerinnen oder Empfänger von Organtransplantationen, kann die Infektion allerdings lebensbedrohlich werden. Außerdem ist die Infektion mit HCMV während der Schwangerschaft die häufigste Ursache für Fehlbildungen bei Neugeborenen, wie beispielsweise angeborene Hörschäden.
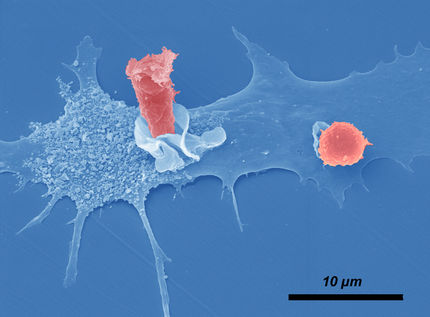
Im menschlichen Körper kann HCMV die myeloiden Zellen des Immunsystems befallen. Zu dieser Gruppe gehören auch die von Monozyten abgeleiteten dendritischen Zellen, zu deren Hauptaufgabe die Weiterverarbeitung von fremden Proteinen gehört, damit diese den T-Zellen präsentiert werden. Antigen-spezifische T-Zellen können dann infizierte Zellen beseitigen.
Die Forschenden aus dem Institut für Experimentelle Infektionsforschung unter der Leitung von Prof. Ulrich Kalinke konnte die von Monozyten abgeleiteten dendritischen Zellen in drei Gruppen unterteilen, von denen eine anfälliger für die Infektion ist als die übrigen. „Durch Einzelzell-RNA-Sequenzierungen haben wir festgestellt, dass in diesen Zellen der Signalweg, der normalerweise Viren erkennt, von HCMV quasi gekidnappt wird, um die produktive Infektion zu etablieren“, sagt Dr. Bibiana Costa, Postdoktorandin am TWINCORE und Erstautorin der Studie. „Es handelt sich um den sogenannten STING-Signalweg.“ STING steht für „stimulator of interferon genes“, zu Deutsch Stimulator von Inferferon-Genen.
Interferone sind Botenstoffe des Immunsystems, die sowohl direkt gegen Viren wirken als auch Abwehrzellen aktivieren können. Außerdem setzen Interferone wie in einer Kettenreaktion weitere Abwehrprozesse in Gang. In der Untergruppe der dendritischen Zellen, die für die Infektion besonders anfällig sind, blockieren viruseigene Proteine diese Schutzfunktion und programmieren sie stattdessen so um, dass ungestört neue Viruspartikel produziert werden.
„Diesen viralen Eingriff in das zelluläre Geschehen haben wir anschließend noch genauer untersucht, um herauszufinden, welche Gene in den Zellen genau betroffen sind“, sagt Costa. „Dabei konnten wir mehrere Kandidaten identifizieren, die entweder antivirale oder provirale Eigenschaften haben.“ Weil bestimmte immunmodulierende Medikamente genau in diese Signalwege eingreifen, bietet sich hier möglicherweise Potential für einen therapeutischen Ansatz. Dies scheint besonders vielversprechend, weil Trägerinnen und Träger von Organtransplantaten lebenslang immunsupprimierende Medikamente einnehmen müssen, um die Abstoßung des Transplantats durch das Immunsystem zu verhindern. „Dazu sind aber weitere Studien notwendig“, sagt Prof. Ulrich Kalinke, Direktor des Instituts für Experimentelle Infektionsforschung und Geschäftsführender Direktor des TWINCORE.
An der Studie waren neben den Forschenden vom TWINCORE Kooperationspartnerinnen und -partner aus mehreren Forschungseinrichtungen beteiligt, unter anderem vom Helmholtz-Institut für RNA-basierte Infektionsforschung HIRI in Würzburg, der Universität Regensburg, vom Helmholtz-Zentrum für Infektionsforschung in Braunschweig sowie der Medizinischen Hochschule Hannover. „Bei der Vernetzung unterstützt uns außerdem der Exzellenzcluster RESIST“, sagt Kalinke. „Ohne diese Partnerschaften könnten wir keine translationale Infektionsforschung auf hohem Niveau betreiben.“
Originalveröffentlichung
Bibiana Costa, Jennifer Becker, Tobias Krammer, Felix Mulenge, Verónica Durán, Andreas Pavlou, Olivia Luise Gern, Xiaojing Chu, Yang Li, Luka Čičin-Šain, Britta Eiz-Vesper, Martin Messerle, Lars Dölken, Antoine-Emmanuel Saliba, Florian Erhard, Ulrich Kalinke; "Human cytomegalovirus exploits STING signaling and counteracts IFN/ISG induction to facilitate infection of dendritic cells"; Nature Communications, Volume 15, 2024-2-26