Durchbruch in der hochauflösenden Fluoreszenzmikroskopie
Schnell auch im Nanometerbereich
Wissenschaftler*innen um Nobelpreisträger Stefan Hell am Max-Planck-Institut für medizinische Forschung in Heidelberg haben ein superauflösendes Mikroskop mit einer räumlich-zeitlichen Genauigkeit von einem Nanometer pro Millisekunde entwickelt. Es ist eine verbesserte Version der kürzlich von der Gruppe um Hell eingeführten MINFLUX-Mikroskopie. Das hochauflösende Mikroskop macht es möglich, winzige Bewegungen einzelner Proteine detaillierter zu beobachten als je zuvor. In dieser Studie untersuchten sie die Schrittbewegung des Motorproteins Kinesin-1, wie es entlang von Mikrotubuli durch die Zelle wandert. Die Ergebnisse unterstreichen das Potenzial von MINFLUX als revolutionäres neues Werkzeug zur Beobachtung von Konformationsänderungen in Proteinen im Nanometerbereich. Die Arbeit wurde kürzlich in Science veröffentlicht.
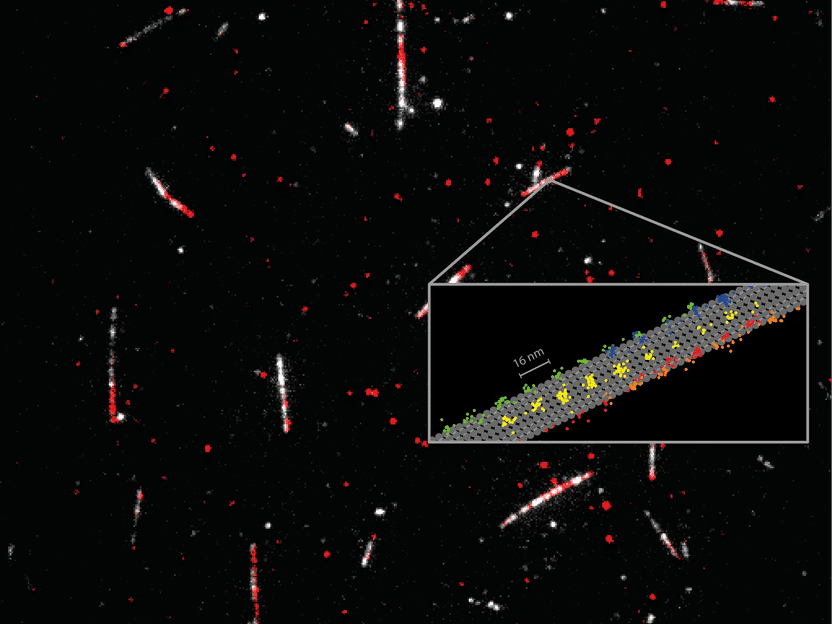
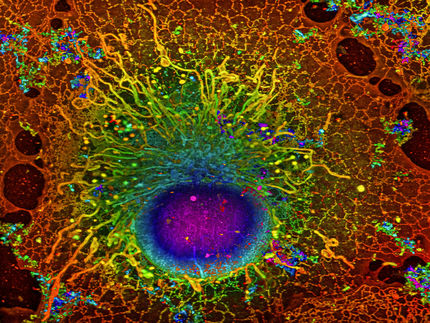
Messung des Motorprotein Kinesin-1 (rot), wie es auf den Mikrotubuli (weiß) entlang „läuft“. Die Beobachtung der 2D-Bewegungen einzelner Kinesin-1-Dimere (auf der Skizze in verschiedenen Farben) unter physiologischen ATP-Konzentrationen zeigt auf, wie sie entlang einzelner Bahnen voranschreiten. MINFLUX erfasst dabei bisher unerkannte Details der Bewegung des Motorproteins auf einzelnen Protofilamenten des Mikrotubulus (grau skizziert) und unterstreicht so das Potenzial von MINFLUX als revolutionäre Methode zur Beobachtung von Konformationsänderungen in Proteinen.
MPI for Medical Research
Um die Geschehnisse innerhalb einer Zelle zu entschlüsseln, müssen wir die Biochemie einzelner Proteine verstehen. Dabei ist die Messung kleinster Lage- und Formänderungen eine der größten Herausforderungen. Fluoreszenzmikroskopie, insbesondere superauflösende Mikroskopie (d.h. Nanoskopie), ist bei dieser Forschung unverzichtbar geworden. MINFLUX, eines der jüngsten Fluoreszenz-Nanoskopie-Verfahren, hat bereits eine räumliche Auflösung von einem bis zu wenigen Nanometern erreicht: die Größe kleiner organischer Moleküle. Aber um unser Verständnis der molekularen Zellphysiologie voranzutreiben, sind Beobachtungen mit noch höherer räumlich-zeitlicher Auflösung erforderlich.
Die Leistungsfähigkeit von MINFLUX maximieren
Als die Gruppe um Stefan Hell 2016 erstmals MINFLUX vorstellte, konnte man damit bereits fluoreszenzmarkierte Proteine in Zellen verfolgen. Die Bewegung der Proteine waren jedoch zufällig, und die Genauigkeit der Messungen lag in einer Größenordnung von zehn Nanometern. Die diese Woche in Science veröffentlichte Studie ist die erste, die das bisher unerreichte raumzeitliche Auflösungsvermögen von MINFLUX auf Konformationsänderungen von Proteinen, insbesondere des Motorproteins Kinesin-1, anwendet. Dazu entwickelten die Wissenschaftler*innen am Heidelberger MPI für medizinische Forschung eine neue MINFLUX-Version, um einzelne fluoreszierende Moleküle in Bewegung zu beobachten.
Bisher genutzte Methoden zur Messung von Proteindynamiken sind stark eingeschränkt in ihrer Fähigkeit, den entscheidenden (Sub-)Nanometer- / (Sub-)Millisekunden-Bereich zu erfassen. Einige bieten eine hohe räumliche Auflösung von bis zu wenigen Nanometern, können Änderungen jedoch nicht schnell genug verfolgen. Andere haben eine hohe zeitliche Auflösung, erfordern aber eine Markierung mit lichtstreuenden Kügelchen (Beads) aus Gold, Germanium oder Latex, die zwei bis drei Größenordnungen größer sind als das zu untersuchende Protein selbst. Dadurch wird die Funktion des Proteins unter Umständen so stark beeinflusst, dass man nicht sicher sein kann, die tatsächliche Proteinfunktion zu beobachten. Für MINFLUX hingegen muss dagegen nur ein herkömmliches Fluoreszenzmolekül mit einer Größe von ca. 1 Nanometer an das Protein gebunden werden. So kann MINFLUX die hohe Auflösung erreichen, während es die Proteinfunktion so gut wie nicht stört. Das ist für die Untersuchung der Bewegung nativer Proteine unabdingbar. „Ein vom Rauschen aus der Umgebung abgeschirmtes MINFLUX-Mikroskop, welches nah an der theoretischen Grenze arbeitet, ist die eine Herausforderung“, sagt Otto Wolff, Doktorand in der Gruppe. „Und die Experimente so durchzuführen, dass sie die Proteinfunktion nicht beeinflussen und dennoch den biologischen Mechanismus zeigen können, ist eine zweite“, ergänzt sein Kollege Lukas Scheiderer.
Das von der Gruppe nun vorgestelltes MINFLUX-Mikroskop kann Proteinbewegungen mit einer raum-zeitlichen Genauigkeit von bis zu 1,7 Nanometern pro Millisekunde aufzeichnen. Dafür braucht das Mikroskop nur etwa 20 vom fluoreszierenden Molekül emittierte Photonen zu detektieren.
„Ich bin sicher, wir sind dabei ein neues Kapitel aufzuschlagen, und zwar in der Erforschung der Bewegungen und Formveränderungen einzelner Proteinmoleküle“, sagt Stefan Hell. „Die Kombination aus hoher räumlicher und zeitlicher Auflösung, die MINFLUX bietet, wird es Wissenschaftlern ermöglichen, Biomoleküle so zu untersuchen, wie es zuvor nicht möglich war.“
Auflösung der Schrittbewegung von Kinesin-1 mit ATP unter physiologischen Bedingungen
Kinesin-1 spielt eine Schlüsselrolle beim Transport von Fracht durch unsere Zellen, und Mutationen des Proteins sind die Ursache mehrerer Krankheiten. Kinesin-1 „schreitet“ an Filamenten (den Mikrotubuli) entlang, die unsere Zellen wie ein Netz von Straßen durchspannen. Man kann sich die Bewegung buchstäblich als „Schritt“ vorstellen, da das Protein zwei „Füße“ hat, die in der Fachliteratur allerdings „Köpfe“ genannt werden, die abwechselnd ihre Position auf den Mikrotubuli wechseln. Diese Bewegung erfolgt normalerweise entlang eines der 13 Protofilamente, die die Mikrotubuli bilden. Das Voranschreiten dieser „Köpfe“ wird dabei durch die Spaltung des Hauptenergielieferanten der Zelle ATP (Adenosintriphosphat) angetrieben.
Die Wissenschaftler*innen markierten Kinesin-1 mit nur einem einzigen Fluoreszenzmolekül, und zeichneten so die regulären ca. 16 Nanometer weiten Schritte der einzelnen Köpfe auf, als auch Unterschritte dieses Schreitprozesses, die bisher nicht beobachtet werden konnten. Dabei lag die räumlich-zeitliche Auflösung im Bereich von Nanometern pro Millisekunde. Ihre Ergebnisse zeigen, dass ATP aufgenommen wird, während nur ein einzelner Kopf an die Mikrotubuli gebunden ist. Dagegen findet die ATP-Hydrolyse statt, während beide Köpfe gebunden sind. Es wurde beobachtet, dass sich der „Stiel“ des Proteins während eines Schrittes dreht. Dies ist der Teil des Kinesin-Moleküls, der die Fracht hält. Durch die hohe räumliche und zeitliche Auflösung von MINFLUX wurde auch eine Rotation des Kopfes in der Anfangsphase jedes Schrittes sichtbar. Die Messungen wurden mit physiologischen ATP-Konzentrationen gemacht, was bisher nicht möglich war.
Zukünftiges Potenzial in der Erforschung von Proteinbewegungen
„Ich bin gespannt, wohin uns MINFLUX noch führen wird. Es fügt der Erforschung der Funktionsweise von Proteinen eine weitere Dimension hinzu. Das kann uns helfen, die molekularen Mechanismen hinter vielen Krankheiten zu verstehen und letztendlich zur Entwicklung von Therapien beitragen“, fügt Jessica Matthias hinzu, eine ehemalige Postdoktorandin in Stefan Hell’s Gruppe, die nun in einer Ausgründung des Max Planck Instituts die Anwendung von MINFLUX auf eine Vielzahl biologischer Fragestellungen erforscht.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Proteinanalytik
Die Proteinanalytik ermöglicht einen tiefen Einblick in diese komplexen Makromoleküle, ihre Struktur, Funktion und Wechselwirkungen. Sie ist unerlässlich für die Entdeckung und Entwicklung von Biopharmazeutika, das Verständnis von Krankheitsmechanismen und die Identifizierung von therapeutischen Zielen. Durch Techniken wie Massenspektrometrie, Western Blot und Immunoassays können Forscher Proteine auf molekularer Ebene charakterisieren, ihre Konzentration bestimmen und mögliche Modifikationen identifizieren.

Themenwelt Proteinanalytik
Die Proteinanalytik ermöglicht einen tiefen Einblick in diese komplexen Makromoleküle, ihre Struktur, Funktion und Wechselwirkungen. Sie ist unerlässlich für die Entdeckung und Entwicklung von Biopharmazeutika, das Verständnis von Krankheitsmechanismen und die Identifizierung von therapeutischen Zielen. Durch Techniken wie Massenspektrometrie, Western Blot und Immunoassays können Forscher Proteine auf molekularer Ebene charakterisieren, ihre Konzentration bestimmen und mögliche Modifikationen identifizieren.