Zielsicherer Test für Antibiotika-Resistenzen in klinischen Enterobacter-Arten
Durchbruch im Kampf gegen Krankenhauskeime: Neue Entdeckung ermöglicht gezielte Antibiotika-Therapie
Bakterien der Gattung Enterobacter gehören weltweit zu den gefährlichsten Krankenhauskeimen. Einige ihrer Vertreter sind in hohem Maße resistent gegen die gebräuchlichen Antibiotika, sodass immer häufiger das Reserve-Antibiotikum Colistin als letzte Therapiemöglichkeit zum Einsatz kommt. Um nicht unnötig auf Colistin zurückzugreifen und damit zunehmende Resistenzen zu riskieren, wird vor einer Behandlung auf Resistenz oder Empfindlichkeit der Bakterien gegenüber Colistin getestet. Doch die gebräuchlichen Tests sind bei Enterobacter nicht verlässlich. In einer umfassenden Studie mit breiter Beteiligung des Deutschen Zentrums für Infektionsforschung (DZIF) haben Wissenschaftler:innen nun herausgefunden, woran das liegt. Auf dieser Grundlage konnten sie für die Gattung Enterobacter einen einfachen, empfindlichen und aussagekräftigen Test entwickeln, der nun eine gezielte Antibiotika-Therapie für die verschiedenen Enterobacter-Arten ermöglicht.
Symbolbild
Unsplash
Die derzeit verwendeten mikrobiologischen Tests auf Colistin-Resistenz und andere Antibiotika-Resistenzen ließen keine genauen Rückschlüsse hinsichtlich der Verbreitung von Resistenzen bei verschiedenen Enterobacter-Arten zu. Das lag zum einen daran, dass die taxonomische Einordnung der klinischen Enterobacter-Isolate ungenau war, zum anderen war die Fehlerquote bei der Bestimmung der Resistenzen hoch. Hier konnte die groß angelegte DZIF-Studie nun einen Durchbruch erzielen und sowohl die Verwandtschaftsbeziehungen der zahlreichen Enterobacter-Arten aufklären als auch die Resistenztestung optimieren. Dazu haben DZIF-Wissenschaftler:innen am Institut für Medizinische Mikrobiologie der Justus-Liebig-Universität Gießen (Deep-iAMR-Projekt) und am Forschungszentrum Borstel, Leibniz Lungenzentrum gemeinsam drei Jahre lang Enterobacter-Isolate analysiert, die an deutschen Universitätskliniken gesammelt wurden.
Bei den taxonomischen Studien erwies sich Enterobacter xiangfangensis als die am häufigsten vorkommende Art in deutschen Kliniken: Aus einem Pool von über 3246 Isolatdaten – weltweit gesammelt in mehr als zwanzig Jahren – machte diese Spezies im weltweiten Vergleich 68,7 Prozent aus.
Die Bestimmung der Antibiotika-Resistenzprofile mithilfe phänotypischer Assays, die vom Europäischen Komitee für antimikrobielle Empfindlichkeitstestung (EUCAST) empfohlen sind, ergab unklare Ergebnisse im Hinblick auf Colistin-Resistenz. „Es zeigte sich, dass viele Isolate in den Tests nicht oder kaum resistent waren, obwohl die Bakterien alle Gene enthielten, die für die Colistin-Resistenz benötigt werden“, erklärt der Erstautor der Studie, Dr. Swapnil Doijad, Friedrich-Schiller-Universität Jena. Ein Ergebnis, das Fragen aufwarf. Eine erste Antwort darauf erhielten die Forscher:innen, indem sie die Isolate, bei denen eine Resistenz nicht klar nachweisbar war, mit Hilfe der Massenspektrometrie weiter untersuchten.
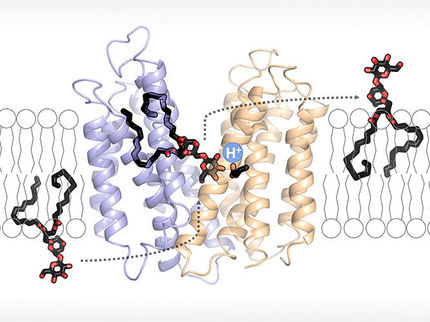
„Abhängig von der jeweiligen Enterobacter-Art entdeckten wir in Colistin-freiem Medium geringe Mengen von modifiziertem Lipid A,“ erklärt Dr. Nicolas Gisch vom Forschungszentrum Borstel, Co-Erstautor der Studie. Lipid A ist die Ankerstruktur von Lipopolyschariden (LPS), die einen entscheidenden Bestandteil der bakteriellen Membran darstellen und wesentlich für die Colistin-Resistenz sind. „Diese Modifikationen von Lipid A scheinen jeweils von der Bakterien-Art abhängig zu sein, ihre Expression unterliegt einem komplexeren Mechanismus und wird nicht alleinig durch Colistin ausgelöst.“ „Das Ergebnis deutet darauf hin, dass es eine Arten-abhängige Variation in der Heteroresistenz von Enterobacter gibt: In Routine-Testsystemen sind sie mal resistent, mal nicht“, so erklärt es PD Dr. Can Imirzalioglu, Co-Autor der Studie und Direktor für Klinische Mikrobiologie und Diagnostik am Institut für Medizinische Mikrobiologie der JLU Gießen.
Mit weiteren ausgeklügelten Methoden konnten die Autor:innen für die Gattung Enterobacter dieses Phänomen der Heteroresistenz aufklären. „Unsere Analysen ergaben, dass diese Bakterien auf der Oberfläche einen Sensor haben, der auf den pH-Wert, also den Säuregrad in der Umgebung reagiert und dementsprechend die Gene hoch- oder herunterreguliert, die für die Colistin-Resistenz zuständig sind“, erklärt Prof. Dr. Trinad Chakraborty, Senior-Autor und ehemaliger Direktor des Instituts für Medizinische Mikrobiologie an der JLU Gießen. Genetische Variationen und Wechselwirkungen mit dem pH-Wert der Umgebung führten in den herkömmlichen Testsystemen zu Spezies-abhängigen und unzuverlässigen Aussagen über das Ausmaß der Colistin-Resistenz verschiedener Enterobacter-Arten.
Basierend auf diesen Ergebnissen konnten die Forscher:innen ein einfaches, neues Testsystem entwickeln, das diese Ungenauigkeit der Heteroresistenz ausschaltet und die Colistin-Resistenz für jedes Isolat eindeutig misst. Damit schaffen sie die Voraussetzung für eine zielgenaue und sparsame Behandlung von Enterobacter-Arten mit dem Reserve-Antibiotikum. Ein Ergebnis, das nicht zuletzt durch die translationale Zusammenarbeit im Rahmen des DZIF zustande gekommen ist.
Originalveröffentlichung
Doijad SP, Gisch N, Frantz R, Kumbhar BV, Falgenhauer J, Imirzalioglu C, Falgenhauer L, Mischnik A, Rupp J, Behnke M, Buhl M, Eisenbeis S, Gastmeier P, Gölz H, Häcker GA, Käding N, Kern WV, Kola A, Kramme E, Peter S, Rohde AM, Seifert H, Tacconelli E, Vehreschild MJGT, Walker SV, Zweigner J, Schwudke D; DZIF R-Net Study Group; and Chakraborty T. Resolving colistin resistance and heteroresistance in Enterobacter species. Nat Commun. 2023 Jan 10;14(1):140.