Zombie-Viren auf Kaperfahrt
Uralte brachliegende Sequenzen im Genom greifen unerwartet in embryonale Entwicklung ein
Das Säugergenom enthält retrovirale Sequenzen in einem „untoten“, aber überwiegend harmlosen Zustand. Ein internationales Forschungsteam fand nun heraus, wie manche dieser viralen Genfragmente die embryonale Entwicklung beeinflussen, wenn sie reaktiviert werden. Unerwarteterweise sind es nicht virale Proteine, sondern Kopien des Erbguts, die dann eine Imbalance in der Zelle verursachen.

Symbolbild
Computer-generated image
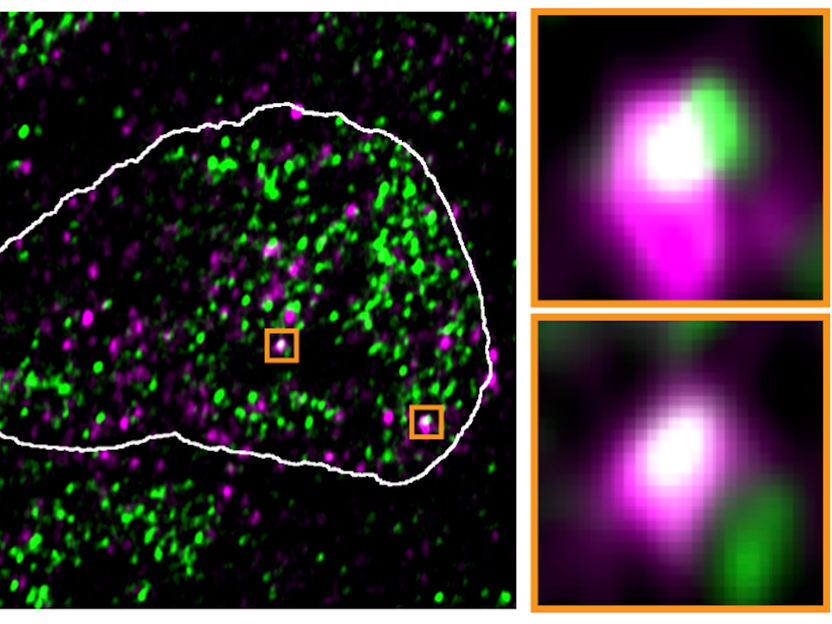
m Zellkern von Mäusestammzellen tauchen die RNA-Moleküle von reaktivierten endogenen Retroviren (violett) an denselben Stellen auf wie Kondensate mit RNA-Polymerase II (grün), wie diese fluoreszenzmikroskopische Aufnahme zeigt
Asimi et al., MPIMG

Über die Jahrmillionen der Evolution haben sich unzählige Viren in unserem Erbgut verankert. Ganze zehn Prozent der DNA von Säugetieren besteht aus uralten, retroviralen Sequenzen. Von ihnen geht keine Gefahr mehr aus, denn die meisten von ihnen sind bis zur Unkenntlichkeit mutiert. Außerdem wurden diese Gene durch die Zelle epigenetisch ruhiggestellt. Schlägt die Stummschaltung der Virus-Überreste jedoch fehl, können sie wieder zu neuem Leben erwachen, was für Chaos in der Zelle sorgt.
„Wir haben herausgefunden, dass die RNA, also die Botenkopie dieser viralen Gene, einen beträchtlichen Effekt auf die Vorgänge auf embryonale Zelle hat“, sagt Denes Hnisz, Leiter einer Forschungsgruppe am Max-Planck-Institut für molekulare Genetik (MPIMG) in Berlin. „Die viralen Sequenzen scheinen sich an ihre ursprüngliche Mission zu erinnern und kapern jene molekularen Maschinen, die den Informationsfluss von DNA zu RNA zu Proteinen sicherstellen. Interessant ist, dass die Boten-RNA dafür verantwortlich zu sein scheint.“
Zusammen mit seinem Team und weiteren Forscherinnen und Forschern beschreibt Hnisz in der Fachzeitschrift Nature Genetics, dass die RNA der auferweckten Viren jene Enzyme anzieht, die die Informationen vom Erbgut ablesen. Die Aufgaben der embryonalen Zelle – etwa wichtige embryonale Entwicklungsgene abzulesen – werden daraufhin vernachlässigt und es kommt zu einem gefährlichen Ungleichgewicht. Dieser entfesselte Zustand kommt beispielsweise in manchen Arten von Krebs und neurologischen Erkrankungen vor.
Eigentlich harmlose Virusreste
Viren sind clever aufgebaute Schnipsel aus genetischer Information. Einige pflanzen sich ins Genom ihrer Wirte und überdauern dort. Tausende Kopien sogenannter endogener Retroviren (ERV) haben sich im Erbgut der Säugetiere breitgemacht, häufig als hunderte Wiederholungen nebeneinander („repeats“).
„Wenn Retroviren während ihres Lebenszyklus von einem Abschnitt der DNA zum nächsten springen, können sie Gene verändern und sogar neu miteinander kombinieren. Damit sind sie ein wichtiges Werkzeug für die Evolution, um neue Gene zu erschaffen“, sagt Henri Niskanen, ein an der Studie beteiligter Wissenschaftler. „Für den Organismus verheißt eine unkontrollierte Genveränderung jedoch nichts Gutes, insbesondere während der Entwicklung des Embryos.“
Im intakten Zustand, identifiziert die Zelle daher die ERV-Sequenzen und legt diese Genabschnitte mit einer Reihe von spezialisierten Proteinen still. Außerdem wird das Chromosom an diesen Stellen enger gepackt.
Auferstandene Viren kapern Transkriptions-Maschinerie
Was passiert, wenn man diese Schutzmechanismen ausschaltet? Das Forschungsteam wollte herausfinden, was als erstes in der Zelle passiert, wenn die ERV-Zombies nicht länger in Schach gehalten werden. Dazu entfernten sie Trim28 aus embryonalen Stammzellen von Mäusen – ein Protein, das normalerweise die Virusreste stummschaltet. Dann beobachteten sie die unmittelbaren Konsequenzen.
Sobald Trim28 verschwunden war, wurden wie erwartet vermehrt ERV-Gene abgelesen, also RNA-Kopien mit Hilfe des Enzyms RNA-Polymerase produziert. Doch gleichzeitig verschwand die Polymerase von Stammzellgenen, also Genregionen, die besonders wichtige Entwicklungsgene steuern.
„Es gibt pro Zelle nur einen begrenzten Pool an Polymerase-Enzymen und anderen benötigten Faktoren“, sagt die Forscherin Christina Riemenschneider, die ebenfalls an der Studie mitgearbeitet hat. Sind zu viele Gene gleichzeitig aktiv, würden sie untereinander um die begrenzten Ressourcen konkurrieren. In einem Experiment ließen die Forschenden die ERV-Repeats und Stammzell-Gene gegeneinander antreten. „Wir sehen, dass die ERV-Repeats eine etwas höhere Affinität haben – sie ziehen die Maschinerie von embryonalen Genen ab und sorgen damit für ein Ungleichgewicht“, sagt Riemenschneider.
Anziehungskräfte zwischen Molekülen
Die RNA-Polymerase und ihre benötigten Faktoren tummeln sich in kleinen Tröpfchen, die viele Proteine enthalten und in der Zelle herumschwimmen wie Fettaugen in einer Suppe. In diesen „Kondensaten“ sind zahlreiche Moleküle für das Ablesen von Genen versammelt. Sie werden besonders stark von DNA-Abschnitten angezogen, die die wichtigsten Gene der Zelle enthalten.
Die ERV-Gene, oder vielmehr die RNA-Moleküle, die anhand dieser Gene produziert wurden, schienen die Kondensate regelrecht zu kapern. In hochauflösenden mikroskopischen Aufnahmen befanden sie sich häufig an den Orten, an denen sich auch die reaktivierten ERV-Gene befanden. Nachdem die Forschenden die Virus-RNA wieder aus den Zellen entfernten, wanderten die Tröpfchen zurück zu ihren angestammten Plätzen.
Die Effekte der virusartigen RNA waren nicht auf die molekulare Ebene beschränkt. In frühen Mäuse-Embryos wies das Forschungsteam nach, dass die Verlagerung der Kondensate hin zu den ERVs negative Auswirkungen auf die Entwicklung hatte. So verloren etwa Stammzellen ihre typische Eigenschaft, sich in jede andere Zelle weiterentwickeln zu können, weil entsprechende Gene nicht mehr aktiv waren.
Relevant für Evolution und die Entstehung von Krankheiten
„Es ist ziemlich bemerkenswert, dass nicht-kodierende, nicht-funktionale Gene so einen starken Effekt über die RNA ausüben“, sagt der Forscher Abhishek Sampath Kumar, der an der Publikation beteiligt war. „Bei Retroviren denkt man vielleicht an Schäden an der DNA oder Viruspartikel, aber das ist hier nicht der Fall.“
Das Team aus Wissenschaftlerinnen und Wissenschaftlern meint, dass ihre Ergebnisse die Forschung zu endogenen Retroviren in ein neues Licht rücken. „Das Kapern von transkriptionalen Kondensaten ist eine wichtige mechanistische Erkenntnis, die in zukünftigen Arbeiten zu Transposons und ihren epigenetischen Regulatoren beachtet werden sollte“, sagt der ebenfalls an der Studie beteiligte Wissenschaftler Vahid Asimi. „Es handelt sich um einen weitere Möglichkeit, wie ERVs zu Innovationen während der Evolution beigetragen haben.“
„Die Reaktivierung von ERVs steht ganz klar im Zusammenhang mit Krankheiten, von Fettleibigkeit über verschiedene Krebsarten bis hin zu neurologischen Erkrankungen wie amyotropher Lateralsklerose und Schizophrenie,“ ergänzt Gruppenleiter Denes Hnisz. „Unsere Forschung hilft hoffentlich dabei, die molekularen Ursachen dieser Erkrankungen zu ergründen.“
Originalveröffentlichung
Asimi V, Sampath Kumar A, Niskanen H, Riemenschneider C, Hetzel S, Naderi J, Fasching N, Popitsch N, Du M, Kretzmer H, Smith ZD, Weigert R, Walther M, Mamde S, Meierhofer D, Wittler L, Buschow R, Timmermann B, Cisse II, Ameres SL, Meissner A, Hnisz D. Hijacking of transcriptional condensates by endogenous retroviruses. Nat Genet. 2022 Aug;54(8):1238-1247.