Ein neuer Nanopartikel, der im Herzen der Zellen wirkt
Ein Team von UNIGE und LMU entwickelte ein Transport-Nanopartikel, um ein entzündungshemmendes Medikament viel wirksamer und weniger giftig zu machen
Wie kann ein Medikament genau dorthin gebracht werden, wo es benötigt wird, und gleichzeitig das Risiko von Nebenwirkungen begrenzen? Die Verwendung von Nanopartikeln zur Verkapselung eines Arzneimittels, um es und den Körper zu schützen, bis es seinen Wirkort erreicht, wird zunehmend untersucht. Dazu muss jedoch für jedes Medikament das richtige Nanopartikel anhand einer Reihe präziser Parameter ermittelt werden. Einem Team der Universität Genf (UNIGE) und der Ludwig-Maximilians-Universität München (LMU) ist es gelungen, ein vollständig biologisch abbaubares Nanopartikel zu entwickeln, das in der Lage ist, ein neues entzündungshemmendes Medikament direkt in die Makrophagen - die Zellen, in denen unkontrollierte Entzündungsreaktionen ausgelöst werden - einzubringen und damit seine Wirksamkeit zu gewährleisten. Darüber hinaus verwendeten die Wissenschaftler eine In-vitro-Screening-Methode, so dass keine Tierversuche erforderlich waren. Diese Ergebnisse, die kürzlich im Journal of Controlled Release veröffentlicht wurden, ebnen den Weg für eine äußerst wirksame und gezielte entzündungshemmende Behandlung.

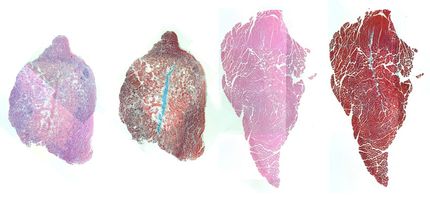
Diese elektronenmikroskopische Aufnahme zeigt die poröse Beschaffenheit der Silika-Nanopartikel. Diese Poren sind groß genug, um den Eintritt einer großen Anzahl von NSA-Molekülen zu ermöglichen. Hier sind sie geschützt, bis sie von den Immunzellen aufgenommen werden. An diesem Punkt wird NSA freigesetzt und kann die Entzündungsprozesse stoppen.
UNIGE - Carole Bourquin
Entzündungen sind eine wichtige physiologische Reaktion des Körpers, um sich gegen Krankheitserreger wie Bakterien zu verteidigen. Sie kann jedoch problematisch werden, wenn sie zu einem chronischen Zustand wird, wie z. B. bei Krebserkrankungen, Autoimmunkrankheiten oder bestimmten Virusinfektionen. Es gibt bereits zahlreiche Behandlungen, doch ihre Wirkung ist oft nicht sehr gezielt, es sind hohe Dosen erforderlich und es treten häufig schädliche Nebenwirkungen auf. Makrophagen, große Immunzellen, deren natürliche Funktion darin besteht, Krankheitserreger aufzunehmen und Entzündungen auszulösen, um sie zu zerstören, sind häufig an entzündlichen Erkrankungen beteiligt. Wenn sie übermäßig aktiviert werden, lösen sie eine übermäßige Entzündungsreaktion aus, die sich gegen den Körper wendet, anstatt ihn zu schützen.
Necrosulfonamid (NSA) ist ein neues Molekül, das die Freisetzung mehrerer wichtiger entzündungsfördernder Mediatoren hemmt und somit einen vielversprechenden Fortschritt bei der Verringerung bestimmter Arten von Entzündungen darstellt. Da es jedoch von Natur aus extrem hydrophob ist, kann es sich im Blutkreislauf nur schlecht fortbewegen und viele Zelltypen angreifen, was potenziell toxische Wirkungen auslösen könnte.
Aus diesem Grund ist dieses Molekül noch nicht als Medikament erhältlich", erklärt Gaby Palmer, Professorin am Fachbereich Medizin und am Genfer Zentrum für Entzündungsforschung an der medizinischen Fakultät der UNIGE, die die Studie mit geleitet hat. Die Verwendung eines Nanopartikels als Transportgefäß würde diese Unzulänglichkeiten umgehen, indem das Medikament direkt in die Makrophagen gebracht wird, um die entzündliche Überaktivierung dort zu bekämpfen, wo sie beginnt."
Drei Nanopartikel unter dem Mikroskop
Die Wissenschaftler testeten verschiedene poröse Nanopartikel, wobei die Hauptkriterien eine Verringerung der Toxizität und der erforderlichen Dosierung sowie die Fähigkeit waren, das Medikament erst dann freizusetzen, wenn der Nanopartikel das Innere der Makrophagen erreicht hat. Wir haben eine In-vitro-Screening-Technologie verwendet, die wir vor einigen Jahren an menschlichen und Mäusezellen entwickelt haben. Das spart Zeit und macht den Einsatz von Tiermodellen überflüssig'', erklärt Carole Bourquin, Professorin an den Fakultäten für Naturwissenschaften (Institut für Pharmazeutische Wissenschaften der Westschweiz) und Medizin der UNIGE (Abteilung für Anästhesiologie, Pharmakologie, Intensivmedizin und Notfälle, Translationales Forschungszentrum für Onkohämatologie, Genfer Zentrum für Entzündungsforschung), die diese Arbeit an der UNIGE mit geleitet hat. Nur die vielversprechendsten Partikel werden dann an Mäusen getestet, was eine Voraussetzung für klinische Versuche am Menschen ist.
Untersucht wurden drei sehr unterschiedliche Nanopartikel mit hoher Porosität: ein Nanopartikel auf Cyclodextrin-Basis, ein Stoff, der häufig in Kosmetika oder industriellen Lebensmitteln verwendet wird, ein poröses Magnesiumphosphat-Nanopartikel und schließlich ein poröses Siliziumdioxid-Nanopartikel. Das erste war in Bezug auf das Aufnahmeverhalten der Zellen weniger zufriedenstellend, während sich das zweite als kontraproduktiv erwies: Es löste die Freisetzung von entzündungsfördernden Mediatoren aus und stimulierte die Entzündungsreaktion, anstatt sie zu bekämpfen", sagt Bart Boersma, Doktorand im Labor von Carole Bourquin und Erstautor dieser Studie.
Der poröse Siliziumdioxid-Nanopartikel hingegen erfüllte alle Kriterien: Er war vollständig biologisch abbaubar, hatte die richtige Größe, um von Makrophagen geschluckt zu werden, und konnte das Medikament in seinen zahlreichen Poren aufnehmen, ohne es zu früh freizusetzen. Die entzündungshemmende Wirkung war bemerkenswert". Das Team wiederholte dann seine Tests, indem es die Nanopartikel mit einer zusätzlichen Lipidschicht überzog, was jedoch keinen größeren Nutzen brachte als die Nanopartikel aus Kieselerde allein.
Winzige Kieselerdeschwämme
Andere von dem deutsch-schweizerischen Team entwickelte Siliziumdioxid-Nanoschwämme hatten bereits ihre Wirksamkeit beim Transport von Antitumor-Medikamenten bewiesen. Hier tragen sie ein ganz anderes Medikament, das das Immunsystem hemmt", sagt Carole Bourquin. ''Mesoporöses Siliziumdioxid erweist sich zunehmend als Nanopartikel der Wahl im pharmazeutischen Bereich, da es sehr wirksam, stabil und ungiftig ist. Allerdings erfordert jedes Medikament einen maßgeschneiderten Träger: Form, Größe, Zusammensetzung und Bestimmung der Partikel müssen jedes Mal neu bestimmt werden." Die Kombination dieses starken entzündungshemmenden Medikaments mit diesen Nanopartikeln aus mesoporösem Siliziumdioxid zeigt einen vielversprechenden Synergismus, den das Team weiter untersuchen wird.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.