Wenn die Tarnkappe fällt – zweistufiger Mechanismus entdeckt, mit dem das angeborene Immunsystem auch Viren wie HIV früh erkennen kann
Das Verständnis dieses Mechanismus könnte für die Entwicklung von AIDS-Impfstoffen hilfreich sein
Forschende des Paul-Ehrlich-Instituts haben in einem internationalen Forschungsverbund einen zweistufigen Mechanismus des angeborenen Immunsystems entdeckt, der es ermöglicht, auch das HI-Virus (Humanes Immundefizienz-Virus, HIV) spezifisch zu erkennen und eine frühe Immunantwort auszulösen. Dieses Wissen könnte bei der Entwicklung von Impfstoffen genutzt werden, die diesen Mechanismus verstärken und damit eine wirksame und frühe körpereigene Abwehr gegen HIV erzeugen könnten.
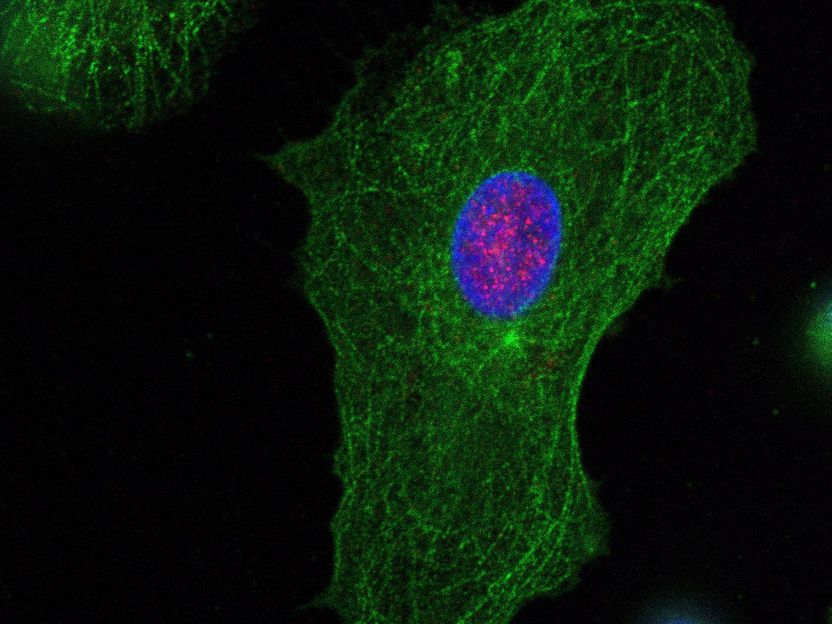
Monozyten-abgeleitete dendritische Zellen (MDDCs) eines gesunden Spenders, gefärbt für PQBP1 (rot) und die zelluläre Strukturkomponente Tubulin-beta (grün). Das Kernkompartiment ist blau gefärbt.
N. Hein-Fuchs / Paul-Ehrlich-Institut
Das Humane Immundefizienz-Virus HIV-1 gehört zur Familie der sogenannten Lentiviren, die die Medizin vor besondere Herausforderungen stellt. HI-Viren verursachen mit AIDS eine langsam fortschreitende, chronische Infektionskrankheit, da sie die Abwehrmechanismen des Immunsystems umgehen können.
Doch scheint das Immunsystem durchaus grundsätzlich die Fähigkeit zu besitzen, auch HIV früh zu erkennen. Forschende des Paul-Ehrlich-Instituts haben in einem internationalen Forschungsverbund, der von Dr. Chanda und Dr. Yoh, Sanford Burnham Prebys Medical Discovery Institute in La Jolla, Kalifornien, koordiniert wurde, zusammen mit Kolleginnen und Kollegen aus New York, Chicago, Sidney und New Haven hierzu neue Erkenntnisse gewonnen. Sie konnten den Mechanismus aufklären, wie die genetische Information, die DNA des HI-Virus in der Zelle als fremd erkannt und dadurch eine Abwehr ausgelöst werden kann. Das HI-Virus ist ein RNA-Virus. Nach dem Eindringen in eine Zelle wird beim HI-Virus nur eine einzige DNA-Kopie ausgehend vom RNA-Genom synthetisiert und anschließend in das Genom des Wirts integriert. So wird es von der Zelle wie ein normales Zellgen behandelt und bleibt damit dem Wirtsabwehrsystem gegenüber unsichtbar.
Wie kann nun die zelluläre Überwachungsmaschinerie diese geringe DNA-Menge, die auch nur vorübergehend vorkommt, erkennen? Die Wissenschaftlerinnen und Wissenschaftler identifizierten einen bisher nicht bekannten Zwei-Schritt-Mechanismus, der genau dies ermöglicht. Ein – bereits in 2015 identifizierter – Rezeptor, das Protein Polyglutamin-Bindungsprotein 1 (PQBP1), markiert in einem ersten Schritt das intakte virale Kapsid. Das Kapsid ist die Proteinstruktur, die der Verpackung des Virusgenoms dient. Das bereits bekannte DNA-Sensor-Protein, die sogenannte zyklische GMP-AMP-Synthase (cGAS), wird im zweiten Schritt benötigt, wenn das HI-Virus seine RNA bei dem Vorgang der Reversen Transkription in DNA umbaut und das virale Kapsid zu zerfallen beginnt.
Dieses zweistufige Erkennen sowohl von Erregerprotein (HIV- Kapsid) als auch von Erreger-DNA (HIV-DNA) stellt sicher, dass die darauffolgende Aktivierung immunstimulierender Signalwege (über Interferon, IFN) nicht spontan durch nur eine Komponente aktiviert wird. So wird sichergestellt, dass nicht versehentlich körpereigene Strukturen angegriffen werden. Kommt es nach dieser doppelten Erkennung zur Aktivierung, wird eine starke und zielgerichtete Entzündungsreaktion vermittelt. Dies löst eine robuste Reaktion auf „echte“ fremde DNA-Spezies aus und umgeht gleichzeitig eine nicht gewollte Selbstaktivierung von Wirts-DNA.
Neues Wissen über die angeborene zelluläre Erkennung von Lentiviren hinaus
Die kooperative Studie bietet nicht nur neue Einblicke in die angeborene zelluläre Erkennung von Viren aus der Familie der Lentiviren, sondern veranschaulicht, wie Sensoren in den Zellen über zusätzliche Faktoren und Kontrollmechanismen auf spezifische und möglicherweise seltene oder kurzzeitig verfügbare, in Mikroben vorkommende Muster (pathogen-associated molecular patterns, PAMPs) gelenkt werden können. Mit diesem generellen Konzept könnten möglicherweise auch andere Pathogene sehr spezifisch und effizient erkannt werden.
Originalveröffentlichung
Yoh SM, Mamede JI, Lau D, Ahn N, Sánchez-Aparicio MT, Temple J, Tuckwell A, Fuchs NV, Cianci GC, Riva L, Curry H, Yin X, Gambut S, Simons LM, Hultquist JF, König R, Xiong Y, García-Sastre A, Böcking T, Hope TJ, Chanda SK (2022): Recognition of HIV-1 capsid by PQBP1 licenses an innate immune sensing of nascent HIV-1 DNA. Mol Cell Jul 8 [Epub ahead of print].