Umprogrammierte Makrophagen fördern Ausbreitung von Brustkrebs
Fehlen Makrophagen, weil sie z.B. mit einem Wirkstoff außer Gefecht gesetzt wurden, kommt es nicht zur Produktion eines krebsfördernden Proteincocktails
Metastasierende Brustkrebszellen zweckentfremden Makrophagen, einen Typ von Immunzellen, um die Ansiedlung von Krebsmetastasen in der Lunge zu fördern. Die umprogrammierten Fresszellen regen dann Blutgefäßzellen dazu an, einen Cocktail an metastasierungsfördernden Proteinen auszuschütten, die Bestandteil der so genannten metastatischen Nische sind. Dies zeigten Wissenschaftlerinnen und Wissenschaftler vom Deutschen Krebsforschungszentrum (DKFZ) und vom Stammzell-Institut HI-STEM an Mäusen, denen menschliche Brustkrebszellen übertragen worden waren. Mit der Arbeit konnte das Forscherteam neue Angriffspunkte identifizieren und erste Konzepte entwickeln, um die metastatische Ausbreitung von Brustkrebs besser zu verhindern.
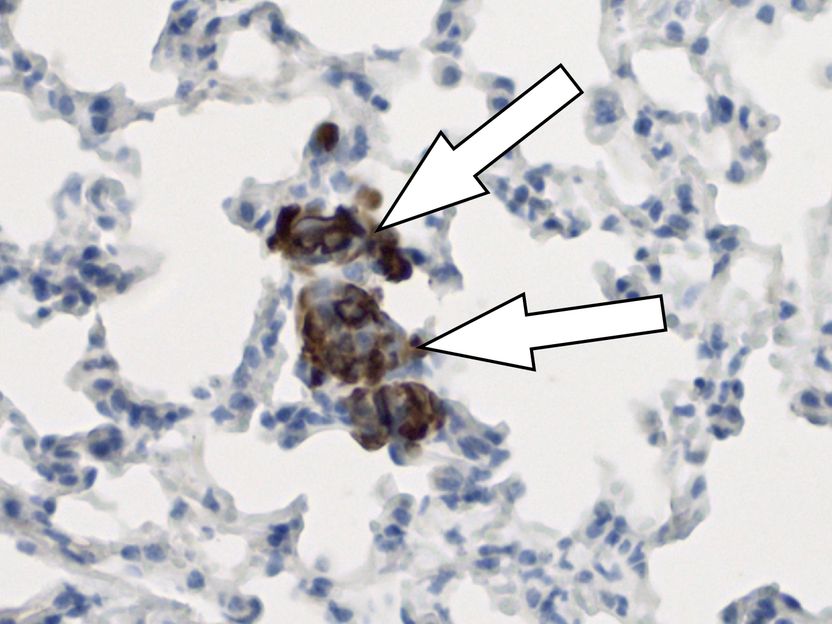
Brustkrebszellen (braun dargestellt) sind in die Lunge eingewandert und zu einer frühen Metastase ausgewachsen
© Oskarsson /HI-STEM und DKFZ
Krebs breitet sich im Körper aus, indem sich einzelne Zellen vom Primärtumor ablösen und über die Blut- oder Lymphbahnen in entfernt liegende Regionen des Körpers vordringen. Bevor sie dort zu einer Metastase auswachsen können, müssen sie sich über vielfältige molekulare Wechselwirkungen mit ihrer neuen Umgebung verständigen. „Um sich in diesem neuen Umfeld ansiedeln zu können, bereiten die Krebszellen zunächst ihre Mikroumgebung vor", sagt Thordur Oskarsson vom Deutschen Krebsforschungszentrum (DKFZ) und vom Stammzell-Institut HI-STEM. Forscher sprechen davon, dass sich die Tumorzellen eine „metastatische Nische" schaffen.
Blutgefäße spielen eine ganz besondere Rolle bei der Metastasierung. Abgelöste Tumorzellen halten sich bevorzugt in ihrer unmittelbaren Nähe auf. Insbesondere die Wechselwirkungen der Krebszellen mit den Endothelzellen, die das Innere der Adern auskleiden, sind entscheidend für die Metastasierung, wie bereits viele Studien gezeigt haben. Allerdings sind die Details dieses molekularen Austauschs noch weitestgehend unbekannt.
Das Team um Oskarsson hat diese Interaktionen nun an Mäusen während der metastatischen Besiedelung der Lunge durch Brustkrebszellen untersucht. Die Forscher beobachteten zunächst, dass vier Gene in den Lungenendothelzellen drei Wochen nach Beginn der Metastasierung eine besonders starke Aktivitätssteigerung aufwiesen. Sie kodieren für vier Proteine, die in die Mikroumgebung ausgeschüttet werden (Inhbb, Lama1, Scgb3a1 und Opg). Sie fördern sowohl einzeln als auch in Kombination die Entstehung von Lungenmetastasen. Inhbb und Scgb3a1 verleihen den Krebszellen Stammzelleigenschaften, Opg verhindert den programmierten Zelltod Apoptose und Lama1 unterstützt das Überleben der Zellen. Tatsächlich korreliert eine hohe Expression dieser vier neu identifizierten Nischenfaktoren sowohl mit einem verkürzten rückfallfreien Überleben als auch mit einem verkürzten Gesamtüberleben von Brustkrebspatientinnen.
Doch auf welche Weise bringen die Krebszellen das Lungenendothel dazu, den metastasierungsfördernden Proteincocktail zu produzieren? Zur Überraschung der Wissenschaftler erledigen die Krebszellen diesen Job nicht selbst, sondern spannen einen Zelltyp des angeborenen Immunsystems dafür ein, die Makrophagen.
„Diese Fresszellen, die sich häufig in der Nachbarschaft der Lungen-Blutgefäße aufhalten, werden ihrerseits aktiviert durch das von den Brustkrebszellen produzierte Tenascin, ein Protein, das die extrazelluläre Matrix bildet", erklärt Tsunaki Hongu, Erstautor der Studie. Tenascin ist bei vielen Krebsarten am Fortschreiten der Erkrankung beteiligt. Nach der Aktivierung durch Tenascin produzieren die Makrophagen verschiedene Faktoren, die in den Endothelzellen die Produktion des krebsfördernden Proteincocktails induzieren. Fehlen Makrophagen – etwa, weil sie mit einem speziellen Wirkstoff außer Gefecht gesetzt wurden, so kommt es nicht zur Produktion des metastasierungsfördernden Proteincocktails.
„Die Komplexität der Interaktionen zwischen Krebszellen, Makrophagen und Endothelzellen ist erstaunlich. Mit dem besseren Verständnis der zahlreichen Proteine und Faktoren, die an der Metastasierung beteiligt sind, konnten wir eine Vielzahl Ansatzpunkte für neue Strategien identifizieren, wie die Ausbreitung von Brustkrebs aufgehalten werden kann", fasst Oskarsson zusammen, der inzwischen am H. Lee Moffitt Cancer Center and Research Institute in Tampa, Florida, forscht. „Aus diesen neuen Erkenntnissen konnten wir bereits erste potentielle Therapiekonzepte entwickeln, die nun in weiteren Studien validiert werden müssen", ergänzt der HI-STEM Direktor Andreas Trumpp.
Originalveröffentlichung
Tsunaki Hongu, Maren Pein, Jacob Insua-Rodriguez, Ewgenija Gutjahr, Greta Mattavelli, Jasmin Meier, Kristin Decker, Arnaud Descot, Matthias Bozza, Richard Harbottle, Andreas Trumpp, Hans-Peter Sinn, Angela Riedel and Thordur Oskarsson: Perivascular tenascin C triggers sequential activation of macrophages and endothelial cells to generate a pro-metastatic vascular niche in the lungs; Nature Cancer 2022



















































