Studie zeigt, wie Wirkstoff wichtigen Rezeptor hemmt
Ergebnisse der Universität Bonn wecken Hoffnung auf neue Medikamente gegen Krebs und Hirnerkrankungen
Der A2A-Rezeptor reguliert, mit welcher Vehemenz das angeborene Immunsystem gegen kranke Zellen vorgeht. Forschende der Universität Bonn haben nun erstmals zeigen können, wie ein wichtiger Hemmstoff an den Rezeptor bindet. Die Ergebnisse erleichtern es künftig, gezielt nach Molekülen zu suchen, die das angeborene Immunsystem schlagkräftiger machen. Diese könnten zum Beispiel im Kampf gegen Krebs, aber auch gegen Hirnerkrankungen wie Alzheimer oder Parkinson zum Einsatz kommen. Die finale Version der Studie ist in der Zeitschrift Angewandte Chemie International Edition erschienen.
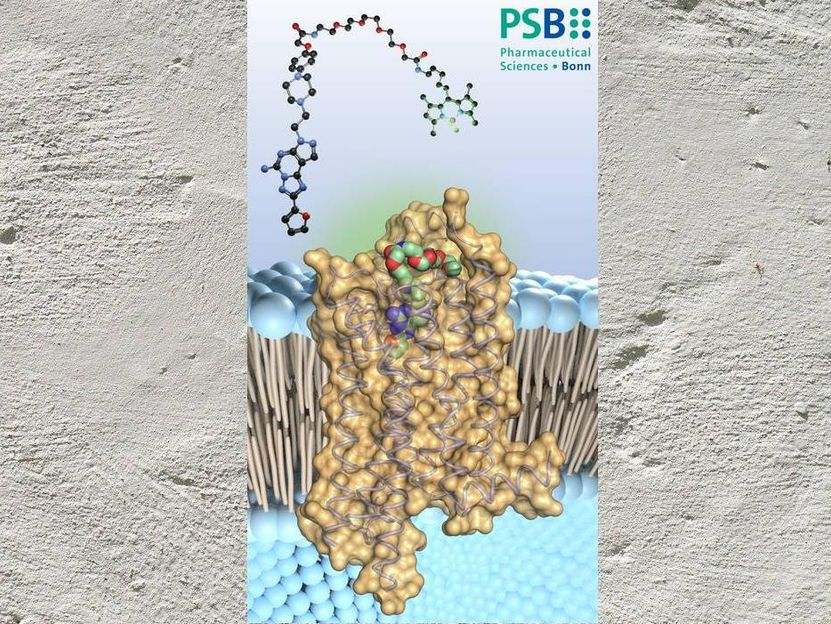
bindet an winzige Antennen auf der Oberfläche der Immunzellen, die Adenosin-Rezeptoren vom Typ 2A. Dadurch werden die Abwehrtruppen ausgebremst.
Pharmazeutische & Medizinische Chemie/Uni Bonn
Wer gerne Krimis liest, weiß: Bevor Diebe in eine Villa einbrechen, werfen sie gerne einmal ein saftiges Kotelett über den Zaun, in dem sie ein paar Schlaftabletten versteckt haben. Wenn sich die Wachhunde über das zweite Abendessen hermachen, versinken sie kurz darauf in einen tiefen Schlummer. Die Juwelen der Hausherrin wechseln danach sehr viel ungestörter ihren Besitzer.
Tumorzellen gehen oft ganz ähnlich vor: Sie werfen Schlaftabletten aus, die das Immunsystem lähmen. Genauer gesagt, umgeben sie sich mit einer Wolke aus Adenosin, eines wichtigen körpereigenen Botenstoffs. Damit setzen sie körpereigene „Killerzellen“ außer Gefecht, die die Krebszellen ansonsten in den Tod treiben würden.
Die Adenosin-Moleküle binden nämlich an winzige Antennen auf der Oberfläche der Immunzellen, die A2A-Rezeptoren (das Kürzel steht für „Adenosin-Rezeptoren vom Typ 2A“). Dadurch werden die Abwehrtruppen gewissermaßen ausgeknockt. Forschende rund um den Globus suchen daher nach Molekülen, die den A2A-Rezeptor blockieren und die lähmende Wirkung von Adenosin verhindern können.
Beschuss mit Röntgenstrahlen
„Unsere Studie dürfte diese Suche ein großes Stück einfacher machen“, erklärt Prof. Dr. Christa Müller vom Pharmazeutischen Institut der Universität Bonn. „Wir haben den A2A-Rezeptor mit neuartigen Varianten eines bekannten Hemmstoffs versetzt, einer Substanz namens Preladenant. Dann haben wir aus den Rezeptor-Hemmstoff-Komplexen Kristalle hergestellt - es ist weltweit das erste Mal, dass das mit Preladenant-artigen Wirkstoffen gelungen ist.“
Die Kristallisierung erlaubte es, die Struktur des Komplexes aufzuklären. „Wir beschießen die Verbindung dazu mit Röntgenstrahlung“, erklärt Tobias Claff, der den Hauptteil der Experimente durchgeführt hat. „Der Kristall lenkt die Strahlen ab. Aus der Art und Weise, wie er das tut, lässt sich dann auf die räumliche Struktur des Komplexes schließen - bis hin zur Anordnung einzelner Atome und ihrer Wechselwirkungen.“
Auf diese Weise konnten die Forschenden zeigen, an welche Punkte des A2A-Rezeptors Preladenant bindet. Mit diesem Wissen ist es nun möglich, den Hemmstoff gezielt so abzuwandeln, dass er bessere Eigenschaften bekommt. Neben einer möglichst starken Wirkung sollen Arzneistoffe beispielsweise nicht zu schnell abgebaut werden. Außerdem müssen sie gut an den Ort gelangen, wo sie ihre Arbeit verrichten sollen - in diesem Fall ins Gehirn. „Unsere Studie wird es deutlich erleichtern, den Wirkstoff zu optimieren“, ist Claff optimistisch.
A2A gehört zu einer Gruppe von Rezeptoren, die im Körper ganz zentrale Aufgaben regulieren. Sie durchspannen die Membran von Zellen. Der Teil von ihnen, der auf der Außenseite der Membran sitzt, dient dabei als Sensor - er empfängt wie eine Antenne molekulare Signale. Wenn er das tut, stößt er mit seinem in die Zelle ragenden Anteil spezifische Reaktionen an. Dadurch werden dann etwa bestimmte Gene aktiviert.
Farbstoff an das hemmende Molekül gebunden
„Diese Rezeptoren sind aufgrund ihrer zentralen Stellung immens wichtig“, sagt Christa Müller, die auch Mitglied in den Transdisziplinären Forschungsbereichen (TRA) „Bausteine der Materie“ und „Leben und Gesundheit“ ist. „Viele von ihnen sind aber leider relativ instabil. Für Röntgenstrukturanalysen ist das ungünstig – die Kristallisation dauert Tage, manchmal sogar Wochen.“ Die Forschenden haben daher den A2A-Rezeptor an einem einzigen Punkt gezielt verändert, wodurch er erheblich stabiler wurde.
Zusätzlich ist es ihnen gelungen, mit einer Art molekularen Schnur an dem Preladenant einen Farbstoff zu befestigen. „Wir können so kontrollieren, wo im Gewebe sich Preladenant an den A2A-Rezeptor heftet“, sagt Müller. Die Länge und Flexibilität des Nanoseils stellt zugleich sicher, dass die Bindung des Hemmstoffs an den Rezeptor nicht behindert wird.
Beide Fortschritte könnten auch als Vorbild für die Arbeit mit anderen Rezeptoren dienen, die zur selben Gruppe gehören. „Die Methoden, die wir in Bonn in den letzten Jahren entwickelt haben, werden es uns in Zukunft erlauben, die Struktur solcher und weiterer Zellmembranproteine aufzuklären“, ist die Pharmazeutin überzeugt. „Es gibt nicht viele Forschungseinrichtungen, die solche Strukturanalysen äußerst komplexer Moleküle beherrschen.“
Beteiligte Institutionen und Förderung:
Neben der Universität Bonn waren das Centre for Structural Systems Biology (CSSB) und das Forschungszentrum Jülich beteiligt. Die Studie wurde durch die Deutsche Forschungsgemeinschaft und das Bundesministerium für Bildung und Forschung gefördert.
Originalveröffentlichung
Publikation: Tobias Claff, Dr. Tim A. Klapschinski, Dr. Udaya K. Tiruttani Subhramanyam, Victoria J. Vaaßen, Jonathan G. Schlegel, Christin Vielmuth, Jan H. Voß, Prof. Dr. Jörg Labahn and Prof. Dr. Christa E. Müller: Single Stabilizing Point Mutation Enables High-Resolution Co-Crystal Structures of the Adenosine A2A Receptor with Preladenant Conjugates, Angewandte Chemie International Edition.