Ein unverzichtbarer Boxenstopp für die Kopiermaschine der Gene
Wie ein Protein für saubere Arbeitskopien von Genen sorgt
Auf dem Enzymkomplex, der Gene von der DNA abliest, fahren andere Proteine „Huckepack“ bis zu ihrem Einsatzort. Essentiell ist dafür das Protein BRD4, an das die Faktoren während einer Arbeitspause andocken. Das komplexe Zusammenspiel der Faktoren erlaubt es der Zelle auch, in den Prozess steuernd einzugreifen.
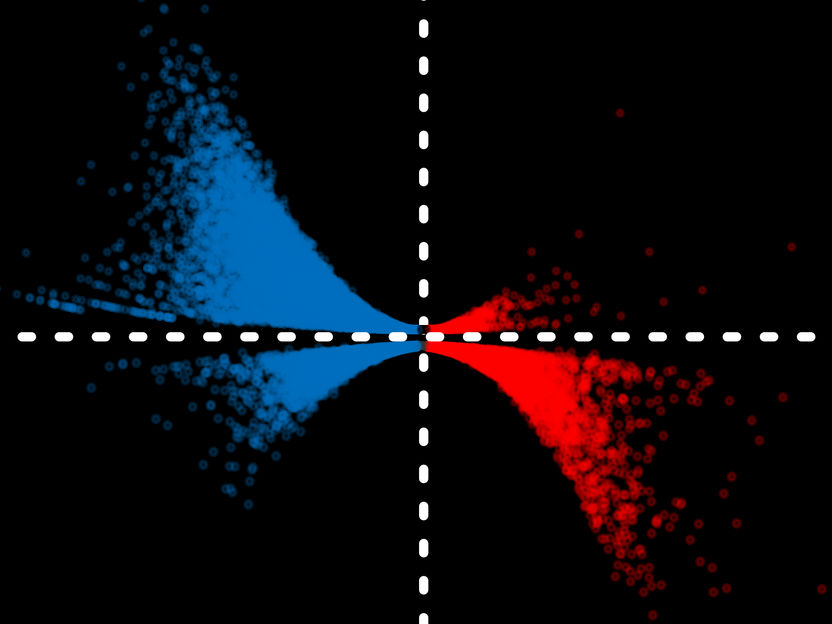
Künstlerische Darstellung basierend auf tatsächlichen Ergebnissen eines Detektionsverfahrens für RNA-Polymerase-Moleküle auf Genabschnitten. In der oberen Bildhälfte überwiegt die blaue Punktwolke, was einen generellen Verlust der Polymerase an Genen symbolisiert. In der unteren Hälfte die Ergebnisse eines älteren Verfahrens, mit dem diese Veränderungen nicht gemessen werden konnten.
Annkatrin Bressin MPI f. molek. Genet.
Von der Erbinformation bis zu einem erkennbaren Merkmal ist es ein langer Weg. Denn damit Gene in Eiweißstrukturen münden oder sogar die Entwicklung eines ganzen Organismus steuern, muss einiges geschehen. Als erstes muss die Zelle das Gen von der DNA ablesen („Transkription“): Sie lässt einen Enzymkomplex auf dem Erbgutfaden entlang fahren und so eine Arbeitskopie des Gens aus RNA anfertigen. Doch schon kurz nach dem Start hält das Kopier-Enzym wieder an.
Bei diesem Boxenstopp sammelt der Komplex, der sich aus der RNA-Polymerase und einigen Helfer-Proteinen zusammensetzt, weitere Enzyme und Faktoren ein. Sie sorgen dafür, dass er überhaupt weiter am Gen entlang fahren kann. Zudem helfen sie, dass der Komplex die RNA-Arbeitskopie zum Schluss korrekt weiterverarbeitet. Eine wesentliche Rolle kommt dabei dem Protein BRD4 zu, das an die beteiligten Moleküle andockt und sie so dorthin entlang des Gens bringt, wo sie gebraucht werden. Dies fand ein Forschungsteam um Andreas Mayer vom Max-Planck-Institut für molekulare Genetik (MPIMG) in Berlin heraus. Die Ergebnisse erschienen im Fachjournal Molecular Cell.
Folgen einer präzisen Störung beobachtet
„Eine Vielzahl von Laboren weltweit forscht derzeit an BRD4 als Zielstruktur für Medikamente, vor allem weil es bei der Entstehung verschiedener Krebsarten, wie etwa von Karzinomen, beteiligt ist“, sagt Mayer. „Unser Ziel war, die grundsätzlichen Aufgaben von BRD4 bei der Transkription und bei der Weiterverarbeitung der RNA in menschlichen Zellen zu verstehen.“
Um die Funktionen von BRD4 zu entschlüsseln, untersuchte die Max-Planck-Forschungsgruppe das Protein an Kulturen von humanen Zellen. Die Forschenden verwendeten eine neue Methode, mit der sie alle BRD4-Moleküle selektiv und innerhalb von nur zwei Stunden aus den Zellen entfernen konnten, ohne dabei die Funktionen von anderen Proteinen in der Zelle zu beeinträchtigen.
„Wir verfolgen das Prinzip, einerseits sehr schnell und spezifisch auf Proteinebene zu intervenieren und andererseits mit ähnlich hoher zeitlicher Auflösung die unmittelbaren Folgen für die Zelle zu messen, noch bevor alles von Stressreaktionen überlagert wird“, sagt Mayer. „Wir streuen Sand in das Getriebe und schauen direkt zu, was danach passiert – nicht erst, wenn die Maschine schon längst zum Stillstand gekommen ist.“
Auf halber Strecke liegen geblieben
Die Forschenden beobachteten, wie die Zelle auf den plötzlichen Verlust des BRD4-Proteins reagierte. Dazu sequenzierten sie etwa in kurzen Zeitabständen die RNA-Moleküle, die bei der Transkription neu entstehen.
„Wir konnten sehen, wie die Transkription global und einheitlich zurückging“, sagt Mirjam Arnold, Doktorandin im Team von Andreas Mayer und Erstautorin der neuen Forschungsarbeit. Der Grund: die Kopiermaschinen verweilten deutlich länger in einem Streckenabschnitt direkt hinter dem Start des Gens und waren seltener im restlichen Bereich des Gens aufzufinden. Offenbar waren sie steckengeblieben.
„Bei vielzelligen Organismen ist es die Regel, dass die RNA-Polymerase losläuft und dann nach 50 bis 100 Nukleotiden erstmal pausiert und wartet, bis es weitergehen kann“, sagt Arnold. „Nun pausierte die Polymerase aber sehr viel länger als normalerweise und schien in ihrer Funktion massiv eingeschränkt zu sein.“
Über das Ziel hinausgeschossen
Zudem schoss der Enzymkomplex bei mindestens 40 Prozent der Gene über die Zielgerade hinweg und kopierte noch mehrere Tausend DNA-Buchstaben aus dem Bereich hinter dem eigentlichen Gen. Es entstanden überlange RNA-Moleküle, die zu einem großen Teil aus Nonsens bestanden und für Chaos in der Zelle sorgen können.
„Es war die Überraschung schlechthin, dass wir einen solchen Defekt am Ende der Gentranskription sehen konnten“, sagt Annkatrin Bressin, ebenfalls Doktorandin und Erstautorin. „Dem Enzymkomplex fehlten sozusagen die Bremsen, um anhalten zu können. Außerdem wurde die RNA anschließend nicht korrekt fertig verarbeitet.“
So hing in einigen Fällen die RNA immer noch fest an dem Enzymkomplex und wurde nicht wie vorgesehen geschnitten und abgetrennt. Auch folgende Verarbeitungsschritte wie die Polyadenylierung, bei der Enzyme einen Schwanz aus bis zu 250 Adenin-Bausteinen an das Ende der RNA anfügen, wurden gar nicht erst angestoßen.
Effekte an entgegengesetzten Enden des Gens
Die scheinbar widersprüchlichen Befunde stellten die Forschenden vor ein Rätsel. Wie hängen die Effekte an den gegenüberliegenden Enden desselben Gens zusammen? Die Erklärung lieferte unter anderem eine massenspektrometrische Suche nach den Molekülen, die im Laufe der Zeit an BRD4 andocken und wieder verloren gehen. Die Versuche dazu entstanden in Zusammenarbeit mit David Meierhofer vom MPIMG, der auf solche Analysen spezialisiert ist.
Es zeigte sich, dass BRD4 an die RNA-Polymerase bindet und zunächst während des initialen Boxenstopps unweit der Startregion auf weitere Signale wartet. Diese kommen in Form von Elongationsfaktoren – diese Proteine motivieren die Polymerase, ihre Arbeit fortzusetzen. Bleiben sie aus, wird das Gen einfach nicht weiter abgelesen und die Transkription bricht ab. BRD4 hilft dabei, die Elongationsfaktoren anzulocken.
Gleichzeitig treten aber schon in dieser frühen Phase die sogenannten RNA-Prozessierungsfaktoren direkt mit BRD4 in Kontakt – mehr als ein dutzend Proteine, die das transkribierte RNA-Molekül schneiden und in seine endgültige Form bringen. Sie werden durch die RNA-Polymerase Huckepack bis zu ihrem Einsatzort getragen. Fehlen sie dort, entsteht letztlich fehlerhafte RNA, mit der die Zelle nichts anfangen kann oder ihr sogar schadet.
Stellschrauben für komplexe Regeltechnik
„BRD4 scheint extrem wichtig zu sein, damit überhaupt erst der Enzymkomplex entsteht, der funktionsfähige RNA-Moleküle produziert“, sagt Mayer. „Das Protein ist für die Elongationsphase, in der die RNA-Kette Glied für Glied gebaut wird, einer der zentralen Stellschrauben.“
Denn nicht nur der Start der Gentranskription, auch Initiationsphase genannt, sei eine Möglichkeit, die Aktivität eines Gens zu steuern, sagt Mayer. Auch bei der Verlängerung der RNA-Kopie sowie bei den Prozessen am Ende der Transkription könne die Zelle regulierend eingreifen. Je nach Bedarf kann sie den Vorgang hier wieder abbrechen.
Das neue Hintergrundwissen über die Funktionsweise von BRD4 könnte auch in die klinische Anwendung einfließen. „In der Krebsforschung wurde beobachtet, dass BRD4 andere Gene, die bei der Entstehung unterschiedlicher Krebsarten beteiligt sind, anschaltet oder angeschaltet hält, weshalb man es mit chemischen Wirkstoffen unterdrücken will. Doch die genauen Aufgaben und der Wirkmechanismus des Proteins waren nicht genau aufgeklärt“, sagt der Wissenschaftler. „Nachdem wir die Funktion des Proteins nun immer besser verstehen, können in Zukunft möglicherweise Medikamente entwickelt werden, die präziser in das Geschehen eingreifen, damit wirksamer sind und gleichzeitig weniger Nebenwirkungen hervorrufen.“