Neuer Sensor für SARS-CoV-2 und andere Viren
Bessere und schnellere Viruserkennung mit Einzel-Nanopor-Membranen
Der einfache und schnelle Nachweis von Viren ist in einer Pandemie entscheidend. Auf der Basis von Single-Nanopor-Membranen von GSI hat ein internationales interdisziplinäres Forscherteam ein Testverfahren entwickelt, das SARS-CoV-2 mit der gleichen Empfindlichkeit wie ein qPCR-Test und in nur zwei Stunden in Speichel nachweist, ohne dass die Probe vorbehandelt werden muss. Darüber hinaus kann der Sensor infektiöse von nicht-infektiösen Coronaviren unterscheiden – eine entscheidende Innovation.
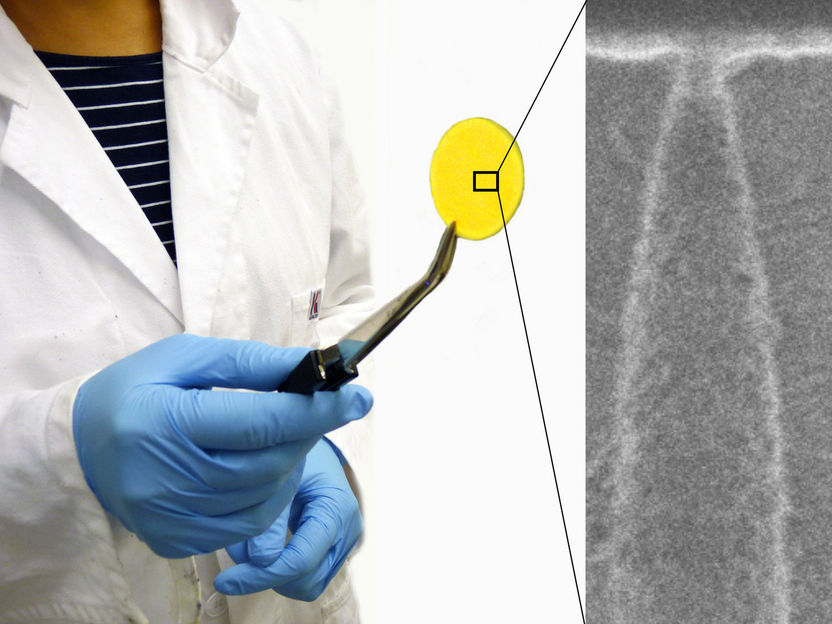
Durch die Ionen-Spur-Nanotechnologie der GSI-Materialforschung entsteht eine hochempfindliche Nanopore.
GSI/FAIR
Durch die Verknüpfung verschiedener Technologien hat ein interdisziplinäres Team von Wissenschaftlern der Materialforschung des GSI Helmholtzzentrums für Schwerionenforschung, des Nationalen Wissenschaftlichen und Technischen Forschungsrates (CONICET) in Argentinien und der University of Illinois in den USA einen hochempfindlichen Nanoporen-Sensor entwickelt, der gezielt SARS-CoV-2-Viren und humane Adenoviren in verschiedensten Proben wie Speichel, Serum oder Umweltproben wie Abwasser nachweist. Der Sensor kombiniert zwei Schlüsselkomponenten: einen empfindlichen Nanokanal und hochspezifische DNA-Moleküle, die an der Kanaloberfläche angebracht sind. Nach Angaben der Forschungsgruppen ist die Methode genauso präzise wie PCR-Tests, aber einfacher und schneller und liefert Ergebnisse in weniger als zwei Stunden. Die Ergebnisse wurden in der Fachzeitschrift Science Advances veröffentlicht.
Die Technologie zur Herstellung von Membranen mit einzelnen Nanoporen wurde am GSI über viele Jahre entwickelt. Dünne Polymerfilme werden am Linearbeschleuniger UNILAC mit einem einzelnen hochenergetischen Schwerionenprojektil (z.B. 1 GeV Goldion) beschossen. Dort, wo das Ion die Folie passiert, erzeugt es eine nanoskopische Schadensspur, die durch chemisches Ätzen in einen offenen Nanokanal umgewandelt wird. Der Durchmesser und die Form des Kanals werden durch die Ätzparameter eingestellt. Für diese Arbeit wurden asymmetrische Nanoporen mit einer kleinen Öffnung von weniger als 50 Nanometern hergestellt. Die geringe Größe und die spezifische Geometrie gewährleisten eine besonders hohe Empfindlichkeit für Transportprozesse durch den Kanal.
Die Selektivität des Sensors wird durch einen In-vitro-Selektionsprozess für DNA-Fragmente erreicht, sogenannte Aptamere, die in die Nanopore eingebaut werden. Diese Aptamere sind nicht nur in der Lage, das Virus zu erkennen, sondern können auch erkennen, ob es infektiös ist oder nicht. Die hier verwendeten Aptamere wurden von Ana Sol Peinetti während ihrer Arbeit als Postdoktorandin an der University of Illinois in Urbana-Champaign entwickelt. Da sie mit der GSI-Nanoporen-Technologie durch ihre vorherige Arbeit mit der Gruppe von Omar Azzaroni am Institut für theoretische und angewandte physikalisch-chemische Forschung (INIFTA, CONICET-UNLP) (Argentinien) vertraut war, konnte sie beide Technologien erfolgreich kombinieren.
Dass mit dieser Methode infektiöse und nicht infektiöse Viren unterschieden werden können, ist laut den Wissenschaftler*innen eine wesentliche Neuerung. Die bekannten PCR-Tests weisen virales Erbgut nach, können aber nicht unterscheiden, ob eine Probe infektiös ist oder ob eine Person ansteckend ist. Die einzigen Tests, die derzeit infektiöse Viren nachweisen können, sind Plaque-Tests. Sie erfordern eine spezielle Vorbereitung und tagelange Inkubation, bevor sie Ergebnisse liefern, während der neue Aptamer-Nanoporen-Sensor Ergebnisse innerhalb von 30 Minuten bis zu zwei Stunden liefert und keine Vorbehandlung der Probe nötig ist.
Ob ein Virus infektiös ist oder nicht gibt nicht nur Aufschluss darüber, ob Patienten ansteckend sind, sondern bietet auch eine Möglichkeit, herauszufinden, ob bestimmte Inaktivierungsstrategien tatsächlich funktionieren. "Zusammen mit Omar Azzaroni und Ana Sol Peinetti (jetzt Gruppenleiterin am Institut für Chemie, Physik der Materialien, Umwelt und Energie in Buenos Aires) arbeiten wir in einem neuen Projekt zusammen, in dem auf der Grundlage dieses neuen Sensors die Effizienz verschiedener Virusinaktivierungsprotokolle getestet werden soll", erklärt Maria Eugenia Toimil-Molares, Leiterin der Ionen-Spur-Nanotechnologiegruppe bei GSI.
Die Nanoporen-Sensortechnologie hat auch über die Corona-Pandemie hinaus großes Potenzial. "Um andere Viren nachzuweisen, muss man nach einem Pool von Molekülen suchen, die als Aptamere dienen: neue Moleküle für neue Viren. Wir beabsichtigen sogar, Aptamere zu erhalten, die zwischen verschiedenen Varianten von SARS-Cov-2 unterscheiden können", erklärt Peinetti. In der Veröffentlichung zeigen die Autoren auch den Nachweis infektiöser humaner Adenoviren, die weltweit für wasserbedingte Atemwegserkrankungen verantwortlich sind.
Über den Virusnachweis hinaus bildet die GSI-Nanoporentechnologie die Grundlage für weitere Sensoroptionen. Zahlreiche Gruppen auf der ganzen Welt entwickeln spezifische Funktionalisierungsstrategien, um Nanoporen-Sensoren selektive Funktionalitäten zu verleihen. Nanoporen in Ionenspurmembranen sind sehr vielseitig, da sie so modifiziert werden können, dass sie auf viele verschiedene äußere Veränderungen wie Temperatur, pH-Wert, Licht, Spannung oder das Vorhandensein bestimmter Ionenspezies, Moleküle oder Medikamente reagieren. In den letzten Jahren wurden in Zusammenarbeit mit den Kollegen am INIFTA mehrere hochempfindliche Nanoporen-Sensorplattformen entwickelt. "Unsere Vision ist es, die funktionalisierte Nanoporenmembran in ein tragbares Gerät zum schnellen und effizienten Nachweis und zur Diagnose von Viren zu integrieren", sagt Christina Trautmann, Leiterin der GSI-Abteilung Materialforschung.