Proteine auf Abstand
Forscher haben eine neue Methode entwickelt, um Proteine auf der Oberfläche von virusartigen Partikeln anzubringen
Zum ersten Mal haben Forscher am Paul Scherrer Institut PSI zwei Proteine über eine frei stehende, starre Verbindung miteinander verknüpft. Das Brückenglied hält die beiden Eiweissmoleküle in einem definierten Abstand und Winkel zueinander − ähnlich dem Griff einer Hantel zwischen zwei Gewichten. Diese Art von Verknüpfung kann beispielsweise dabei helfen, sogenannte virusartige Partikel für Impfstoffe zu entwickeln. Die Forscher veröffentlichen ihre Ergebnisse in der Fachzeitschrift Structure.
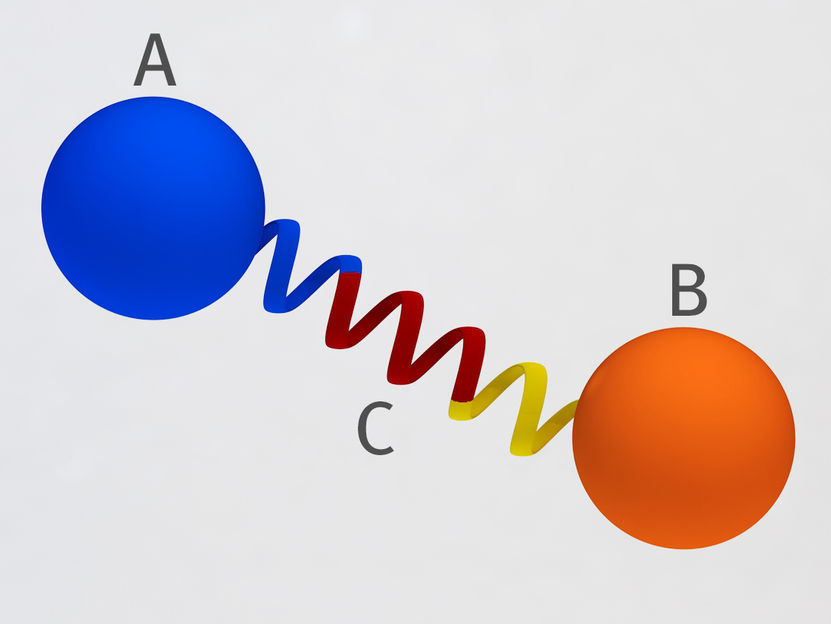
Prinzip der am PSI entwickelten Eiweissbrücke: Zwei Proteine (A und B) sind durch eine starre Proteinspirale (C) in festem Abstand und Winkel miteinander verknüpft. So können sie sich nicht nahekommen und nicht miteinander interagieren.
Mahir Dzambegovic, Paul Scherrer Institut
«Proteine wurden in der Evolution über Jahrmillionen optimiert», sagt Molekularbiologe Roger Benoit vom PSI-Labor für Biologie im Nanobereich. «Wo Proteine starr sein müssen, sind sie das in der Natur auch. Aber das im Labor nachzuahmen, ist schwierig.»
Wer zwei Proteine über eine Eiweissbrücke in definiertem Abstand und Winkel miteinander verknüpfen will, hat es schwer. Das Bindeglied entpuppt sich meistens als zu flexibel, die beiden Proteine kommen sich dadurch zu nahe. Das ist so, als würde man zwei Gewichte mit einem Seil verbinden. Sobald man das Seil anhebt, bis die Gewichte frei schwingen können, nähern sich die Gewichte einander an. Wenn sich Eiweissmoleküle nahekommen, können sie allerdings interagieren. Die Kontakte zwischen den Proteinen schränken oft die natürliche Bewegungsfreiheit in der Struktur ein – die Moleküle bewegen sich anders, als das ohne Kontakt zu dem anderen Protein der Fall wäre.
Es gäbe viele Anwendungen für Verbindungen mit geringerer Flexibilität, doch das Design ist schwierig. «Wie sich die Proteine falten und wie ihre Struktur in der Realität aussieht, lässt sich oft nur schwer voraussagen», sagt Benoit. Sprich: Mehrere Proteine lassen sich meistens nur mit extrem aufwendiger Optimierung im Labor in gewünschtem Abstand und Orientierung aneinanderreihen.
Roger Benoit und sein Team haben jetzt eine Lösung dafür gefunden. Sie verwendeten ein Segment eines Proteins, das beispielsweise an der Wundheilung im menschlichen Körper beteiligt ist. Ein Teilstück dieses Proteins bildet eine Helix, also eine Art Spirale. Deren Rückgrat wird durch Wechselwirkungen zwischen ihren Seitenketten stabilisiert. Dadurch bleibt die Helix alleinstehend intakt und ist recht starr – quasi wie eine Metallspirale aus gehärtetem Stahl. Damit verknüpfte Benoit erfolgreich mehrere Proteine in der gewünschten Weise miteinander.
Auf die Hantelanalogie übertragen heisst das: Die Forschenden haben die Proteine statt mit einem Seil nun mit einer Metallspirale verbunden und so auf einen konstanten Abstand gebracht. Auch legten sie die Orientierung der beiden Proteine zueinander fest.
Input für neue Impfstoffe
Solche starren Verbindungen haben das Potenzial für viele praktische Anwendungen. Unter anderem könnte es bei der Entwicklung von Impfstoffen gegen Viren helfen, auch gegen Sars-CoV-2.
Oft stellt man Impfstoffe her, indem man die Krankheitserreger inaktiviert. Sie können dem Menschen dann nicht mehr schaden, regen aber das Immunsystem an, Antikörper zu bilden. Eine andere Möglichkeit bieten sogenannte virus-like particles, im Labor nachgebaute virusartige Partikel. Auf deren Oberfläche bringt man viele charakteristische Oberflächenproteine eines Virus an, sodass das Immunsystem sie wahrnimmt und daraufhin ebenfalls Antikörper bildet.
Virus-like particles bieten den Vorteil, dass sie kein Erbmaterial des Erregers enthalten und somit jegliche Wahrscheinlichkeit ausgeschlossen ist, dass sie sich vermehren. Sie sind daher sicherer als abgeschwächte Krankheitserreger und werden derzeit für mehrere Viren erforscht, etwa für Hepatitis B und humane Papillomviren.
Mit dem Verbindungsstück lassen sich die Virusproteine auf der Oberfläche solcher virusartigen Partikel genauer anbringen. Denn die Starrheit der Helix bietet Vorteile: «Ist die Verbindung zwischen Partikel und Virusprotein zu flexibel, können sich die Proteine möglicherweise wieder zurückfalten und sind dann nicht mehr so präsent», erklärt Benoit. Das Immunsystem erkennt sie weniger gut. Stehen die Proteine mehr von den Partikeln ab und präsentieren sich alle in einem bestimmten Winkel und Abstand, wie es mit dem Abstandhalter möglich ist, liessen sich bessere und wirksamere Impfstoffe damit entwickeln.
Knochen und Seide
Auch neue Biomaterialien lassen sich so erschaffen, hofft Benoit. Die Helix könnte als Baustein in Kombination mit anderen Proteinen dienen. So können Forschende in Zukunft womöglich 3-D-Proteingerüste bauen, um beispielsweise ein Stück Knochen zu ersetzen. «Oder man kann Proteine damit zu langen Schnüren verbinden und so neue seidenartige Textilien erschaffen, die dann sogar biologisch abbaubar sind.»
Auch Forschende am PSI und an Forschungsinstituten weltweit, die an der Strukturaufklärung von Proteinen arbeiten, profitieren von der neuen Methode. Denn Eiweissmoleküle, die über die unbiegsame Helix verknüpft sind, lassen sich so optimieren, dass sie kristallisieren und in den Kristallen ihre natürliche Bewegungsfreiheit beibehalten. Das erleichtert die Untersuchung ihrer Struktur. Mit neuen Methoden der Proteinkristallstrukturanalyse, zum Beispiel mit dem Freie-Elektronen-Röntgenlaser SwissFEL am PSI, lassen sich sogar Proteine in Aktion beobachten, beispielsweise wenn Membranpumpen Substanzen aus der Zelle heraustransportieren.