Wie resistente Keime Gift auf molekularer Ebene transportieren
Erkenntnisse können helfen, Wirkmechanismen gegen gefährliche Erreger zu entwickeln
Um der zunehmenden Bedrohung durch multiresistente Keime zu begegnen, ist das Verständnis der Resistenzmechanismen zentral. Eine wichtige Rolle dabei spielen Transportproteine. Ein deutsch-britisches Forschungsteam unter Leitung der Heinrich-Heine-Universität Düsseldorf (HHU) beschreibt nun in der Fachzeitschrift Nature Communications die dreidimensionale Struktur des Transportproteins Pdr5, das ähnlich auch bei humanpathogenen Pilzen vorkommt. Die Ergebnisse können helfen, Wirkmechanismen gegen gefährliche Erreger zu entwickeln.
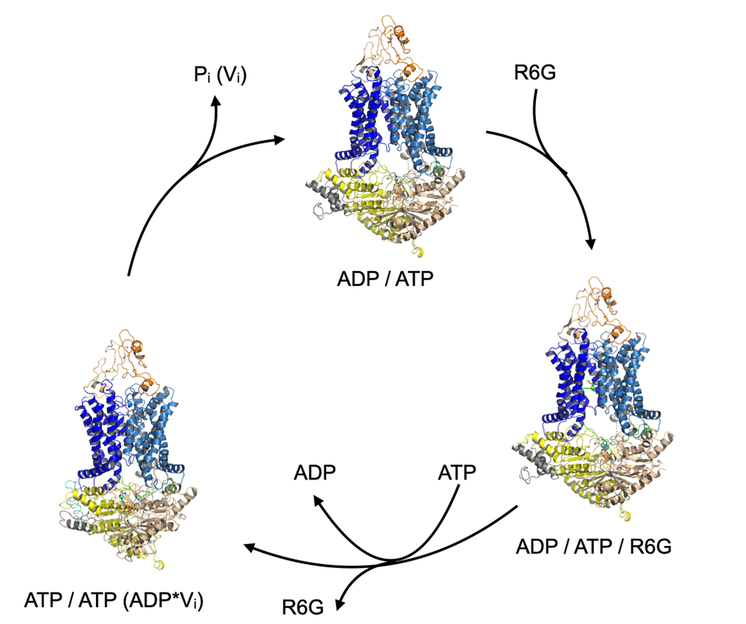
Transportzyklus des ABC-Transporters Pdr5 (orange/ blau / gelb), Zyklus durch Bindung und Hydrolyse von ATP zu ADP. Das Substrat Rhodamin 6G (grün) wird an einem bestimmten Punkt des Zyklus gebunden und in einem folgenden Schritt wieder abgegeben.
HHU / Lutz Schmitt
Für den klinischen Alltag ist die Resistenz von Mikroorganismen gegen Wirkstoffe, speziell gegen Antibiotika, ein großes Problem. Die Zahl resistenter Mikroben nimmt dabei drastisch zu. Aufgrund dessen können Infektionen inzwischen wieder für Menschen lebensbedrohlich werden, die bereits mit modernen Medikamenten besiegt schienen. Die Situation wird weiter dadurch kompliziert, dass vermehrt multiresistente Keime auftreten, die gleich vor mehreren Antibiotika oder anderen Wirkstoffen gefeit sind.
Die Forschung untersucht die Mechanismen, mithilfe derer sich Mikroben gegen die für sie giftigen Stoffe wappnen. Unter anderem transportieren sie die Giftstoffe aktiv aus der Zelle heraus, bevor sie Schaden anrichten können. Sie nutzen dazu spezielle Membrantransportproteine. Insbesondere in eukaryotischen Mikroben – solchen mit einem Zellkern, im Gegensatz zu den Bakterien, die keinen Zellkern besitzen – wie Pilzen gehören diese Membranproteine der Familie der ABC-Transporter („ATP binding cassette“) an; sie exportieren die Giftstoffe, indem sie den zellulären Energieträger ATP aufspalten.
Ein deutsch-britisches Forschungsteam unter der Leitung von Prof. Dr. Lutz Schmitt vom Institut für Biochemie der HHU stellt in einer aktuellen Publikation in Nature Communications die dreidimensionale Struktur des ABC-Transporters Pdr5 aus einem Pilz in mehreren funktionalen Zustände vor. Sie bestimmten diese Strukturen mithilfe der Einzelpartikel-Kryoelektronenmikroskopie, mit der insbesondere biologische Moleküle mit höchster Auflösung und in ihrer natürlichen Form untersucht werden können, indem sie auf tiefe Temperaturen schockgefroren werden.
Das Forschungsteam zeigte, dass Pdr5 nicht nur ein zentrales Transportprotein ist, durch das die Membranprotein-vermittelten Resistenzen bewirkt wird. Anhand der aufgelösten Strukturen konnte sowohl die Substratbindestelle lokalisiert als auch der Transportzyklus definiert werden.
Pdr5 stellt seit mehr als 30 Jahren das Modellsystem für PDR-Proteine aus humanpathogenen Pilzen – wie etwa Candida albicans, das Candidiasis verursacht – dar. Die neuen Ergebnisse helfen zu erklären, was auf molekularer Ebene ein einziges Membranprotein befähigt, viele strukturell unterschiedliche Moleküle effizient am Eintritt in die Zelle zu hindern bzw. effizient aus der Zelle herauszutransportieren. Auf dieser Grundlage kann nun begonnen werden, gezielt neue Wirkstoffe zu designen, die den Resistenzen entgegenwirken.
Seit fast 20 Jahren forscht die Arbeitsgruppe von Prof Schmitt daran, die Wirkungsweise des Transportproteins aufzuklären. Die Strukturaufklärung gelang durch gemeinsame Arbeit mit der Gruppe um Prof. Dr. Ben Luisi vom Department of Biochemistry der Universität Cambridge. Ebenfalls an der HHU beteiligt waren die Arbeitsgruppe um Prof. Dr. Holger Gohlke vom Institut für Medizinische und Pharmazeutische Chemie und das Center for Structural Studies (Leitung Dr. Sander Smits).
Originalveröffentlichung
Meistgelesene News
Originalveröffentlichung
Andrzej Harris, Manuel Wagner, Dijun Du, Stefanie Raschka, Lea-Marie Nentwig, Holger Gohlke, Sander H. J. Smits, Ben F. Luisi & Lutz Schmitt; "Structure and efflux mechanism of the yeast pleiotropic drug resistance transporter Pdr5"; Nature Communications; (2021)12:5254.
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte
Dysplastischer_Nävus
Basedow-Krankheit

Neue Einblicke in die Genetik des Gemeinen Kraken: Genom auf Chromosomenebene entschlüsselt - Wissenschaftlicher Meilenstein ermöglicht vertiefte Einblicke in die Evolution und Biologie von Octopus vulgaris
Scailyte sammelt CHF 2.75 Mio. an Seedfinanzierung - Investitionen von Swisscom Ventures & Zürcher Kantonalbank
Schädliche Wirkung auf Embryonen frühzeitig in vitro testen - Neuer Zellkultur-Test spart Kosten und reduziert Tierversuche
Effloreszenz
Kategorie:Nuklearmediziner

Neue Echtzeit-Methode für die Umweltüberwachung - Hyperspektrale Bildgebung
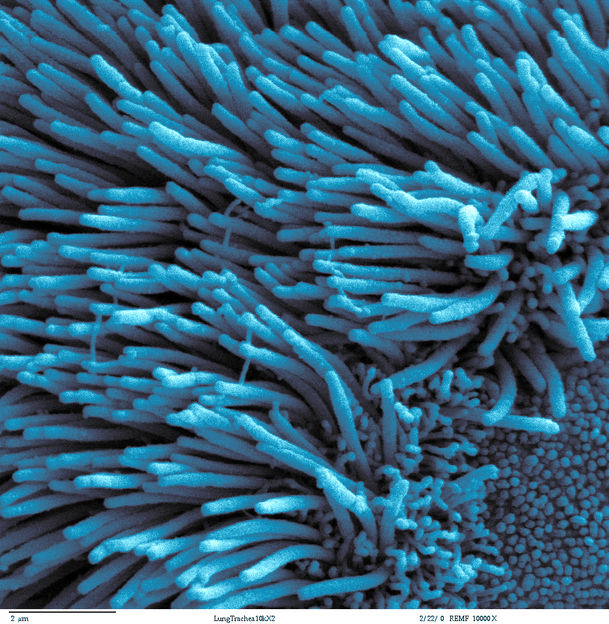
Flimmern in den Atemwegen erwünscht - Forscherteam klärt wichtigen Regulationsmechanismus bei der Flimmerhärchenbildung in Zellen der Luftröhre und Lunge auf
Entfesselte RNA-Moleküle mit therapeutischem Potenzial - EXIST-Forschungstransferförderung für Ausgründung aus dem Plazenta-Labor des Universitätsklinikums Jena
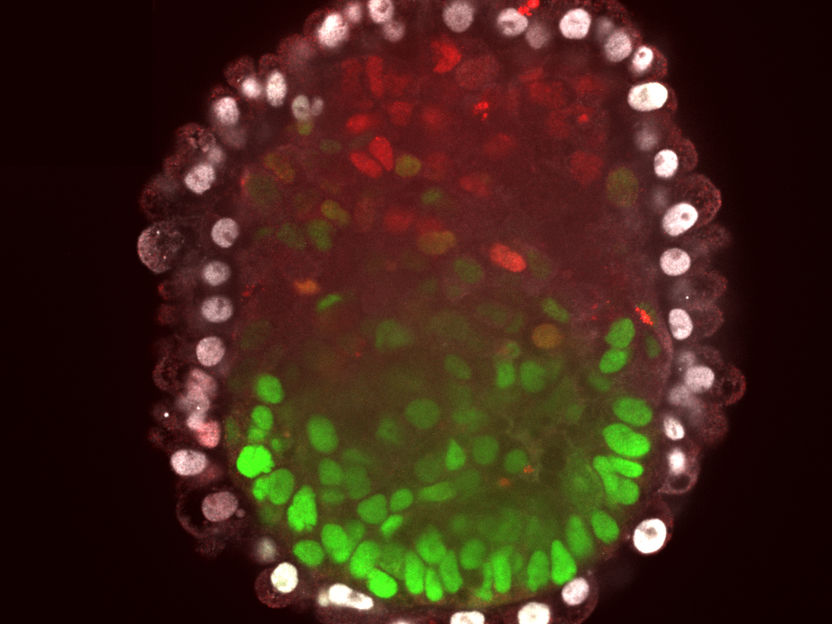
Stammzellen organisieren sich selbsttätig zum Embryoid - Studie an Mäusen könnte mittelfristig Alternativ-Methoden zu Tierversuchen ermöglichen





















































