Wie SARS-CoV-2 in das Gehirn gelangt
Erstmals elektronenmikroskopische Aufnahmen intakter Coronaviruspartikel in der Riechschleimhaut erstellt
Ein Forschungsteam der Charité – Universitätsmedizin Berlin hat anhand von Gewebeproben verstorbener COVID-19-Patienten analysiert, auf welche Weise das neuartige Coronavirus ins Gehirn eindringen kann und wie das Immunsystem dort auf das Virus reagiert. Die jetzt in Nature Neuroscience veröffentlichten Ergebnisse zeigen, dass SARS-CoV-2 über die Nervenzellen der Riechschleimhaut in das Gehirn übertritt. Den Forschenden ist es dabei erstmals gelungen, elektronenmikroskopische Aufnahmen intakter Coronaviruspartikel in der Riechschleimhaut anzufertigen.
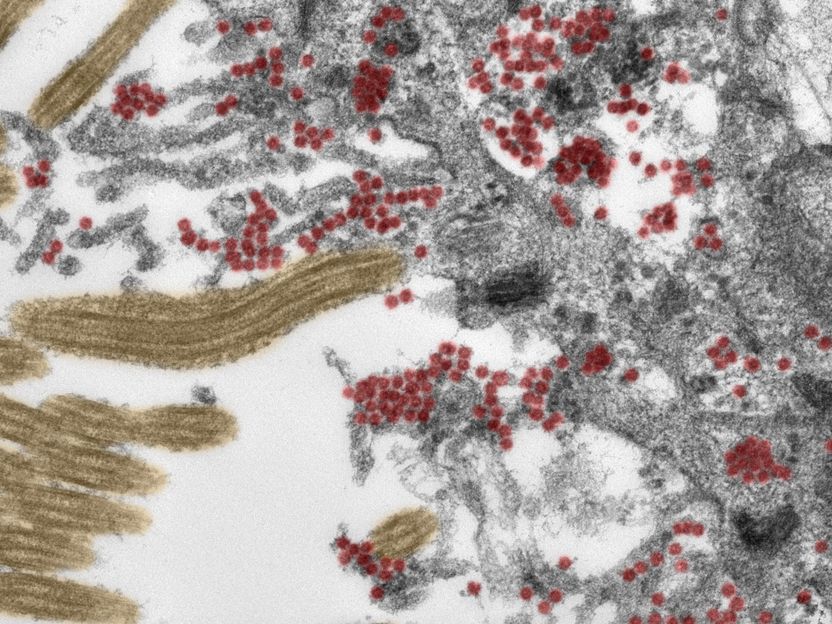
EM-Aufnahme (koloriert): Ausschnitt einer Zelle in der Riechschleimhaut. Sowohl innerhalb der Zelle als auch auf den Zellfortsätzen findet sich eine große Zahl intakter SARS-CoV-2-Partikel (rot). Gelb: Flimmerhärchen.
Michael Laue/RKI & Carsten Dittmayer/Charité
Dass COVID-19 nicht allein eine Atemwegserkrankung ist, gilt mittlerweile als gesichert. Nicht nur die Lunge, das Herz-Kreislauf-System oder den Magen-Darm-Trakt, sondern auch das zentrale Nervensystem kann SARS-CoV-2 beeinträchtigen: Mehr als ein Drittel der COVID-19-Betroffenen berichten über neurologische Symptome wie Geruchs- und Geschmacksverlust, Kopfschmerzen, Abgeschlagenheit, Schwindel und Übelkeit. Vereinzelt kommt es auch zu Schlaganfällen und anderen schwerwiegenden Erkrankungen. Forschende haben die Ursache dafür darin vermutet, dass das Virus in das Gehirn eindringt und dort bestimmte Zellen befällt. Doch wie gelangt SARS-CoV-2 dorthin? Unter Leitung von Dr. Helena Radbruch vom Institut für Neuropathologie der Charité und Prof. Dr. Frank Heppner, Direktor desselben Instituts, hat ein multidisziplinäres Forschungsteam den Eintritt des Virus in das Nervensystem und seinen weiteren Weg im Gehirn jetzt nachgezeichnet.
Dazu untersuchten Experten aus Neuropathologie, Pathologie, Rechtsmedizin, Virologie und der klinischen Versorgung die Gewebeproben von 33 Menschen, die an der Charité oder der Universitätsmedizin Göttingen infolge einer COVID-19-Infektion verstorben waren – im Schnitt in einem Alter von knapp 72 Jahren. Mit modernsten Methoden analysierten die Forschenden Proben aus der Riechschleimhaut sowie vier verschiedenen Hirnregionen: Sowohl im Gewebeverbund als auch in einzelnen Zellen fahndeten sie nach dem Erbgut von SARS-CoV-2 sowie einem Protein der Virushülle – dem sogenannten Spike-Protein. Dem Team gelang es so, das Virus in verschiedenen neuroanatomischen Strukturen nachzuweisen, die Auge, Mund und Nase mit dem Hirnstamm verbinden. Die höchste Viruslast zeigte sich dabei in der Riechschleimhaut. Dort konnte das Forschungsteam mithilfe von Spezialfärbungen und elektronenmikroskopischen Aufnahmen auch erstmals intakte Coronaviruspartikel sichtbar machen: Sie fanden sich sowohl im Inneren von Nervenzellen als auch auf den Fortsätzen der dort ansässigen Deckzellen. Für diese Analysen elementar war eine ausgezeichnete Gewebequalität, die die Forschungsgruppe durch eine enge Abstimmung zwischen krankenversorgenden und pathologischen Bereichen und eine ausgefeilte Infrastruktur erreichte.
„Auf Basis dieser Daten gehen wir davon aus, dass SARS-CoV-2 die Riechschleimhaut als Eintrittspforte ins Gehirn benutzen kann“, sagt Prof. Heppner. Das ist anatomisch auch naheliegend: Hier befinden sich Schleimhautzellen, Blutgefäße und Nervenzellen sehr nah beieinander. „Von der Riechschleimhaut aus nutzt das Virus offenbar neuroanatomische Verbindungen wie beispielsweise den Riechnerv, um das Gehirn zu erreichen“, ergänzt der Neuropathologe. „Wichtig zu betonen ist aber, dass die von uns untersuchten COVID-19-Betroffenen per Definition – sie gehören zu der kleinen Gruppe von Patientinnen und Patienten, die letztlich daran versterben – einen schweren Verlauf gezeigt hatten. Die Ergebnisse unserer Studie können deshalb nicht zwangsläufig auf leichte oder mittelschwere Fälle übertragen werden.“
Noch nicht abschließend geklärt ist, wie exakt das Virus sich von den Nervenzellen weiterbewegt. „Unsere Daten sprechen dafür, dass das Virus von Nervenzelle zu Nervenzelle wandert, um das Gehirn zu erreichen“, erklärt Dr. Radbruch. „Vermutlich wird das Virus aber gleichzeitig auch über das Blutgefäßsystem transportiert, da sich auch in den Gefäßwänden im Gehirn Virus nachweisen ließ.“ SARS-CoV-2 ist dabei nicht das einzige Virus, das über bestimmte Bahnen ins Gehirn gelangen kann. „Andere Beispiele hierfür sind Herpes-simplex-Viren und das Rabiesvirus, das Tollwut verursacht“, erklärt die Wissenschaftlerin.
Die Forschenden untersuchten außerdem, wie das Immunsystem auf den Befall mit SARS-CoV-2 reagiert: So wiesen sie aktivierte Immunzellen im Gehirn und in der Riechschleimhaut nach und entdeckten deren Immun-Signaturen im Hirnwasser. In einigen der untersuchten Fälle stellten sie auch Gewebeschädigungen durch Schlaganfälle fest, die als Folge von Thrombembolien, also Verstopfungen der Gefäße durch Blutpfröpfe, entstanden waren. „In unseren Augen liefert der SARS-CoV-2-Befall der Nervenzellen in der Riechschleimhaut eine gute Erklärung für die typischen neurologischen Symptome von COVID-19-Erkrankten, wie Geruchs- und Geschmacksstörungen“, erklärt Prof. Heppner. „Außerdem haben wir SARS-CoV-2 in Hirnregionen gefunden, die lebenswichtige Funktionen wie zum Beispiel die Atemtätigkeit steuern. Es ist nicht auszuschließen, dass bei schweren COVID-19-Verläufen der Virusbefall in diesen Hirnarealen die Atmung übergeordnet erschwert – zusätzlich zu der Beeinträchtigung der Atemfunktion durch den Virusbefall der Lungen. Ähnliches kann für Herz und Kreislauf gelten.“