Großer Schritt auf dem Weg zum sehnsüchtig erwarteten Wirkstoff gegen Corona
Biontech und Pfizer beantragen US-Zulassung: Produktion könnte sofort nach Genehmigung beginnen
(dpa) Das Mainzer Unternehmen Biontech und der US-Pharmariese Pfizer haben bei der US-Arzneimittelbehörde FDA eine Notfallzulassung für ihren Corona-Impfstoff beantragt. Das bestätigte Pfizer am Freitag bei Twitter. Anträge auf eine Zulassung für Europa und weitere Regionen seien in Vorbereitung, hatten die Firmen vorher mitgeteilt. «Wir können innerhalb von Stunden liefern, wenn wir eine Genehmigung erhalten sollten», sagte eine Sprecherin von Biontech in Mainz. Falls der Wirkstoff zugelassen werde, könnten besonders gefährdete Menschen in den USA Mitte bis Ende Dezember mit dem Impfstoff versorgt werden.
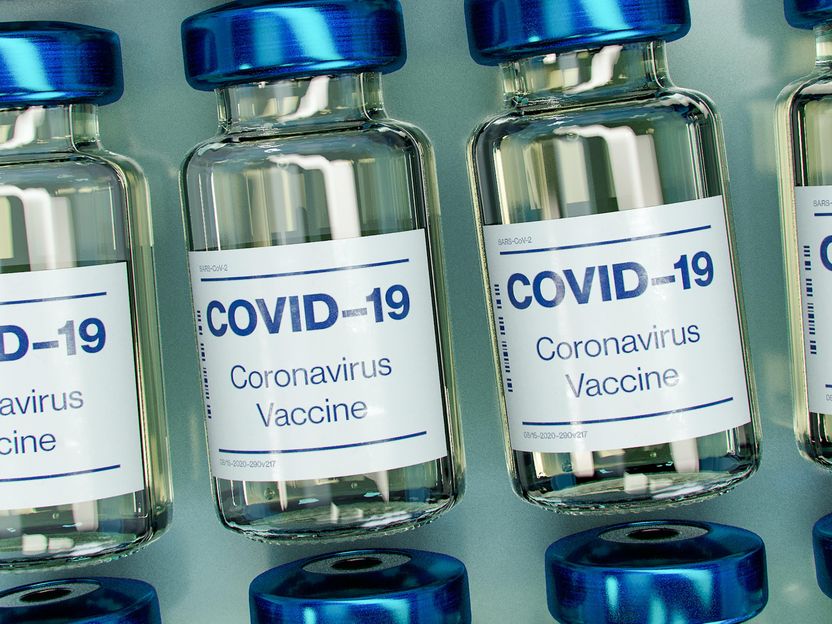
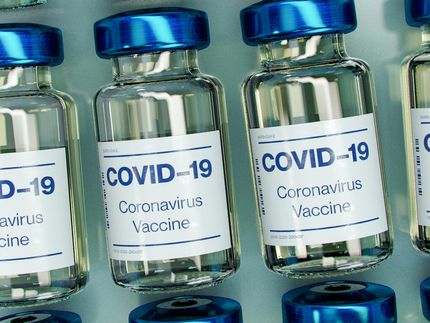
Symbolbild
Photo by Daniel Schludi on Unsplash
Biontech-Vorstandschef und Mitgründer Ugur Sahin sprach von einem «entscheidenden Schritt, um unseren Impfstoffkandidaten so schnell wie möglich der Weltbevölkerung zur Verfügung zu stellen». Ziel sei die schnelle globale Verteilung des Impfstoffs. «Als Unternehmen mit Sitz in Deutschland im Herzen Europas» sei der enge Kontakt mit der Europäischen Arzneimittel-Agentur (EMA) für Biontech von besonderer Bedeutung.
Biontech und Pfizer sind die ersten westlichen Hersteller, die vielversprechende Studienergebnisse veröffentlicht haben und den Weg für eine Notfallzulassung bei der FDA gehen. Für den Impfstoff mit der Bezeichnung BNT162b2 ergaben umfangreiche Testreihen nach Angaben der Unternehmen eine Wirksamkeit, die einen 95-prozentigen Schutz vor der Krankheit Covid-19 bietet. Das Vakzin funktioniere über alle Altersgruppen und andere demografische Unterschiede hinweg ähnlich gut und zeige praktisch keine ernsten Nebenwirkungen, hatten die Firmen nach Abschluss letzter Analysen mitgeteilt.
Die FDA muss den Antrag nach der Einreichung erst prüfen. Wie lange das dauern könnte, war zunächst unklar. US-Experten zeigten sich aber zuversichtlich, dass es noch vor Jahresende ein Ergebnis der Prüfung geben könnte. Für Corona-Impfstoffe gilt wegen der besonderen Dringlichkeit ein beschleunigter Zulassungsprozess.
Bei der Europäischen Arzneimittelbehörde (EMA) und in weiteren Ländern reichen Biontech und Pfizer bereits Daten ein. So können Hersteller schon vor dem formellen Zulassungsantrag Teilinformationen zu Qualität, Unbedenklichkeit und Wirksamkeit eines Präparats weitergeben. «Wir reichen kontinuierlich Daten ein im rollierenden Einreichungsprozess», antwortete die Biontech-Sprecherin auf die Frage nach den Vorbereitungen für Anträge zur Zulassung des Impfstoffs bei der EMA und in der Schweiz. Ziel sei es, mit diesen Daten einen Antrag auf Zulassung zu ermöglichen.
Bereits in der zweiten Dezemberhälfte könnte ein erster Impfstoff in Europa zugelassen werden, sagte EU-Kommissionschefin Ursula von der Leyen am Donnerstag unter Hinweis auf Informationen der EMA.
Eine wichtige Rolle bei der Produktion des Impfstoffs soll ein Werk in der hessischen Stadt Marburg spielen. Die Übernahme dieser Produktionsanlage vom Schweizer Pharmakonzern Novartis wurde laut Biontech im Oktober abgeschlossen.
Im Anschluss an die Fertigung sollen die Impfstoffdosen nach Unternehmensangaben «fair» verteilt werden. Es werde nicht «ein Land alles erhalten». Deutschland und die EU haben bereits einen Rahmenvertrag über den Kauf von 300 Millionen Dosen des Impfstoffs von Biontech und Pfizer abgeschlossen. Auf der Grundlage von Lieferprognosen geht Biontech davon aus, dass in diesem Jahr weltweit bis zu 50 Millionen Impfstoffdosen ausgeliefert und im nächsten Jahr bis zu 1,3 Milliarden Dosen hergestellt werden.
Biontech hatte bereits Mitte Januar angefangen, den Impfstoff BNT162b2 im Projekt «Lightspeed» (Lichtgeschwindigkeit) zu entwickeln. Die für eine Zulassung entscheidende Phase-3-Studie begann Ende Juli.
Das Präparat ist ein sogenannter mRNA-Impfstoff, der auf einem neuen Mechanismus basiert. Er enthält genetische Informationen des Erregers, aus denen der Körper ein Viruseiweiß herstellt - in diesem Fall das Oberflächenprotein, mit dessen Hilfe das Virus in Zellen eindringt. Ziel der Impfung ist es, den Körper zur Bildung von Antikörpern gegen dieses Protein anzuregen, um die Viren abzufangen, bevor sie in die Zellen eindringen und sich vermehren.
Ein Vorteil von mRNA-Impfstoffen ist, dass sie wesentlich schneller als konventionelle Impfstoffe produziert werden können. Der Impfstoff muss jedoch bei minus 70 Grad gelagert werden. Pfizer habe große Erfahrungen darin, Impfstoffe gekühlt zu lagern und zu transportieren und verfüge bereits über eine entsprechende weltweite Infrastruktur, teilten die Unternehmen mit.
Neben Biontech/Pfizer arbeiten derzeit auch mehrere andere Pharmafirmen in fortgeschrittenem Stadium an Corona-Impfstoffen, darunter Johnson&Johnson, Astrazeneca und Sanofi-GSK. In Russland, China und kürzlich erst in Bahrain wurden bereits Impfstoffe mit Einschränkungen freigegeben, dort haben die Impfungen begonnen. Wie gut diese Wirkstoffe tatsächlich schützen und welche Nebenwirkungen sie haben können, ist allerdings kaum bekannt.
Bundesgesundheitsminister Jens Spahn (CDU) hat kürzlich erklärt, er erwarte einen zügigen Zulassungsprozess. Zugleich kündigte er eine umfangreiche Informationskampagne zur Corona-Impfung an. Zuerst sollen Ältere, Menschen mit Vorerkrankungen, Ärzte und Pflegekräfte, Polizisten, Feuerwehrleute, Lehrer und Erzieher geimpft werden - entsprechend der Empfehlungen des Deutschen Ethikrats, der Wissenschaftsakademie Leopoldina und der Ständigen Impfkommission.
Der Mainzer Oberbürgermeister Michael Ebling (SPD) erklärte am Freitag, die Welt schaue in diesen Tagen voller Hoffnung auf Mainz. Neben der Entwicklung des Impfstoffs in den Mainzer Laboren von Biontech produziere der Mainzer Spezialglashersteller Schott die Pharmafläschchen für den Transport von Impfstoffen.