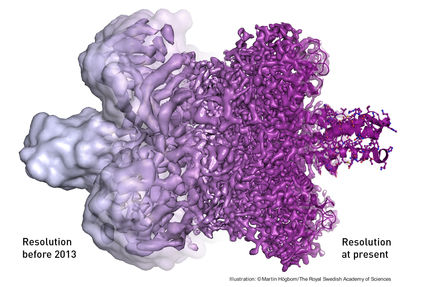
Neuer Algorithmus schärft den Blick der leistungsstärksten Mikroskope der Welt
Wissenschaftler entwickeln eine Technik, die die Auflösung der Kryo-Elektronenmikroskopie verbessert
Wir alle kennen den Moment in einer Polizeisendung im Fernsehen, in dem ein Detektiv körniges, niedrig aufgelöstes Sicherheitsmaterial durchsieht, eine Person von Interesse auf dem Band entdeckt und nonchalant einen CSI-Techniker bittet, "das zu verbessern". Ein paar Tastenklicks später, und voila - sie haben ein perfektes, klares Bild vom Gesicht des Verdächtigen. In der realen Welt funktioniert das natürlich nicht, wie viele Filmkritiker und Leute im Internet gerne betonen.
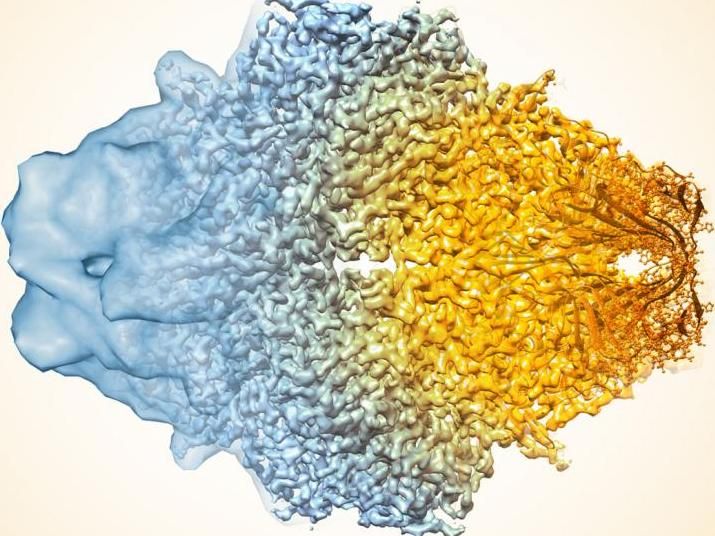
Ein zusammengesetztes Bild des Enzyms Laktase, das zeigt, wie sich die Auflösung der Kryo-EM in den letzten Jahren dramatisch verbessert hat. Ältere Bilder auf der linken Seite, neuere auf der rechten Seite.
Veronica Falconieri/National Cancer Institute
Wissenschaftler aus dem wirklichen Leben haben jedoch vor kurzem ein echtes "Enhancement-Tool" entwickelt: eines, das die Auflösung und Genauigkeit von leistungsstarken Mikroskopen verbessert, die dazu dienen, Einblicke in Biologie und Medizin zu gewähren.
In einer in Nature Methods veröffentlichten Studie zeigt ein multiinstitutionelles Team unter der Leitung von Tom Terwilliger vom New Mexico Consortium, dem Forscher des Lawrence Berkeley National Laboratory (Berkeley Lab) angehören, wie ein neuer Computeralgorithmus die Qualität der mit der Kryo-Elektronenmikroskopie (Kryo-EM) erstellten 3D-Molekularstrukturkarten verbessert.
Seit Jahrzehnten sind diese Kryo-EM-Karten, die durch die Aufnahme vieler Mikroskopiebilder und die Anwendung von Bildverarbeitungssoftware erzeugt werden, ein wichtiges Hilfsmittel für Forscher, die wissen wollen, wie die Moleküle in Tieren, Pflanzen, Mikroben und Viren funktionieren. Und in den letzten Jahren ist die Kryo-EM-Technologie so weit fortgeschritten, dass sie für viele Arten von Molekülen Strukturen mit atomarer Auflösung erzeugen kann. Doch in manchen Situationen erzeugen selbst die ausgeklügeltsten Kryo-EM-Methoden immer noch Karten mit geringerer Auflösung und größerer Unsicherheit, als es erforderlich ist, um die Details komplexer chemischer Reaktionen herauszukitzeln.
"In der Biologie gewinnen wir so viel, wenn wir die Struktur eines Moleküls kennen", sagte Paul Adams, Mitverfasser der Studie und Direktor der Abteilung Molekulare Biophysik und integrierte Bildgebung am Berkeley Lab. "Die Verbesserungen, die wir mit diesem Algorithmus sehen, werden es den Forschern erleichtern, aus den Daten der Elektronen-Kryo-Mikroskopie atomistische Strukturmodelle zu bestimmen. Dies ist besonders wichtig für die Modellierung sehr wichtiger biologischer Moleküle, wie z.B. derjenigen, die an der Transkription und Übersetzung des genetischen Codes beteiligt sind, die aufgrund ihrer großen und komplexen Multi-Unit-Strukturen oft nur in Karten mit niedrigerer Auflösung zu sehen sind.
Der Algorithmus schärft molekulare Karten, indem er die Daten auf der Grundlage des vorhandenen Wissens darüber filtert, wie Moleküle aussehen und wie Rauschen (unerwünschte und irrelevante Daten) in Mikroskopiedaten am besten abgeschätzt und entfernt werden kann. Ein Ansatz mit der gleichen theoretischen Grundlage wurde bereits früher zur Verbesserung von Strukturabbildungen aus der Röntgenkristallographie verwendet, und Wissenschaftler haben seine Verwendung in der Kryo-EM bereits früher vorgeschlagen. Doch laut Adams konnte bisher niemand definitiv nachweisen, dass es für die Kryo-EM funktioniert.
Das Team - bestehend aus Wissenschaftlern des Konsortiums von New Mexico, des Los Alamos National Laboratory, des Baylor College of Medicine, der Universität Cambridge und des Berkeley Labors - wandte den Algorithmus zunächst auf eine öffentlich zugängliche Karte des menschlichen Proteins Apoferritin an, von dem bekannt ist, dass es eine Auflösung von 3,1 Angström hat (ein Angström entspricht einem 10-Milliardstel eines Meters; als Referenz wird der Durchmesser eines Kohlenstoffatoms auf 2 Angström geschätzt). Dann verglichen sie ihre verbesserte Version mit einer anderen öffentlich zugänglichen Apoferritin-Referenzkarte mit einer Auflösung von 1,8 Angström und fanden eine verbesserte Korrelation zwischen den beiden.
Als nächstes wandte das Team seinen Ansatz auf 104 Kartendatensätze aus der Datenbank für Elektronenmikroskopie an. Bei einem großen Teil dieser Kartensätze verbesserte der Algorithmus die Korrelation zwischen der experimentellen Karte und der bekannten Atomstruktur und erhöhte die Sichtbarkeit von Details.
Die Autoren stellen fest, dass die klaren Vorteile des Algorithmus bei der Aufdeckung wichtiger Details in den Daten in Verbindung mit seiner Benutzerfreundlichkeit - es handelt sich um eine automatisierte Analyse, die auf einem Laptop-Prozessor durchgeführt werden kann - ihn wahrscheinlich zu einem Standardteil des fortschreitenden Kryo-EM-Workflows machen werden. Tatsächlich hat Adams den Quellcode des Algorithmus bereits der Phenix-Software-Suite hinzugefügt, einem beliebten Paket für die automatisierte Lösung makromolekularer Strukturen, für das er das Entwicklungsteam leitet.
Diese Forschung war Teil der kontinuierlichen Bemühungen von Berkeley Lab, die Fähigkeiten der Kryo-EM-Technologie zu verbessern und Pionierarbeit bei ihrer Verwendung für grundlegende wissenschaftliche Entdeckungen zu leisten. An vielen der bahnbrechenden Erfindungen, die die Entwicklung der Kryo-EM ermöglichten und sie später zu ihrer außergewöhnlichen aktuellen Auflösung führten, waren Wissenschaftler von Berkeley Lab beteiligt.
Hinweis: Dieser Artikel wurde mit einem Computersystem ohne menschlichen Eingriff übersetzt. LUMITOS bietet diese automatischen Übersetzungen an, um eine größere Bandbreite an aktuellen Nachrichten zu präsentieren. Da dieser Artikel mit automatischer Übersetzung übersetzt wurde, ist es möglich, dass er Fehler im Vokabular, in der Syntax oder in der Grammatik enthält. Den ursprünglichen Artikel in Englisch finden Sie hier.