Ein genetischer Nano-Baukasten für neue Biomaterialien
Magnetbakterien können zur Herstellung neuartiger Biomaterialien genutzt werden. Ein Team von Mikrobiologen an der Universität Bayreuth unter der Leitung von Prof. Dr. Dirk Schüler hat mit diesem Ziel erstmals ein Baukasten-System entwickelt, das die genetische Umprogrammierung der Bakterien ermöglicht. Die Bakterien werden dadurch zu Produzenten magnetischer Nanopartikel, die verschiedene nützliche Funktionen und Eigenschaften miteinander kombinieren. Erste Studien lassen auf eine gute Biokompatibilität der Partikel schließen. Das Anwendungspotenzial in der Biomedizin und Biotechnologie ist deshalb hoch.
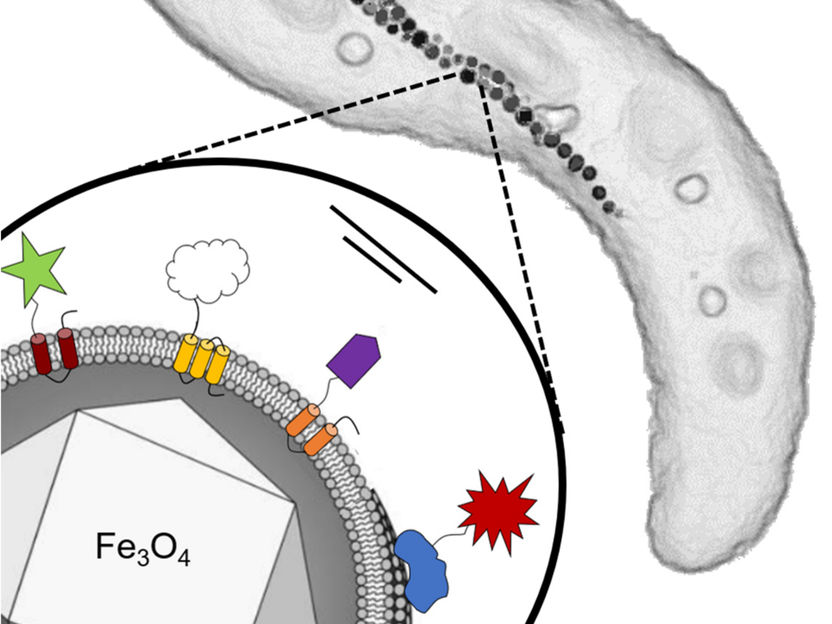
Zelle des magnetischen Bakteriums Magnetospyrillum gryphiswaldense mit verketteten Magnetosomen. Eine Zelle ist zwischen drei und fünf Mikrometern lang. Unten links: Einzelnes Magnetosom mit Eisenoxid-Kern und umgebender Membran. Auf spezifischen Proteinen der Membran werden genetisch verschiedene funktionelle Gruppen aus unterschiedlichen Fremdorganismen installiert.
Frank Mickoleit / Clarissa Lanzloth
Von Magnetosomen zu vielseitig nützlichen Nanopartikeln
Magnetbakterien der Spezies Magnetospirillum gryphiswaldense richten ihre Fortbewegungen am Erdmagnetfeld aus. In ihren Zellen sind magnetische Nanopartikel, die Magnetosomen, kettenförmig angeordnet und bilden damit eine Art Kompass-Nadel. Jedes Magnetosom besteht aus einem magnetischen Eisenoxid-Kern, welcher von einer Membran umgeben ist. Diese enthält neben Lipiden (Fetten) eine Vielzahl von Proteinen (Eiweißen).
Den Bayreuther Mikrobiologen ist es nun gelungen, an diese Proteine biochemisch aktive funktionelle Gruppen anzukoppeln, welche aus verschiedenen Fremdorganismen stammen. Das dabei angewendete Verfahren setzt bei den Genen an, die für die Biosynthese der Membran-Proteine zuständig sind. Diese Gene werden aus dem Genom (Erbgut) der Bakterien herausgelöst und mit Genen gekoppelt, welche die Herstellung der jeweiligen funktionellen Gruppen steuern. Sobald die Gene wieder in das Genom eingebaut sind, produzieren die umprogrammierten Bakterien Magnetosomen, auf deren Oberfläche diese Gruppen fest installiert sind.
Im Einzelnen wurden vier unterschiedliche funktionelle Gruppen mit Membran-Proteinen gekoppelt. Hierzu gehört das Enzym Glukose-Oxidase aus einem Schimmelpilz, das heute bereits als „Zuckersensor“ bei Diabetes-Erkrankungen biotechnologisch angewendet wird. Ebenso konnten ein grün-fluoreszierendes Protein aus einer Qualle sowie ein farbstoffbildendes Enzym aus dem Bakterium Escherichia coli, dessen Aktivität sich leicht messen lässt, auf der Oberfläche der Magnetosomen installiert werden. Die vierte funktionelle Gruppe stellt ein Antikörper-Fragment aus einem Lama dar.
„Mit dieser genetischen Umprogrammierung haben wir die Bakterien dazu gebracht, Magnetosomen zu produzieren, die bei einer Bestrahlung mit UV-Licht grün leuchten und zugleich biokatalytische Funktionen haben. Auf ihren Oberflächen können zielgenau verschiedene biochemische Funktionen installiert werden. So verwandeln sich Magnetosomen, die aus lebenden Bakterien stammen, in multifunktionale Nanopartikel mit faszinierenden Funktionen und Eigenschaften. Die Partikel bleiben unverändert, wenn man sie aus den Bakterien isoliert. Dies ist aufgrund ihrer herausragenden magnetischen Eigenschaften leicht möglich“, sagt Professor Dirk Schüler, der die Forschungsarbeiten koordiniert hat.
Ein genetischer Baukasten für Anwendungen in Biomedizin und Biotechnologie
Die Funktionen, mit denen die Magnetosomen von den Bayreuther Mikrobiologen ausgestattet wurden, sind nicht die einzigen, die auf der Membran installiert werden können. Sie können leicht durch andere Funktionen ersetzt werden. Das Verfahren der genetischen Umprogrammierung eröffnet daher ein weites Spektrum von Design-Möglichkeiten. Es stellt die Grundlage für einen „genetischen Baukasten" dar, der die Herstellung maßgeschneiderter Magnet-Nanopartikel erlaubt. Ganz unterschiedliche nützliche Funktionen und Eigenschaften lassen sich dabei kombinieren. Jeder dieser Partikel hat einen Durchmesser zwischen 30 und 50 Nanometern.
„Unser gentechnisches Verfahren zeichnet sich durch eine hohe Selektivität und Kontrollierbarkeit aus. Herkömmliche chemische Kopplungsmethoden sind dagegen längst nicht so leistungsfähig“, erklärt der Bayreuther Mikrobiologe Dr. Frank Mickoleit, der Erstautor der Studie. Er verweist auf einen entscheidenden Vorteil der neuen Biomaterialien: „Bisherige Studien zeigen, dass die Magnet-Nanopartikel in Zellkulturen keinen Schaden anrichten. Gute Biokompatibilität ist eine wichtige Voraussetzung, um die Partikel zukünftig in der Biomedizin anwenden zu können, etwa als Kontrastmittel in Bildgebungsverfahren oder als Sensoren in der Diagnostik. Die Partikel könnten so zum Beispiel helfen, Tumorzellen aufzuspüren und zu zerstören.“ Ein weiteres Anwendungsfeld sind Bioreaktorsysteme. Hierfür eignen sich Magnet-Nanopartikel, die mit winzigen Katalysatoren bestückt sind und komplexe biochemische Prozesse ermöglichen.
„Für die Kopplung verschiedener funktioneller Gruppen auf der Oberfläche von Nanopartikeln gibt es insbesondere in der Biotechnologie und auch in der Biomedizin ein enormes Anwendungspotenzial. Die Magnetbakterien sind die Plattform für einen faszinierenden Nano-Baukasten, der die wissenschaftliche Kreativität auf dem Gebiet der Synthetischen Biologie beflügelt. Er wird weitere interessante Forschungsansätze anstoßen“, ergänzt die Mikrobiologin Clarissa Lanzloth B.Sc., die als Mitautorin wesentlich an der neuen Studie beteiligt war und in Bayreuth den Masterstudiengang „Biochemie und Molekulare Biologie“ absolviert.
























































