Rezeptorkomplexe am Fließband
Zusammenbau von Glutamat-Rezeptoren und dessen Bedeutung für die Gedächtnisbildung entschlüsselt
Die schnelle Kommunikation von Nervenzellen im Gehirn hängt, ebenso wie die Fähigkeit zu lernen, fundamental von Neurotransmitter-Rezeptoren in den Kontaktstellen von Neuronen, den Synapsen, ab. Die wichtigsten Rezeptoren des Säugergehirns sind Glutamat-Rezeptoren des AMPA-Typs, die das zur Kommunikation notwendige elektrische Signal erzeugen. Ihre Anzahl wird durch den Grad der Aktivität einer Synapse moduliert: Beim Lernen erhöht sie sich, wodurch die Signalübertragung zuverlässiger funktioniert und die Synapse auf langdauernde Nutzung im Sinne von Gedächtnisbildung angelegt wird. Entscheidende Voraussetzung für diese synaptische Plastizität ist der effiziente Zusammenbau der AMPA-Rezeptoren aus verschiedenen Proteinuntereinheiten im endoplasmatischen Retikulum (ER) von Nervenzellen – ein Prozess, über den bislang wenig bekannt ist.
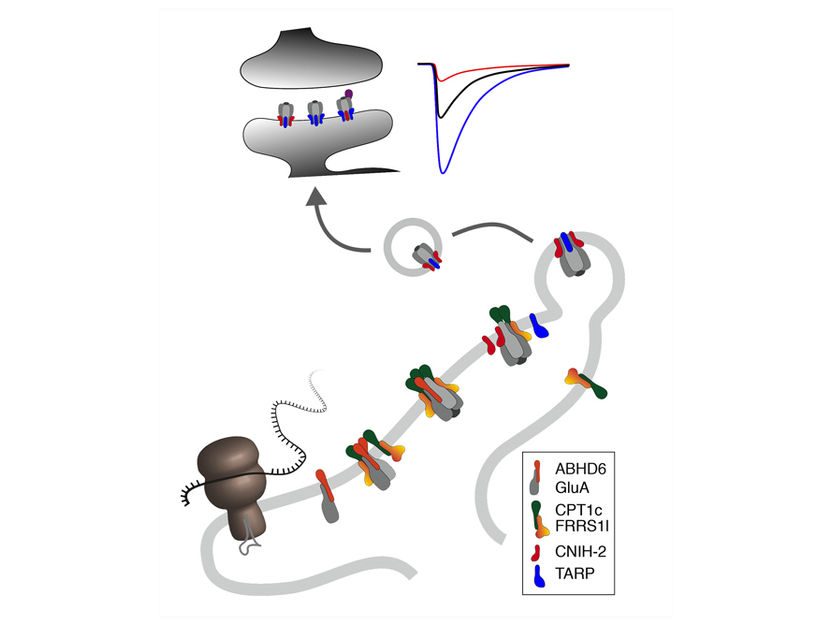
Der schrittweise, kontrollierte Zusammenbau von AMPA-Rezeptoren im endoplasmatischen Retikulum von Nervenzellen ist entscheidend für die Fähigkeit zum Lernen und zur Gedächtnisbildung.
Bernd Fakler
Freiburger Neurobiologen um Prof. Dr. Bernd Fakler vom Institut für Physiologie haben in Zusammenarbeit mit Kollegen der Universität Frankfurt und des Max-Planck-Instituts für medizinische Forschung in Heidelberg erstmals gezeigt, dass AMPA-Rezeptoren wie auf einem Fließband schrittweise aus Haupt- und Hilfsuntereinheiten zusammengesetzt werden. Die einzelnen Bauschritte werden von verschiedenen Proteinen und Proteinkomplexen des ER ausgeführt. Wird dieser Zusammenbau durch Mutationen in den Fließbandelementen beim Menschen oder durch deren gezielte genetische Inaktivierung – dem Knock-out – bei Mäusen gestört, kommt es zu massiven Einschränkungen in der synaptischen Signalübertragung sowie der Fähigkeit zu lernen. Umgekehrt führt die Steigerung der Rezeptorherstellung durch Überproduktion der Fließbandproteine zu erhöhter Plastizität der Synapsen. Diese Ergebnisse haben die Wissenschaftler in der Fachzeitschrift Neuron veröffentlicht.
Unter Anwendung hochauflösender Proteomanalyse-Techniken haben die Forscher Proteine in den ER-Membranen von Neuronen identifiziert, die für den Zusammenbau funktionsfähiger AMPA-Rezeptoren aus vier porenbildenden Untereinheiten und vier Hilfsuntereinheiten notwendig sind: Der erste Baustein, die Proteine ABHD6 und PORCN, schützt die einzelnen porenbildenden Untereinheiten vor vorzeitigem Abbau. Der zweite Baustein, ein Komplex aus den Proteinen FRRS1l und CPT1c, fügt vier dieser Einzelbausteine zu einem Rezeptor-Kanal zusammen und bereitet die Bindung der vier Hilfsuntereinheiten, der Cornichon- oder TARP-Proteine, vor. Dieser letzte Arbeitsschritt löst dann den FRRS1l-CPT1c Komplex ab und ermöglicht so den Export der funktionsfähigen AMPA-Rezeptoren aus dem ER und ihren Transport in die Synapsen.
Die einzelnen Arbeitsschritte dieses Fließbands sind exakt aufeinander abgestimmt und auf den effizienten Zusammenbau der Rezeptoren hin optimiert. Wird die Fließbandarbeit gestört, etwa durch mutationsbedingten Funktionsverlust des FRRS1l-Proteins, führt dies beim Menschen zu schwersten Funktionsstörungen des Gehirns, was die Forscher schon in einer 2017 publizierten Arbeit beschrieben haben: Alle Patienten zeigten stark eingeschränkte intellektuelle Fähigkeiten und Intelligenzquotienten unter 40, verzögerte oder fehlende Sprachentwicklung sowie eine erhöhte Neigung zu epileptischen Anfällen.
Das entschlüsselte Fließband ist zwar auf AMPA-Rezeptoren spezialisiert, doch die Forscher vermuten, dass der Prozess der schrittweisen Fertigung beispielgebend ist für andere Membranproteine und -proteinkomplexe, die an der Informationsverarbeitung im Gehirn oder der Erregungsausbreitung sowie am Stofftransport in anderen Zellen beteiligt sind.
Originalveröffentlichung
Schwenk, S. Boudkkazi, M. Kocylowski, A. Brechet, G. Zolles, T. Bus, K. Costa, W. Bildl, A. Kollewe, J. Jordan, J. Bank, W. Bildl, R. Sprengel, A. Kulik, J. Roeper, U. Schulte, and B. Fakler: "An ER assembly line of AMPA-receptors controls excitatory neurotransmission and its plasticity"; Neuron; 2019
Meistgelesene News
Originalveröffentlichung
Schwenk, S. Boudkkazi, M. Kocylowski, A. Brechet, G. Zolles, T. Bus, K. Costa, W. Bildl, A. Kollewe, J. Jordan, J. Bank, W. Bildl, R. Sprengel, A. Kulik, J. Roeper, U. Schulte, and B. Fakler: "An ER assembly line of AMPA-receptors controls excitatory neurotransmission and its plasticity"; Neuron; 2019
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte
COMET_(Studie)
Genveränderte Hefe kann Opiate aus Zucker produzieren - Morphin, Codein und andere Substanzen aus Schlafmohn lassen sich bald aus Mikroorganismen gewinnen
Kardiale_Resynchronisationstherapie
ACTIVE_W
Arthrose: Zuckerbindendes Protein kurbelt die Entzündung an
Liste_sequenzierter_Organismen
Biophoton
Neue Zielstruktur gegen Corona entdeckt - Völlig unerwartet zeigt sich das Enzym Ceramidase als neue Zielstruktur für die Therapie von SARS-CoV-2-Infektionen
Präkordialer_Faustschlag
Visuelle_Analogskala