Sensoren aus bioinspirierten Nanoporen
Interdisziplinäres Team ermöglicht gezielten Substanznachweis
Mediziner und Umweltanalytiker wünschen sich Mikrochips, die Substanzen direkt vor Ort messen. Wissenschaftler der TU Darmstadt haben ein auf Nanoporen basiertes System mit breitem Potential entwickelt und patentiert.

Professor Wolfgang Ensinger und Ivana Duznovic begutachten ihr hochsensibles Produkt: einen Chip mit Sensoren aus synthetischen Nanoporen.
Katrin Binner
Wer heute Laborwerte zur Diagnostik einer Erkrankung oder deren Verlaufskontrolle nutzen will oder die Belastung von Abwässern mit Pflanzenschutzmitteln oder Medikamenten testen möchte, muss die Proben fast immer ins Labor schicken und auf die Ergebnisse warten. Das kostet Zeit. Ein „Lab-on-a-Chip-System“ bestimmt die Werte noch während des Besuchs beim Arzt oder am Probenort.
Checkkartengroß und mit der Funktionalität eines Labors arbeiten diese Systeme schneller, kostengünstiger und mit weniger Aufwand als ein klassisches Labor, allerdings müssen sie auch genauso präzise, robust und zuverlässig sein. Die Forschungsgruppen von Wolfgang Ensinger, Professor für Materialwissenschaften, und Helmut Schlaak, Professor für Elektrotechnik und Informationstechnik an der TU Darmstadt, haben im Rahmen des LOEWE-Schwerpunkts iNAPO einen Prototyp für ein „Lab-on-a-Chip-System“ entwickelt, das Substanzen mit Sensoren aus synthetischen Nanoporen erfasst. An dem Projekt beteiligt sind die Chemikerin Ivana Duznovic und der Elektrotechniker Mario El Khoury.
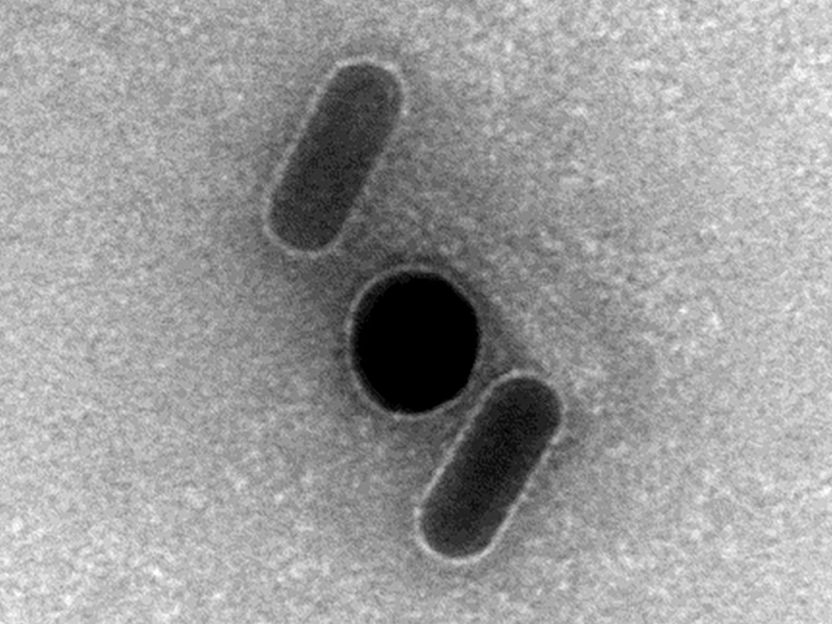
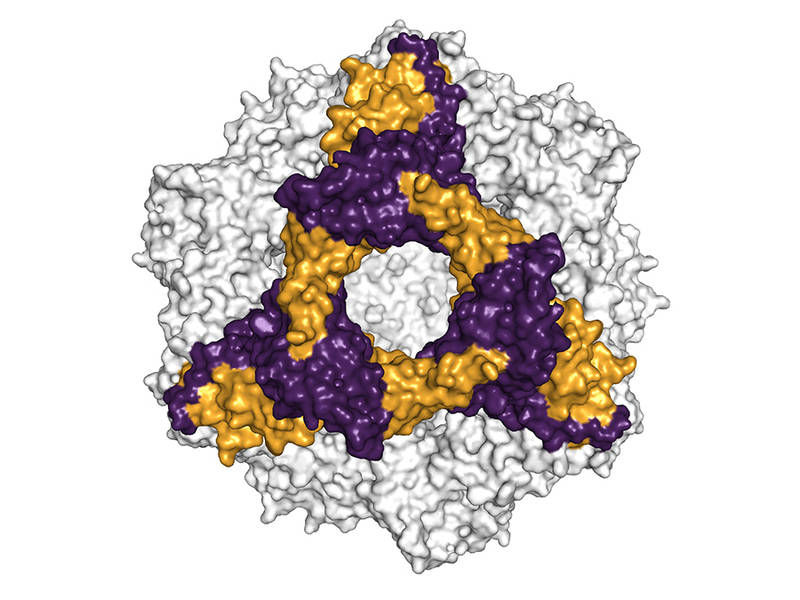
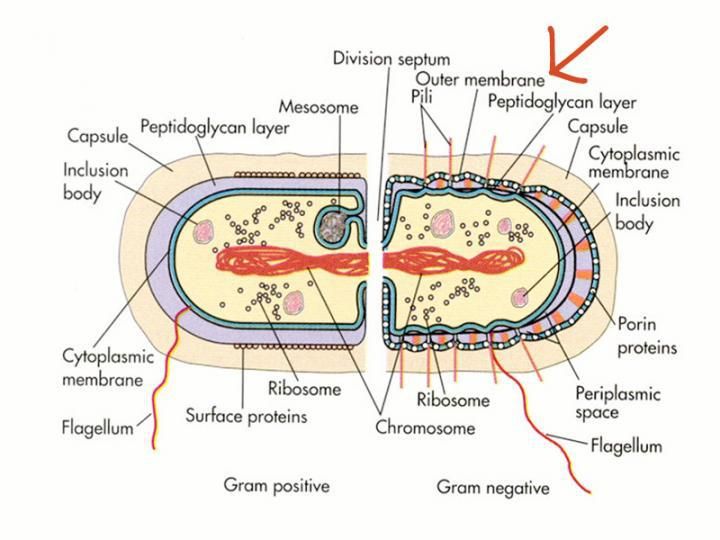
Inspiriert wurden die Wissenschaftler dabei von der Natur. In die Zellmembranen integriert, sorgen biologische Nanoporen dafür, dass Substanzen von außen nach innen oder von innen nach außen transportiert werden. Sie funktionieren dabei entweder als Schleusen oder als selektive Transportsysteme, die auf bestimmte Substanzen spezialisiert sind. Es gibt bisher kein technisches System, das es mit der Sensitivität und Spezifität der biologischen Nanoporen aufnehmen kann. Ihre Leistungsfähigkeit ist unerreicht. Biologische Nanoporen selbst sind allerdings für eine technische Anwendung ungeeignet, weil sie zu fragil sind. Ensinger und Duznovic setzen daher auf synthetische Nanoporen, die sie mit einem chemischen oder biologischen Sensor ausstatten.
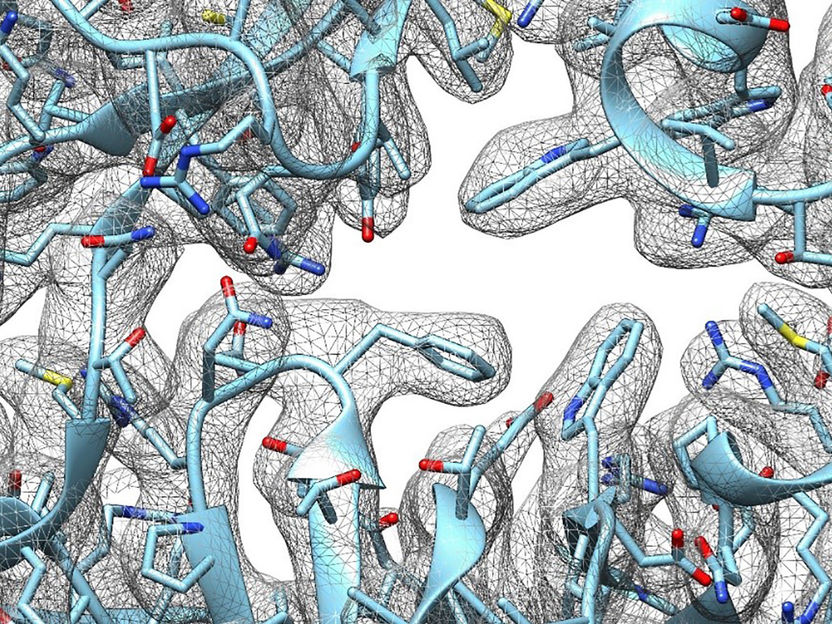
Dafür werden die Oberflächen der Nanoporen entsprechend funktionalisiert. „Unser Ziel ist es, eine neue Generation von Sensoren zu entwickeln, die in enger Anlehnung an ihre biologischen Vorbilder eine hohe Empfindlichkeit und Leistungsfähigkeit besitzen“, sagt Ensinger. „Wenn wir diese bioinspirierten Sensoren dann in ein mikrofluidisches System mit einer tragbaren Auswertelektronik integrieren, wird daraus ein Lab-on-a-Chip-System“, ergänzt Schlaak.
Dafür sind allerdings mehrere Schritte notwendig. Zuerst müssen die synthetischen Nanoporen hergestellt werden. Das geschieht durch den Beschuss von Polymer-Folien mit Schwerionen. Diese Aufgabe übernimmt das GSI Helmholtz-Zentrum für Schwerionenforschung in Darmstadt. Nach dem Beschuss der Folien werden die Nanoporen vergrößert und in eine konische Form gebracht. Sie haben dann eine enge und eine weite Öffnung und sehen aus wie ein Trichter. Vergrößert werden die Nanoporen, indem die Folie von einer Seite mit Lauge behandelt wird. „Durch den Ätzvorgang entstehen freie Carboxygruppen, über die wir die Nanoporen dann durch Koppelungschemie funktionalisieren können“, erklärt Ivana Duznovic. „Wir können im Grunde alles Mögliche an die Carboxygruppen anhängen.
Allerdings sind nur Substanzen sinnvoll, die biologisch oder chemisch relevant sind und mit deren Hilfe wir die für Diagnose oder Umweltanalytik relevanten Biomoleküle mit hoher Spezifität und Sensitivität nachweisen können. Sonst würde der Sensor keinen Sinn machen.“
Funktionalisiert wurden die Nanoporen unter anderem für den Nachweis von Histamin. Histamin spielt eine zentrale Rolle bei den allergischen Reaktionen und könnte auch bei der Alzheimer-Demenz wichtig sein. Der Nachweis, den Ensinger und Duznovic konzipiert haben, basiert auf einer Verdrängungsreaktion. Eine an die Carboxygruppe gekoppelte Substanz bindet ein Metallion, das auch an Histamin binden kann. Enthält die Probe Histamin, wechselt das Metallion zum Histamin über, was an einem Stromabfall in den Nanoporen zu erkennen ist. Dabei gilt: Je stärker der Strom abfällt, desto mehr Histamin ist in der Probe enthalten. Weil die an die Carboxygruppe gekoppelte Substanz wieder mit dem Metallion beladen werden kann, sind die Nanoporen regenerierbar und können für einen weiteren Nachweis verwendet werden.
Der nächste Schritt ist die Entwicklung des „Lab-on-a-Chip-Systems“. „Wir haben schon einen funktionierenden Mikrochip, allerdings sind noch einige Probleme zu lösen, weil der Nachweis nicht nur in wässriger Lösung funktionieren soll, sondern auch in einer Blutprobe“, sagt Schlaak. Da das Team den Chip aus Kostengründen auch gerne wiederverwerten möchten und dies wegen der Regenerierbarkeit der Nanoporen auch grundsätzlich möglich ist, sollte es zudem bei späteren Ergebnissen keine Verfälschungen durch die Erstverwendung geben. „Wir dürfen keine sogenannten Memory-Effekte haben“, bringt El Khoury das Problem auf den Punkt.
Ein Nadelöhr für die Kommerzialisierung ist auch die Suche nach einem geeigneten Kandidaten für einen entsprechenden Nachweis, etwa für die Medizin. „Wir brauchen einen Marker, der schon entsprechend validiert worden ist“, sagt Ensinger. „Es muss sicher sein, dass der Nachweis tatsächlich medizinisch sinnvoll und hilfreich ist, etwa für die Diagnostik, das Screening oder die Verlaufskontrolle einer Erkrankung“, so der Materialwissenschaftler weiter. „Wir sind derzeit noch auf der Suche nach interessanten Kandidaten und kollaborieren bereits mit der Universitätsklinik in Mainz. Allerdings sind wir offen für weitere Ideen.“
Ein auf bioinspirierten Nanoporen basiertes „Lab.on-a-Chip-System“ lässt sich nur in enger Zusammenarbeit mit anderen Disziplinen erarbeiten. Ensinger und Schlaak loben daher auch das interdisziplinäre Vorgehen im Rahmen des LOEWESchwerpunkts iNAPO. An der Entwicklung waren Chemiker, Biologen, Materialwissenschaftler, Physiker und Elektrotechniker beteiligt. „Wir sind an der TU Darmstadt für derartige Projekte sehr gut aufgestellt“, sagt Ensinger. Als nächstes möchte das Team die Oberflächen der Nanoproben für den Nachweis von Proteinen ausrüsten, um damit auch komplexe Biomarker nachzuweisen.
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Diagnostik
Die Diagnostik ist das Herzstück der modernen Medizin und bildet in der Biotech- und Pharmabranche eine entscheidende Schnittstelle zwischen Forschung und Patientenversorgung. Sie ermöglicht nicht nur die frühzeitige Erkennung und Überwachung von Krankheiten, sondern spielt auch eine zentrale Rolle bei der individualisierten Medizin, indem sie gezielte Therapien basierend auf der genetischen und molekularen Signatur eines Individuums ermöglicht.

Themenwelt Diagnostik
Die Diagnostik ist das Herzstück der modernen Medizin und bildet in der Biotech- und Pharmabranche eine entscheidende Schnittstelle zwischen Forschung und Patientenversorgung. Sie ermöglicht nicht nur die frühzeitige Erkennung und Überwachung von Krankheiten, sondern spielt auch eine zentrale Rolle bei der individualisierten Medizin, indem sie gezielte Therapien basierend auf der genetischen und molekularen Signatur eines Individuums ermöglicht.