Wie Licht Gehirnaktivitäten anstoßen kann
Bochumer und Berliner Forscher haben im Detail aufgeklärt, wie sich ein Ionenkanal nach Lichteinwirkung öffnet – ein Meilenstein für das Verständnis optogenetischer Werkzeuge.

Max Dreier, Klaus Gerwert und Stefan Tenningkeit (von links) betrachten die Darstellung eines Proteins.
© RUB, Kramer
Die Optogenetik erlaubt es, Gehirnprozesse mit Licht zu steuern. Sie beruht auf der Nutzung lichtgesteuerter Proteine wie dem Channelrhodopsin-2, einem Ionenkanal, der sich bei Lichteinwirkung öffnet und damit zelluläre Prozesse aktivieren kann. Seine Arbeitsweise haben Forscher der Ruhr-Universität Bochum (RUB) gemeinsam mit Kollegen von der Humboldt-Universität zu Berlin nun im Detail aufgeklärt. Das Team um Prof. Dr. Klaus Gerwert und Prof. Dr. Peter Hegemann berichtet in der Fachzeitschrift PNAS vom 19. April 2019.
Großes therapeutisches Potenzial
In der Optogenetik sehen Forscher ein großes therapeutisches Potenzial. „Man kann sich vorstellen, dass Blinde damit wieder sehen könnten, oder dass es gelingt, die Schüttellähmung bei Parkinson mittels Licht zu behandeln“, erklärt Klaus Gerwert.
Das von Peter Hegemann entdeckte Channelrhodopsin-2 ist das zentrale lichtaktivierbare Protein in der Optogenetik. Stattet man Nervenzellen mit diesem Ionenkanal aus, kann man die Kanäle durch Lichteinstrahlung öffnen und damit Gehirnaktivitäten gezielt steuern.
Allerdings gab es bislang widersprüchliche Vorstellungen davon, wie sich der Kanal im Detail öffnet. „Aber gerade das Verständnis der molekularen Reaktionen im Protein und der resultierenden Ionenleitung ist essenziell, um das Protein für seine möglichen Anwendungen gezielt zu optimieren“, sagt Gerwert.
Zwei parallele Wege
Gemeinsam konnten die Bochumer und Berliner Forscher die Details der Kanalöffnung nun enträtseln. Die Kombination von zeitaufgelöster Fourier-Transform-Infrarot-Spektroskopie, biomolekularen Simulationen und elektrophysiologischen Experimenten zeigte, dass durch Lichtanregung nicht nur wie bisher angenommen eine, sondern zwei unterschiedliche Strukturen angeregt werden. Eine führt dabei zu der gewünschten Kanalöffnung, die in der Optogenetik genutzt wird. Der parallele Weg liefert nur einen schwachen Protonenstrom, gewinnt aber bei längerer Belichtung die Oberhand und unterdrückt die gewünschte Kanalöffnung. Dadurch nimmt die Effektivität des optogenetischen Werkzeugs nach kurzer Zeit stark ab. „Wenn wir den unerwünschten Parallelweg durch gezieltes Proteindesign blockieren, können wir das optogenetische Werkzeug also entscheidend verbessern“, folgert Gerwert.
Bei der Arbeit am Channelrhodopsin profitierten die Bochumer Forscher von ihren umfangreichen Erfahrungen mit dem Mechanismus der lichtgetriebenen Protonenpumpe Bakteriorhodopsin, den sie vor Jahren im Detail aufklärten konnten. „Wie beim Bakteriorhodopsin spielen proteingebundene Wassermoleküle eine zentrale Rolle für die Protonenleitung“, erklärt Klaus Gerwert.
Originalveröffentlichung
Jens Kuhne, Johannes Vierock, Stefan Alexander Tennigkeit, Max-Aylmer Dreier, Jonas Wietek, Dennis Petersen, Konstantin Gavriljuk, Samir F. El-Mashtoly, Peter Hegemann, Klaus Gerwert; "Unifying photocycle model for light adaptation and temporal evolution of cation conductance in channelrhodopsin-2"; PNAS; 2019
Meistgelesene News
Originalveröffentlichung
Jens Kuhne, Johannes Vierock, Stefan Alexander Tennigkeit, Max-Aylmer Dreier, Jonas Wietek, Dennis Petersen, Konstantin Gavriljuk, Samir F. El-Mashtoly, Peter Hegemann, Klaus Gerwert; "Unifying photocycle model for light adaptation and temporal evolution of cation conductance in channelrhodopsin-2"; PNAS; 2019
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte
Bayerische Patentallianz GmbH verhandelt Patentübertragungsvertrag mit SEQUENOM, Inc. - SEQUENOM erhält Patent für DNA-Methylierungsanalyse-Technologie

Materialforschung auf dem Holzweg - Grüne Alternativen zu fossilen Rohstoffen: Biobasierte Materialien sollen Umweltverschmutzung reduzieren und den Wandel zu einer nachhaltigeren Wirtschaft vorantreiben

Licht an – Licht aus: Das Testergebnis ist da - Von der Natur abgeschaut - Lichtgesteuerte biobasierte OptoAssays können Krankheiten leicht und günstig diagnostizieren
Fine-Tuning für die Abwehrzellen im Darm
Molzym ist Teil von Gradian Diagnostics
Bayer übernimmt Biotech-Start-up - Bayer treibt Stammzelltherapie voran
Bayer kommt bei Prostatakrebs-Medikament Darolutamid voran
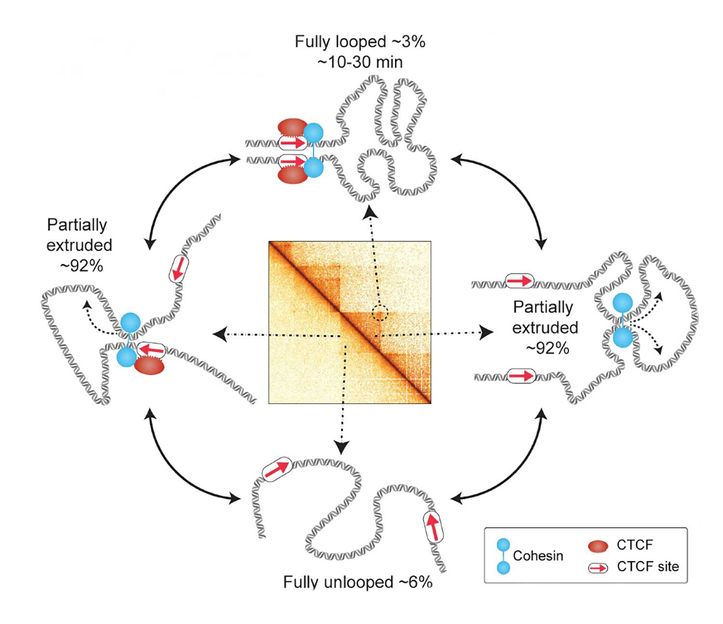
Erstaunlich kurze Lebensdauer von vermeintlichen Schlüsselstrukturen in der Genexpression - Genomschlaufen in Zellen überleben nicht lange: Theorien, wie diese Schlaufen Genexpression steuern, müssen möglicherweise neu überdacht werden
Bifidobacterium
Glückshormon Dopamin steuert Immunabwehr - Forscher simulieren Mechanismus der Kommunikation in Infektionsprozessen




















































