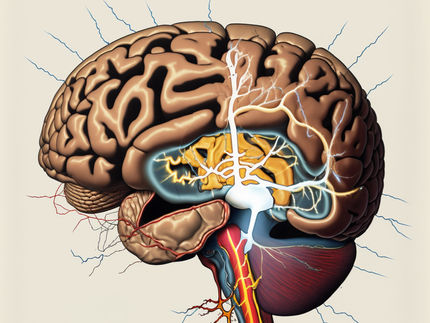
Wichtige Fette für wachsende Nerven
Forscher bestimmen Rolle von Sphingolipiden bei Gehirnentwicklung
Eine genetisch-bedingte Störung in der Bildung von Fetten – sogenannten Sphingolipiden –, einer wichtigen Komponente von Zellmembranen, führt beim Menschen zur neuronalen Degeneration im Nervensystem. Wie diese die Entwicklung und Funktion von Nervenzellen unterstützen ist bisher wenig verstanden. Wissenschafter vom Department für Neurobiologie der Universität Wien haben nun gezeigt, dass Sphingolipide bei der Sortierung von Proteinen in wachsenden Nervenzellen entscheidend sind.
Symbolbild
geralt, pixabay.com, CC0
Nervenzellen zeigen eine auffällige Polarisierung in ihrer Struktur und Funktion. An weitverzweigten Dendriten wird Information von benachbarten Nervenzellen aufgenommen und durch ein langes Axon an entfernte Neurone weitergegeben. Hierfür müssen Rezeptoren und Signalmoleküle gezielt in die beiden Kontaktstellen der Nervenzellen transportiert werden. Wie Nervenzellen diese Transportprozesse regulieren, insbesondere während der Verschaltung von Nervenzellen bei der Gehirnentwicklung, ist noch weitgehend unbekannt.
Um die molekularen Mechanismen der neuronalen Verschaltung besser zu verstehen nutzt das Team um Neurobiologen Thomas Hummel die Taufliege Drosophila als experimentelles Modellsystem. Obwohl mit ihren 100.000 Nervenzellen weit weniger komplex als das menschliche Gehirn, sind in Drosophila die Mehrzahl der neuronalen Entwicklungsprozesse und genetischen Regulatoren verwandt mit jenen des Menschen. Die Forscher konnten nun eine Drosophila Mutante mit spezifischen Verschaltungsdefekten identifizieren, bei der die Funktion des Gens SPT gestört ist. SPT ist für die Bildung von Sphingolipiden essentiell, eine besondere Klasse von lang-kettigen Fettmolekülen, die in der Zellmembran angereichert sind und dort die Lokalisation von Proteinen bestimmen. Beim Menschen führt der gleiche Gendefekt zu vielseitigen neuro-pathologischen und -degenerativen Symptomen im Nervensystem (HSAN Typ1).
Mit Hilfe der in Drosophila verfügbaren genetischen Analysetechniken konnten die Forscher zeigen, dass besonders das Zellmembranmolekül Dscam bei reduzierten Sphingolipiden nicht mehr korrekt zu den Dendriten und Axonen von wachsenden Nervenzellen transportiert wird und dadurch eine Fehlverschaltung in den neuronalen Netzwerke verursacht.
Besonders überraschend war die Beobachtung, dass diese fehlverteilten Dscam Moleküle in den erwachsenen Drosophila Gehirnen große Proteinaggregate bilden, die sich an den Kontaktstellen der Nervenzellen anreichern und den Informationsfluss beeinträchtigen. Interessanterweise finden sich im Fliegengehirn die gleichen toxischen Proteinaggregate, wenn die HSAN Typ1 Mutationen aus dem Menschen in Drosophila induziert werden. In weiterführenden Studien lässt sich dieses Drosophilamodell nun vielseitig nutzen, nicht nur um den genauen Verlauf der neuronalen Erkrankung besser zu verstehen sondern auch wirksame Substanzen zu identifizieren, die eine Bildung der Proteinaggregate in Nervenzellen verhindern.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.