Entwicklung von Wirkstoffen gegen Parkinson
LCSB und Ksilink beschreiten gemeinsam neue Wege
Am Freitag haben Vertreter der Universität Luxemburg und des Technologieunternehmens Ksilink, das neuartige, patientenbasierte Therapieformen entwickelt, ein Abkommen unterschrieben. Die Vereinbarung bildet den Rahmen für die Zusammenarbeit von Ksilink mit dem Luxembourg Centre for Systems Biomedicine (LCSB) der Universität Luxemburg zur Entwicklung von Wirkstoffen gegen die Parkinson-Krankheit.
Etwa sieben Millionen Menschen weltweit sind an Parkinson erkrankt – Tendenz steigend. Zwar können Mediziner mittlerweile die Symptome der Krankheit, bei der Nervenzellen im Gehirn absterben, recht gut behandeln. Eine Therapie, die die Ursachen der Krankheit beseitigt, gibt es bislang nicht. Das LCSB und das in Straßburg ansässige privat-öffentliche Technologieunternehmen Ksilink kooperieren ab sofort, um dieses Problem anzugehen: Gemeinsam wollen sie neuartige, patienten-basierte Zellkulturmodelle entwickeln, auf denen automatisiert und unter Einsatz von Künstlicher Intelligenz (KI) Wirkstoffkandidaten aus einer großen Substanz-Bibliothek getestet werden sollen. Mit einer Laufzeit von fünf Jahren und einem Investitionsvolumen von mehr als acht Millionen Euro bildet das Vorhaben eine bedeutende Public-Private-Partnerschaft. Teil dieses Budgets wird über das BRIDGES-Programm des Fonds National de la Recherche (FNR) finanziert. „Das unterstreicht das Potenzial, das Ksilink in unserer klinisch-wissenschaftlichen Expertise sieht“, sagt Prof. Dr. Rejko Krüger, Leiter der Clinical & Experimental Neuroscience Gruppe am LCSB. Auch Dr. Mona Boye, Business Developer bei Ksilink, bestätigt: „Die patienten-basierten Zellkulturen und die klinische Kompetenz vom LCSB gepaart mit unserem Knowhow für phänotypische Drug Discovery und industrienaher Wirkstoffentwicklung bieten die Chance, in der Therapieentwicklung für Parkinson wirklich einen Durchbruch zu erzielen.“
Die Parkinson-Krankheit hat viele Ursachen. Unter anderem können Genveränderungen die Auslöser sein. Solche Mutationen stehen im Fokus der Forscher von LCSB und Ksilink, wie Rejko Krüger erläutert: „Unsere Patienten-Kohorte, im Rahmen des National Centre for Parkinson’s Disease (NCER-PD), bietet uns am LCSB Zugang zu Gewebeproben von Parkinsonpatienten und gesunden Studienteilnehmern. Dank neuartiger Labormethoden mit einer Robotik für Hochdurchsatzanalysen von Patienten-Zellkulturen, die wir in den vergangenen Jahren mit finanzieller Unterstützung durch den FNR entwickelt haben, lassen sich an diesen Proben jetzt Untersuchungen durchführen, die sehr zielgerichtet Hinweise auf mögliche Wirkstoffe gegen Parkinson geben können.“
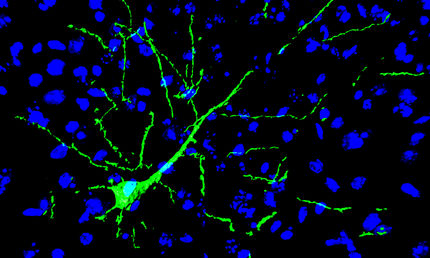
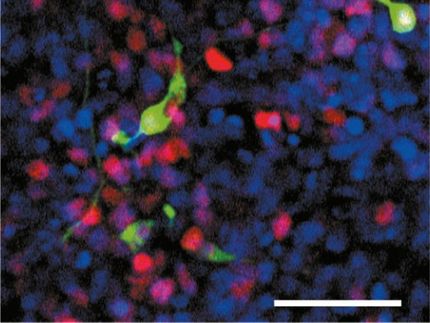
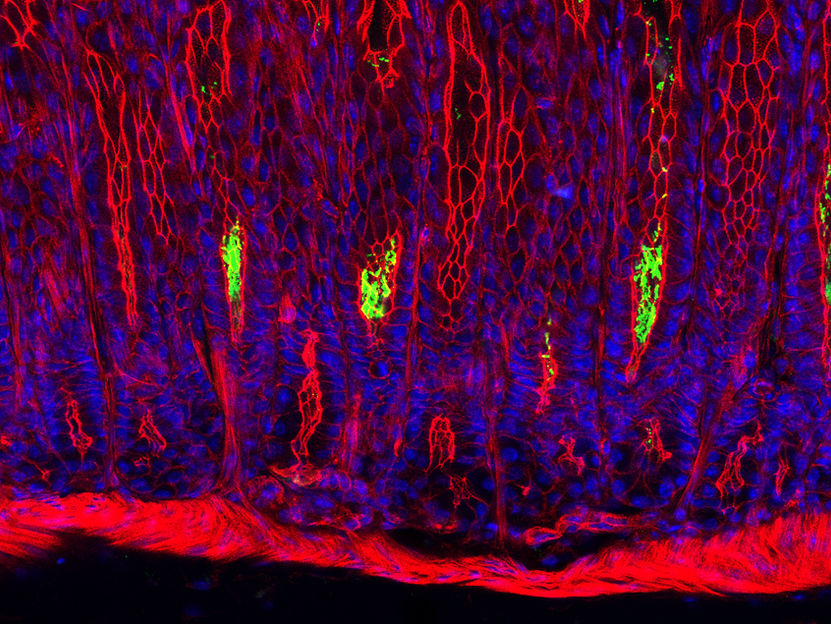
Dazu werden die Zellen aus den Gewebeproben zunächst im Labor in so genannte pluripotente Stammzellen umgewandelt. Aus ihnen können die Forscher dann genau den Zelltyp gewinnen, der von der Parkinson-Krankheit hauptsächlich betroffen und der in diesem Zusammenhang von Bedeutung ist: so genannte dopaminerge Nervenzellen, die ganz spezifische Mutationen im Erbmaterial aufweisen. „Wir haben am LCSB in Zusammenarbeit mit der Developmental & Cellular Biology Gruppe von Prof. Jens Schwamborn in den vergangenen Jahren die Spezial-Expertise aufgebaut, die für die Entwicklung solch spezifischer Parkinson-Zellmodelle erforderlich ist“, so Krüger.
Die von Patienten stammenden Zellkulturen werden dann in großer Zahl unter hochauflösenden Mikroskopen von Ksilink betrachtet. Zellkulturen gesunder Angehöriger oder so genannten Rescue-Modelle – Zellkulturen, in denen die Mutation mit Hilfe neuartiger Gene-Editing-Methoden, wie zum Beispiel „CRISPR-Cas“, der so genannten Genschere, wieder repariert worden sind – dienen hierbei als Kontrolle. „Wir verfügen über bildgebende Techniken, um automatisiert und unter Einsatz selbstlernender Algorithmen, also künstlicher Intelligenz, die Zellkulturen zu analysieren“, sagt Mona Boye: „Der Einsatz von KI ermöglicht es uns, selbst sehr geringfügige und heterogene Strukturveränderungen in den Zellen zu erkennen, wenn wir sie mit den Kontrollzellen vergleichen. Nur mit einer vollautomatisierten Hochdurchsatz-Technologie wie der von Ksilink lassen sich große Substanzbibliotheken untersuchen, um aussagekräftige Ergebnisse zu erzielen.“
Die von Patienten stammenden und parkinson-typische Veränderungen aufweisenden Zellkulturen werden unter den hochauflösenden Mikroskopen ebenso mit den Molekülen aus der Substanzbibliothek in Kontakt gebracht, wie die gentechnisch generierten Kontrollen, die kein Parkinson entwickeln. „In den Zellkulturen werden wir dann mit Hilfe unserer bildanalysierenden Verfahren beobachten, welche Substanzen in der Lage sind, die erkrankenden Zellen hin zum gesunden Zustand zu verschieben so Boye: „So identifizieren wir potentielle Wirkstoff-Kandidaten, die wir genauer unter die Lupe nehmen und bis zum präklinisch validierten Kandidaten weiterentwickeln.“
Ein weiterer Schritt wird die Aufklärung des Wirkmechanismus sein: „Unsere Vorgehensweise wird als „ungerichtet“ bezeichnet“, erklärt Boye: „Wir fokussieren uns nicht auf ein bestimmtes Zielmolekül oder einen bestimmten Signaltransduktionsweg, sondern testen die Substanzen am vollständigen, komplexen Zellsystem. Die Chance hier einen neuartigen Wirkstoff zu identifizieren, der für eine völlig neue Wirkstoffklasse steht, ist hoch. Im Rahmen der weiteren Wirkstoffentwicklung werden das genaue Zielmolekül und der Wirkmechanismus bestimmt.“ Wenn diese Untersuchungen erfolgreich sind, also eine Substanz die erhoffte Wirkung im Zellsytem zeigt und sich ein verträglicher Wirkmechanismus nachweisen lässt, kann der potentielle Wirkstoff in die weitere präklinische und klinische Entwicklung gehen. „Die Aussicht, dass dieser innovative Ansatz zur Identifikation neuer Wirkstoffe erfolgreich zu einem Medikament führt, ist wesentlich höher als bei klassischen Ansätzen“, erklärt Boye: „In unserer Kooperation mit dem LCSB kommen von Anfang an patienten-basierte Zellmodelle zum Einsatz. Potentielle Wirkstoffe werden direkt mit Hilfe dieser Patientenzellen identifiziert und unter Berücksichtigung industrieller Standards bis zu einem präklinisch validierten Kandidaten vorangetrieben. Technische oder regulatorische Fehler, die in der Frühphase in Labors ohne enge industrielle Anbindung passieren können, werden vermieden.“
Für Rejko Krüger ist die Kooperation von Ksilink und LCSB ein Glanzlicht seiner mittlerweile vierjährigen Arbeit in Luxemburg: „Dank des PEARL-Grants des FNR und der Luxemburger Parkinson-Studie (NCER-PD), die wir mit starker Unterstützung Luxemburgs aufbauen konnten, und den idealen Forschungsbedingungen im Großherzogtum konnten wir eine wissenschaftliche Exzellenz entwickeln, die unsere Arbeitsgruppen am LCSB ebenso wie unsere zahlreichen klinisch-wissenschaftlichen Partner im Land sehr attraktiv für Kooperationen mit Pharma-Unternehmen gemacht hat. Wenn aus der Zusammenarbeit mit Ksilink jetzt wirklich ein viel versprechender Wirkstoffkandidat herauskommt, der auch die folgenden klinischen Studien besteht, wäre dies sicher ein Höhepunkt für unsere gemeinsame Parkinson-Forschung in Luxemburg.“