Alzheimerforschung: Toxische Proteinklümpchen können eigenen Abbau verhindern
Viele neurodegenerative Erkrankungen wie auch die Alzheimer-Demenz werden durch die Verklumpung von bestimmten Eiweißmolekülen (Proteinen) ausgelöst. Forscher der Heinrich-Heine-Universität Düsseldorf (HHU) und des Forschungszentrums Jülich (FZJ) haben nun zusammen mit Kollegen aus den USA festgestellt, dass sich die besonders giftigen kleinen Aggregate, die sogenannten Oligomere, gegen ihren eigenen Abbau schützen und somit länger toxisch wirken können.
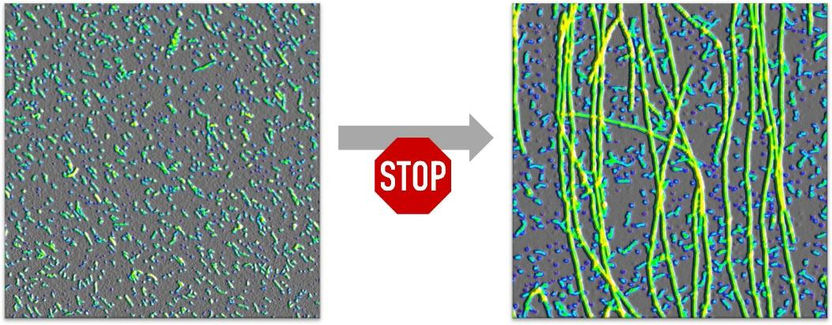
Oligomere (links) verhindern aktiv, dass sie zu Fibrillen (Fäden im rechten Bild) abgebaut werden.
Copyright: Wolfgang Hoyer / HHU
Oligomere sind Aggregate aus wenigen Protein-Molekülen, im Falle der Alzheimer-Demenz beispielsweise des Proteins Amyloid-beta (Aβ). Neben Oligomeren können aus diesen Proteinen auch größere Strukturen entstehen, die Fibrillen und schließlich Plaques, die sich aus Fibrillen bilden. Alle diese Stoffe sind giftig für Nervenzellen. Man hat allerdings herausgefunden, dass die Oligomere am gefährlichsten sind, da sie schon in besonders kleinen Mengen Nervenzellen schädigen oder sogar töten.
Die Düsseldorfer und Jülicher Forscher um Dr. Wolfgang Hoyer vom HHU-Institut für Physikalische Biologie untersuchten zusammen mit Kollegen von der University of South Florida, wie Oligomere entstehen und wie sie im Laufe der Zeit zu Fibrillen abgebaut werden. Dabei stellte sich heraus, dass sich Oligomere und Fibrillen unabhängig voneinander bilden und beide um den gleichen Vorrat von Amyloid-beta-Proteinbausteinen konkurrieren. Die Oligomere sind zwar kurzlebiger als die Fibrillen und zerfallen nach gewisser Zeit wieder in ihre Bestandteile. Die Forscher fanden aber, dass die Oligomere aktiv die Bildung der Fibrillen stören, sich also selbst vor dem Abbau schützen können.
Dr. Hoyer zu den weiterreichenden Konsequenzen der Studie: “Unsere Ergebnisse geben einen Erklärungsansatz, warum die Schwere einer Alzheimer-Demenz nur wenig mit der Menge an Plaques zusammenhängt. Die klinische Symptomatik kann vielmehr mit der Menge der Oligomere korreliert sein.” Entsprechend wären auch die Oligomere ein vorrangiges Ziel für die Wirkstoffentwicklung bei der Alzheimertherapie.
Originalveröffentlichung
Filip Hasecke, Tatiana Miti, Carlos Perez, Jeremy Barton, Daniel Schölzel, Lothar Gremer, Clara S. R. Grüning, Garrett Matthews, Georg Meisl, Tuomas P. J. Knowles, Dieter Willbold, Philipp Neudecker, Henrike Heise, Ghanim Ullah, Wolfgang Hoyer, Martin Muschol; "Origin of metastable oligomers and their effects on amyloid fibril self-assembly"; Chemical Science; 2018
Meistgelesene News
Originalveröffentlichung
Filip Hasecke, Tatiana Miti, Carlos Perez, Jeremy Barton, Daniel Schölzel, Lothar Gremer, Clara S. R. Grüning, Garrett Matthews, Georg Meisl, Tuomas P. J. Knowles, Dieter Willbold, Philipp Neudecker, Henrike Heise, Ghanim Ullah, Wolfgang Hoyer, Martin Muschol; "Origin of metastable oligomers and their effects on amyloid fibril self-assembly"; Chemical Science; 2018
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.