Protein steuert Verklumpung der Blutplättchen bei Thrombose und Schlaganfall
Ein Zellprotein namens TRPM7 übernimmt bei der Verklumpung der Blutplättchen im Zuge der Blutgerinnung vermutlich eine wichtige Doppelfunktion. Das konnten Wissenschaftler des Rudolf-Virchow-Zentrums und des Klinikums der Universität Würzburg nun in einer aufwändigen Studie zeigen. Ihre Ergebnisse könnten dazu beitragen, die Behandlung von Thrombosen, Herzinfarkten oder Schlaganfällen zu verbessern.
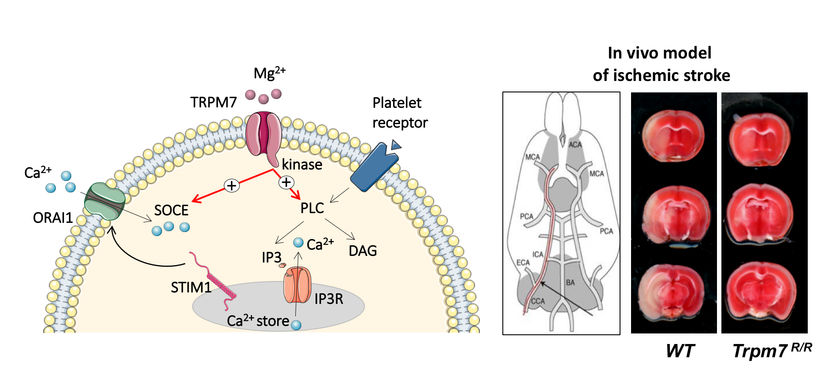
Mechanismus vom TRPM7-Protein (Abb. links) / Mäuse ohne TRPM7 (R/R) hatten erheblich weniger Hirngewebe geschädigt als die Kontrollmäuse (WT), nach einem induzierten Schlaganfall (Abb. rechts).
Universität Würzburg
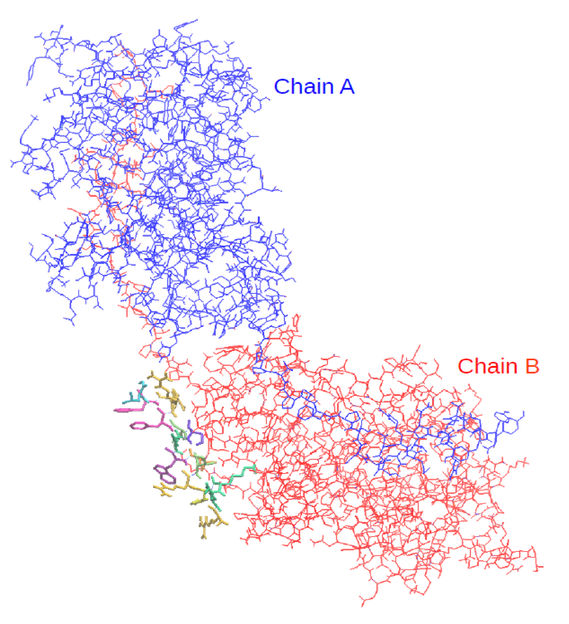
Proteinstruktur von der TRPM7 Kinase-Domäne
Prof. Thomas Dandekar, Universität Würzburg
So entwickelten Mäuse, bei denen das TRPM7 nur eine seiner beiden Funktionen erfüllte, nach einem Schlaganfall deutlich geringere Hirnschädigungen.
Blutplättchen dichten Verletzungen ab
Blutplättchen, fachsprachlich Thrombozyten, fließen mit dem Blutstrom durch den Körper. Normalerweise ähneln sie winzigen Frisbee-Scheiben. Bei einer Verletzung verändert sich ihre Gestalt: Binnen Minuten wachsen ihnen Dutzende tentakelartiger Ärmchen. Diese verhaken sich mit den Tentakeln benachbarter Thrombozyten, ganz ähnlich wie bei einem Klettverschluss. Es entsteht ein Pfropf, der das Loch in der Gefäßwand abdichtet und der in der Folge durch zusätzliche Gerinnungsprozesse weiter verstärkt wird.
Die Aktivierung der Blutplättchen unterliegt einer strengen Kontrolle. Ansonsten bestünde die Gefahr, dass sie sich ohne Not unterhaken und auch intakte Gefäße verstopfen. Ein wichtiger Regulator sind Kalzium-Ionen: Bei einer Verletzung nehmen die Blutplättchen Kalzium auf und leiten damit unter anderem ihren Gestaltwechsel ein. Als Gegenspieler fungieren dagegen Magnesium-Ionen, die die Aktivierung der Plättchen und damit die Bildung von Gerinnseln verhindern.
Das Zellprotein TRPM7 scheint an der Schnittstelle dieser beiden regulatorischen Prozesse zu stehen. „TRPM7 fungiert einerseits als Kanal, der Magnesium-Ionen in die Zelle lässt“, erklärt der Leiter der Studie, Dr. Attila Braun. „Ein anderer Teil des TRPM7 arbeitet zudem als Enzym, das in den Kalzium-Stoffwechsel der Blutplättchen eingreift. Wir konnten nun erstmals zeigen, dass dieses Enzym indirekt die Aufnahme von Kalzium-Ionen und somit die Verklumpung der Blutplättchen fördert.“
Mäuse hatten weniger Beeinträchtigungen
Dieser Nachweis gelang den Wissenschaftlern mit Hilfe von Mäusen, bei denen das TRPM7 seine Enzymfunktion eingebüßt hatte. „Die Kalziumaufnahme in die Thrombozyten war bei den Tieren dadurch vermindert“, betont Braun. „Als Kanal für Magnesium-Ionen war das TRPM7 dagegen weiterhin voll funktionstüchtig.“ Als Folge bildeten die Nager kaum noch größere Blutgerinnsel, wie sie beispielsweise bei einer Thrombose entstehen. Nach einem Schlaganfall entwickelten sie zudem deutlich weniger Hirnschädigungen. „Die abgestorbenen Regionen waren bei ihnen um 60 Prozent kleiner als bei normalen Mäusen“, sagt Braun. „Auch waren bei ihnen die neurologischen Folgen des Schlaganfalls wie etwa Lähmungserscheinungen erheblich schwächer ausgeprägt.“
Bislang war völlig unbekannt, welche physiologische Rolle die Enzymfunktion des TRPM7 spielt. „Unsere Arbeit ist ein erster Schritt, um diese Frage zu klären“, betont Braun. „Weitere Details müssen jetzt erforscht werden – wie auch die Frage, ob das TRPM7 im Menschen eine ähnliche Doppelrolle erfüllt wie in der Maus.“
Falls ja, haben die Erkenntnisse möglicherweise langfristig auch medizinische Relevanz. Denn Blutplättchen spiele eine wichtige Rolle bei der Entstehung von Schlaganfällen, Herzinfarkten und Thrombosen. Wirkstoffe, die ganz gezielt die enzymatische Funktion des TRPM7 hemmen, könnten daher eventuell irgendwann dazu beitragen, die Behandlung dieser schweren Erkrankungen zu verbessern.