Von Hefe für Demenzerkrankungen lernen
Biophysiker des Forschungszentrums Jülich und der Heinrich-Heine-Universität Düsseldorf (HHU) untersuchten zusammen mit japanischen Kollegen die Faltung bestimmter Proteine bei Hefepilzen. Sie fanden ähnliche Mechanismen wie bei sogenannten Prionen, also solchen Eiweißen, die fehlgefaltet sind und die neurodegenerative Erkrankungen auslösen. Mit den Prionen in Hefen gewannen die Forscher neue Erkenntnisse über die Entstehung der schädlichen Eiweiße.
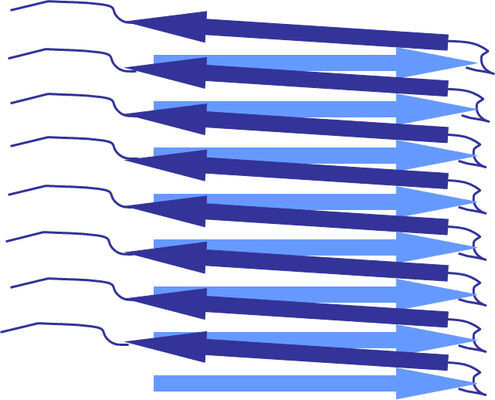
Schematische Darstellung von Amyloid-Fibrillen mit parallel verlaufenden beta-Faltblättern, wie sie auch in dem untersuchten Prion vorliegen.
Copyright: HHU / Henrike Heise
Proteine sind zentrale Bausteine jedes lebenden Organismus, sie dienen sowohl als Strukturmaterial als auch als Botenstoffe im Körper. Diese Proteine setzen sich ihrerseits aus einzelnen Aminosäurebausteinen zusammen. Der Bauplan, nach dem der Körper sie herstellt, ist im genetischen Code hinterlegt.
Die Proteine, die zum Teil aus hunderten bis tausenden Aminosäuren bestehen, sind komplex gefaltete dreidimensionale Gebilde. Ihre Struktur ist von entscheidender Bedeutung für ihre Funktion. Kommt es zu Faltungsfehlern, verlieren die Proteine nicht nur ihre biologische Funktion; sie können unter anderem auch neurodegenerative Erkrankungen verursachen. Für die Rinderkrankheit BSE beziehungsweise die Creutzfeld-Jakob-Erkrankung beim Menschen sind Prionen verantwortlich, Aggregate aus fehlgefalteten körpereigenen Proteinen. Diese sind in der Lage, ihre falsche Struktur auf andere Proteine zu übertragen und sind damit ansteckend. Prionen können Nervengewebe zerstören.
Auch in Hefen gibt es Proteine, die – wie bei den Krankheitserregern beim Tier und Menschen – infektiöse Zusammenlagerungen, Prionen, bilden können. Hefen eignen sich deshalb gut als Studienobjekt, um zentrale Mechanismen bei den humanen Krankheiten zu untersuchen. Die Arbeitsgruppe um Prof. Dr. Henrike Heise vom Jülicher Institute for Complex Systems – Strukturbiochemie und dem Institut für Physikalische Biologie der HHU untersuchte zusammen mit Kollegen des japanischen RIKEN-Forschungsinstituts mit Hilfe der Kernspinresonanztomografie vor allem, welchen Einfluss Umweltbedingungen oder genetische Faktoren auf die Struktur der Prionen und damit auf ihre spezifischen Eigenschaften wie Infektiosität haben.
In der aktuellen Studie untersuchten die Wissenschaftler eine Punktmutation, in der eine einzige Aminosäure im Zentrum des fehlgefalteten Bereiches – des Amyloid-Kernbereiches – durch eine andere ersetzt ist. Dieser einzelne Aminosäureaustausch führt u.a. dazu, dass der Proteinmutant bereits im ungefalteten Zustand weniger kompakt ist, was letztendlich Auswirkungen auf die Zusammenlagerung der Proteine hat.
Dies sind wichtige Erkenntnisse für das Verständnis der Bildung von fehlerhaften und krankmachenden Proteinstrukturen. Auf dieser Grundlage kann es auch möglich sein, neue Therapieansätze zu finden. Neben der Creutzfeld-Jakob-Krankheit ist dies auch für andere neurologische Erkrankungen wie die Alzheimer-Demenz oder Parkinson relevant, da auch diese von fehlerhaft aufgebauten Proteinen verursacht werden, die sich verklumpen und in der Folge Nervenzellen schädigen können.
Originalveröffentlichung
"Molecular basis for diversification of yeast prion strain conformation"; Yumiko Ohhashi, Yoshiki Yamaguchi, Hiroshi Kurahashi, Yuji O. Kamatari, Shinju Sugiyama, Boran Uluca, Timo Piechatzek, Yusuke Komi, Toshinobu Shida, Henrik Müller, Shinya Hanashima, Henrike Heise, Kazuo Kuwata and Motomasa Tanaka; PNAS; 2018.
Meistgelesene News
Originalveröffentlichung
"Molecular basis for diversification of yeast prion strain conformation"; Yumiko Ohhashi, Yoshiki Yamaguchi, Hiroshi Kurahashi, Yuji O. Kamatari, Shinju Sugiyama, Boran Uluca, Timo Piechatzek, Yusuke Komi, Toshinobu Shida, Henrik Müller, Shinya Hanashima, Henrike Heise, Kazuo Kuwata and Motomasa Tanaka; PNAS; 2018.
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren

Antibody Stabilizer von CANDOR Bioscience
Protein- und Antikörperstabilisierung leicht gemacht
Langzeitlagerung ohne Einfrieren – Einfache Anwendung, zuverlässiger Schutz

DynaPro NanoStar II von Wyatt Technology
NanoStar II: DLS und SLS mit Touch-Bedienung
Größe, Partikelkonzentration und mehr für Proteine, Viren und andere Biomoleküle

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.



















































