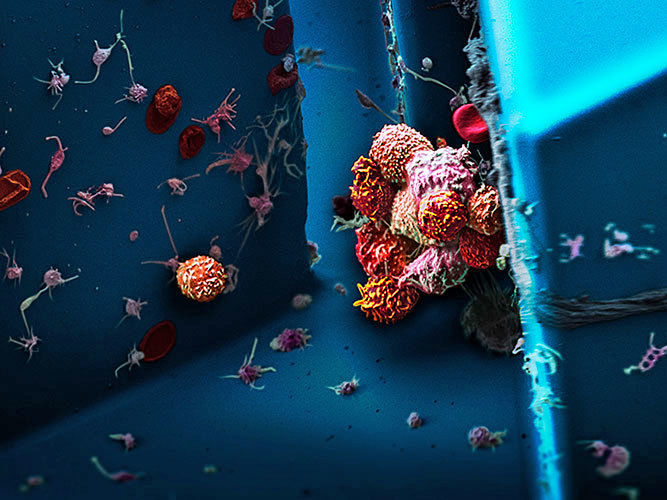
Strahlentherapie: Gelöste Elektronen gefährlicher als freie Radikale?
Göttinger Forscher entdecken möglichen neuen Mechanismus für Strahlenschäden an der DNA
Lange Zeit nahm man an, dass die Schäden an der menschlichen Erbsubstanz (DNA) durch Hochenergiestrahlung in erster Linie durch so genannte freie Radikale hervorgerufen werden. Wissenschaftler an der Universität Göttingen und am Göttinger Max-Planck-Institut für Dynamik und Selbstorganisation haben nun herausgefunden, dass ein anderes Teilchen bei der Bestrahlung möglicherweise viel gefährlicher für die DNA ist: ein hydratisiertes, also von Wassermolekülen umgebenes Elektron. Ihre Erkenntnisse könnten Folgen haben für den Einsatz von Strahlentherapien im Kampf gegen Krebs. "Unsere Forschungsergebnisse könnten dazu führen, dass Strahlungsdosen in Zukunft möglicherweise neu bewertet werden müssen. Der neue DNA-Spaltungsmechanismus könnte dabei möglicherweise auch Auswirkungen auf die Dosierung der Strahlentherapie von Krebs haben," so der Leiter der Arbeitsgruppe Prof. Dr. Bernd Abel von der Universität Göttingen.
45 Jahre nach der Entdeckung des freien gelösten Elektrons in Wasser gelang es den Forschern in Zusammenarbeit mit Kollegen aus Leipzig und Berlin, erstmals die bisher unbekannte Bindungsenergie des Elektrons zu messen. Das ist die Energie, die benötigt wird, um das Elektron wieder aus der Wasserumgebung herauszulösen. Wenn Hochenergiestrahlung auf die DNA einer Zelle trifft, werden lebenswichtige Zellbestandteile zerstört und die Zelle damit abgetötet - ein Mechanismus, der bei der Strahlentherapie zur Bekämpfung von Krebs ausgenutzt wird. Gleichzeitig schädigt die Strahlung aber auch gesunde Zellen.
Neben freien Radikalen entstehen bei der hochenergetischen Bestrahlung von Wasser in biologischem Gewebe in Wasser gelöste Elektronen an Grenzflächen wie zum Beispiel Membranen oder den Wänden von Biomolekülen. Bei ihren Untersuchungen stießen die Wissenschaftler erstmals auf eine bisher unbekannte Spezies: das nur teilweise gelöste Elektron an einer Wasser-Grenzfläche. Dessen Existenz und Lebensdauer wiesen sie erstmalig mit einer schnellen Kamera für kurzlebige reaktive Teilchen nach. Diese Elektronen sind offenbar deshalb so gefährlich, weil sie aufgrund ihrer "gerade passenden" (Bindungs-)Energie ebenfalls DNA spalten können. Da sie lange leben, können sie ihre schädigende Wirkung zudem besonders gut entfalten.
Prof. Abel ist Mitglied der Graduiertenschule für Neurowissenschaften und molekulare Biowissenschaften sowie Principal Investigator des Courant Forschungszentrums "Nanospektroskopie und Röntgenbildgebung" der Universität Göttingen. Beide Einrichtungen werden im Rahmen der Exzellenzinitiative des Bundes und der Länder gefördert. Seit 2008 ist er außerdem Professor für Physikalische Chemie und Reaktionsdynamik an der Universität Leipzig. Prof. Dr. Udo Buck und Dr. Manfred Faubel arbeiten am Göttinger Max-Planck-Institut für Dynamik und Selbstorganisation.
Originalveröffentlichung: K. R. Siefermann, Y. Liu, E. Lugovoy, O. Link, M. Faubel, U. Buck, B. Winter and B. Abel; "Binding energies, lifetimes and implications of bulk and interface solvated electrons in water"; Nature Chemistry, Published online: 7 March 2010
Meistgelesene News
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte
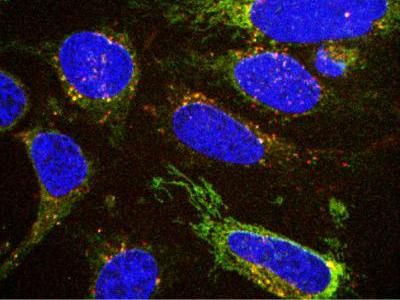
Ausspionieren der Essgewohnheiten von Zellen könnte die Krebsdiagnose erleichtern
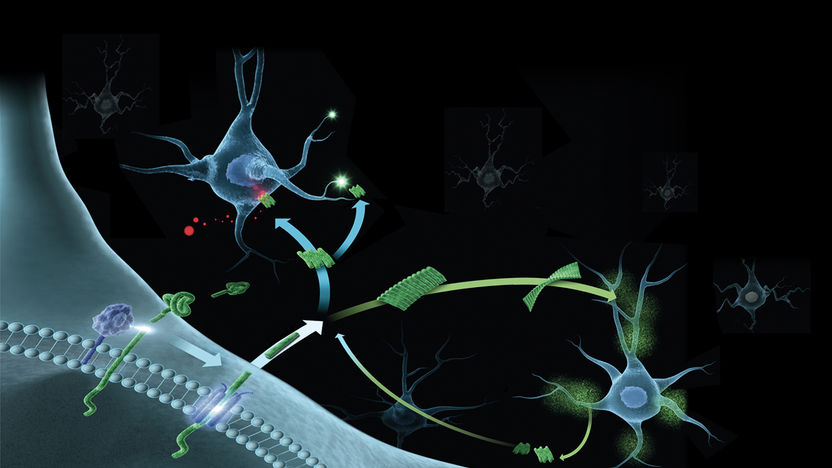
Erstmals "Funktionsverlust" des Alzheimer-Proteins Aβ beobachtet - Durch Aggregation verliert Aβ die Bindefähigkeit an einen wichtigen Bestandteil der Nervenzellmembran
Cytonet präsentiert weltweit erste klinische Studie zu Leberzell-Medikament - Neue Hoffnung bei schweren Lebererkrankungen
Nervus_mandibularis
Zirkumventrikuläres_Organ
3-Caren
Metabolisches_Äquivalent
Darwin_(Einheit)
MDC-Forscher dem Geheimnis der Berührung auf der Spur

Lonza erzielt 2022 ein starkes Ergebnis - Wachstumsinvestitionen werden fortgesetzt