Scoperta la funzione di un blocco di costruzione dell'HIV finora misterioso
I ricercatori hanno acquisito nuove conoscenze su come matura lo strato di matrice dell'HIV-1
I ricercatori dell'Istituto Max Planck di Biochimica hanno scoperto il meccanismo alla base di un'importante fase del ciclo vitale dell'HIV. In collaborazione con team delle Università di Heidelberg e Yale, hanno scoperto che l'enigmatico "peptide spaziatore 2", uno dei componenti virali, svolge un ruolo chiave nella conversione delle particelle immature di HIV-1 in particelle infettive. I risultati dello studio sono stati pubblicati sulla rivista Nature .
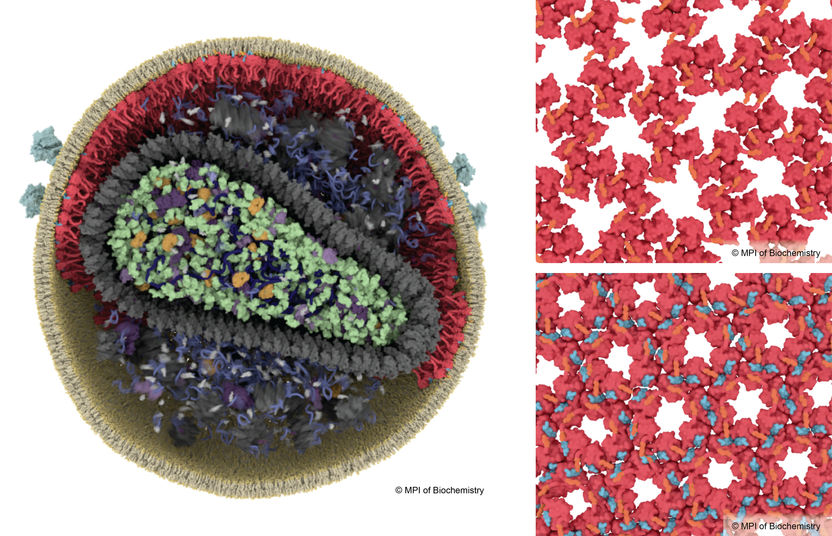
Per diventare infettivo, l'HIV deve subire un processo di maturazione. Nell'HIV immaturo, le proteine della matrice (in rosso) formano un reticolo non compatto (in alto a destra), mentre nell'HIV maturo la formazione di un reticolo stabile è innescata dalla proteina SP2 (in blu, in basso a destra).
Margot Riggi, MPI of Biochemistry
Le particelle di HIV-1 (virus dell'immunodeficienza umana) vengono rilasciate dalle cellule infette in forma immatura e non infettiva. Il principale materiale di costruzione di una particella virale è costituito da circa 2000 copie di una proteina lunga e a forma di bastoncino chiamata Gag. Per diventare infettivo, l'HIV deve subire un processo di maturazione. Questo processo coinvolge la proteasi dell'HIV-1 (un enzima virale), che taglia la Gag in sei proteine più piccole, tra cui le proteine del capside e della matrice. Questo porta a un ampio riarrangiamento strutturale dei componenti del virus.
Per molti anni gli scienziati hanno studiato le trasformazioni strutturali del capside virale che avvolge il genoma virale. Al contrario, si sa molto meno della matrice virale - l'involucro proteico esterno direttamente sotto la membrana lipidica che circonda il virus. I ricercatori guidati da John Briggs, direttore e biologo strutturale dell'Istituto Max Planck di Biochimica, hanno ora scoperto come le proteine della matrice si riorganizzano durante la maturazione in una particella infettiva.
I ricercatori hanno utilizzato microscopi crioelettronici all'avanguardia per visualizzare le particelle del virus e poi hanno usato l'analisi delle immagini assistita dal computer per creare modelli 3D molto dettagliati delle proteine del virus. Contrariamente alle loro aspettative, hanno scoperto che il riarrangiamento della matrice è innescato dal "peptide spaziatore 2", che si lega alla matrice e la riorganizza. Il peptide spaziatore 2 è un altro dei sei blocchi di costruzione che vengono prodotti dal taglio di Gag, ma la cui funzione era finora sconosciuta. Legando il peptide spaziatore 2 alla proteina matrice, il virus può fondersi più rapidamente con le cellule ospiti da infettare. Il lavoro è stato svolto insieme a partner dell'Università di Heidelberg e dell'Università di Yale, negli Stati Uniti.
John Briggs spiega: "Nel nostro laboratorio abbiamo ottenuto i primi dati strutturali sulla matrice del virus nel 2021, ma non sapevamo cosa causa la ristrutturazione della matrice durante la maturazione del virus. In questo nuovo studio abbiamo prodotto viste 3D molto più dettagliate dello strato di matrice, importanti per comprendere i processi di rimodellamento virale".
James Stacey e Dominik Hrebík, i due primi autori dello studio, spiegano i loro risultati. James spiega: "La matrice del virus presenta una cavità nella sua forma matura. Sapevamo che qualcosa vi si legava, ma pensavamo che fosse una molecola lipidica della membrana. Ora siamo riusciti a dimostrare che si tratta del peptide spaziatore 2". Questo solleva la questione se questa cavità potrebbe essere un bersaglio per le molecole di farmaci in futuro". Dominik aggiunge: "Finora la funzione del peptide spaziatore 2 non era nota. Grazie alla microscopia crioelettronica ad alta risoluzione, abbiamo visto che questo peptide si lega direttamente alle proteine della matrice dopo il suo rilascio e collega le proteine tra loro nel virus maturo".
John Briggs riassume: "L'HIV-1 è probabilmente il virus meglio studiato, ma ci sono ancora fasi importanti della sua replicazione che non abbiamo ancora compreso".
Nota: questo articolo è stato tradotto utilizzando un sistema informatico senza intervento umano. LUMITOS offre queste traduzioni automatiche per presentare una gamma più ampia di notizie attuali. Poiché questo articolo è stato tradotto con traduzione automatica, è possibile che contenga errori di vocabolario, sintassi o grammatica. L'articolo originale in Tedesco può essere trovato qui.
Pubblicazione originale
James C. V. Stacey, Dominik Hrebík, Elizabeth Nand, Snehith Dyavari Shetty, Kun Qu, Marius Boicu, Maria Anders-Össwein, Pradeep D. Uchil, Robert A. Dick, Walther Mothes, Hans-Georg Kräusslich, Barbara Müller, John A. G. Briggs; "The conserved HIV-1 spacer peptide 2 triggers matrix lattice maturation"; Nature, 2025-2-26




















































