Un nuevo software detecta las mutaciones genéticas que causan enfermedades
El software encuentra "la aguja en un pajar", por ejemplo, en el diagnóstico de enfermedades raras
Anuncios
Una enfermedad grave suele ser el resultado de un único defecto genético. Pero dado que dos personas sanas ya tienen alrededor de tres millones de diferencias en su composición genética, no es tarea fácil determinar la desviación que causa una enfermedad de las muchas variantes genéticas inofensivas. Los científicos de la Unidad Central de Bioinformática del Instituto de Salud de Berlín (BIH) unieron sus fuerzas con los colegas de Charité - Universitätsmedizin Berlin y el Centro Max Delbrück de Medicina Molecular de la Asociación Helmholtz (MDC) para desarrollar un software que ayude a localizar esta "aguja en un pajar" genética, lo cual es particularmente importante en el diagnóstico de enfermedades raras. El software resultante "VarFish" está disponible gratuitamente y se explica en el último número de la revista Nucleic Acids Research.
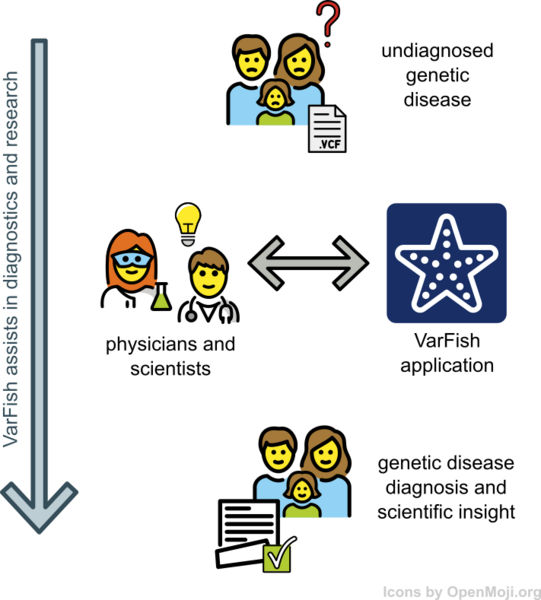
Berlin Institute of Health (BIH)
Las enfermedades raras no son necesariamente tan raras: Afectan a unos cuatro millones de personas sólo en Alemania. Pero de las 8.000 enfermedades diferentes que se estiman que entran en esta categoría, por lo general sólo hay unos pocos casos registrados de cada una. Como resultado, puede tomar años para que los afectados reciban el diagnóstico correcto - y sin embargo esto es un prerrequisito para una terapia efectiva. "Los padres de los niños afectados suelen acabar sentados frente a nosotros después de un largo y arduo viaje", dice la Dra. Nadja Ehmke, especialista del Instituto de Genética Médica y Genética Humana de la Charité. "Tienen un niño enfermo que no se desarrolla adecuadamente, ni mental ni físicamente, y quieren saber por qué. Si podemos usar un análisis genético para explicarles dónde está el defecto, esto es a menudo un gran alivio para los padres - aunque no significa necesariamente que se pueda hacer algo por su hijo en términos de tratamiento". Estos conocimientos permiten a los padres intercambiar información con otras personas que se encuentran en la misma situación, visitar o crear grupos de autoayuda, y evaluar mejor si otro niño también podría caer enfermo.
Los potentes programas informáticos detectan las diferencias
Para realizar el análisis genético, los científicos aíslan el material genético de las células sanguíneas de los pacientes, leen la secuencia - es decir, el orden de las letras - y lo comparan con el material genético de los padres, los hermanos o los análisis genéticos existentes en grandes bases de datos. "Aquí es donde los humanos alcanzan sus límites naturales", informa el Dr. Dieter Beule, jefe de la Unidad Central de Bioinformática del BIH. "Incluso si sólo analizamos las regiones codificadoras de proteínas del material genético, el llamado exoma, hay millones de bloques de construcción para comparar. Necesitamos un software potente para detectar las diferencias." Pero incluso en el material genético de dos individuos sanos, hay alrededor de 30.000 posiciones en estas regiones codificadoras (solamente) que difieren. ¿Cuál de las muchas variantes es la causa de la enfermedad? Esta fue la misma pregunta que motivó a Dieter Beule y su equipo a desarrollar VarFish. VarFish compara la secuencia del paciente con las secuencias de las bases de datos mundiales. Los científicos de la Unidad Central de Bioinformática utilizaron muchos recursos de datos abiertos y gratuitos, incluyendo las bases de datos estadounidenses del Centro Nacional de Información Biotecnológica (NCBI) de la Universidad de Washington en Seattle, y el Instituto Europeo de Bioinformática (EBI) en Cambridge, Reino Unido, así como las bases de datos y algoritmos propios de Charité y el BIH.
El ajuste en cuestión de segundos
"En cuestión de segundos, VarFish puede eliminar 29.950 de las 30.000 diferencias", explica Dieter Beule. "Esto se debe a que el software encuentra muchas de las mismas desviaciones, por ejemplo, en las secuencias de las muestras de población, donde aparentemente no conduce a problemas notables y por lo tanto, con toda probabilidad no es responsable de la enfermedad rara". Los científicos pueden entonces comparar las 50 variantes genéticas restantes con enfermedades hereditarias conocidas, reduciendo así el grupo de posibles culpables a unas diez mutaciones genéticas.
En algunos casos, los científicos también pueden descubrir mutaciones en un gen conocido durante su investigación. "VarFish permite realizar pruebas rápidas de mutaciones en genes conocidos", explica la profesora Ute Scholl, que tiene una cátedra Johanna Quandt en el BIH. "Esto es importante, ya que puede darnos pistas sobre qué droga puede ayudar y debe ser estudiada más a fondo en los ensayos clínicos." Si no hay mutaciones en los genes conocidos, VarFish puede ser usado para identificar un nuevo gen candidato dentro de una familia más grande o comparando varias familias afectadas con la misma enfermedad. El resultado producido por las mutaciones en ese gen candidato puede entonces determinarse a menudo en el laboratorio. El laboratorio de Ute Scholl introduce los genes mutados en cultivos celulares o en ratones y observa los efectos de la mutación. "Usando este método, hemos caracterizado recientemente un nuevo gen para una rara forma hereditaria de hipertensión arterial", informa el médico. Pero el desarrollo de la droga e incluso el tratamiento específico están todavía muy lejos: "En primer lugar, queremos entender cómo se desarrolla la enfermedad en primer lugar y dónde se originan los síntomas."
Diagnóstico rápido y preciso
El Dr. Manuel Holtgrewe, autor principal del artículo, está encantado de que el nuevo software esté encontrando tantos usuarios: "En sólo las primeras semanas, VarFish ha sido utilizado cientos de veces por científicos y médicos de todo el mundo. En nuestro propio laboratorio hemos analizado miles de conjuntos de datos con la ayuda de VarFish". La cooperación internacional es particularmente importante en la investigación y el tratamiento de las enfermedades raras, ya que cada mutación individual suele ocurrir sólo unas pocas veces en cada país. Informa el profesor Stefan Mundlos, jefe del Instituto de Genética Médica y Genética Humana de Charité y del Grupo de Desarrollo y Enfermedades del Instituto Max Planck de Genética Molecular de Berlín: "VarFish ha sido muy útil para permitirnos diagnosticar con rapidez y precisión a los participantes de nuestros ensayos clínicos".
Manuel Holtgrewe y Dieter Beule están planeando ahora ampliar VarFish para permitir el análisis a nivel de todo el genoma de las llamadas variantes estructurales. Además, se añadirán otras funciones para la colaboración eficaz y segura entre los genetistas humanos. "VarFish apoya a los usuarios en el análisis de sus datos genéticos moleculares tanto en la investigación básica como en la aplicación clínica", dice Dieter Beule. "La misión principal del BIH es la traducción - que implica la transferencia de los resultados de la investigación a la clínica y, viceversa, llevar las observaciones clínicas al laboratorio. Con nuestro software VarFish, apoyamos este mismo objetivo".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Manuel Holtgrewe, Oliver Stolpe, Mikko Nieminen, Stefan Mundlos, Alexej Knaus, Uwe Kornak, Dominik Seelow, Lara Segebrecht, Malte Spielmann, Björn Fischer-Zirnsak, Felix Boschann, Ute Scholl, Nadja Ehmke, Dieter Beule; "VarFish: comprehensive DNA variant analysis for diagnostics and research"; Nucleic Acids Research; 2020