Cortar el cáncer de riñón en sus raíces
Anuncios
Los científicos del MDC han descubierto células madre responsables de la forma más común de cáncer de riñón. El equipo de Walter Birchmeier ha encontrado una manera de bloquear el crecimiento de estos tumores en tres modelos de la enfermedad.
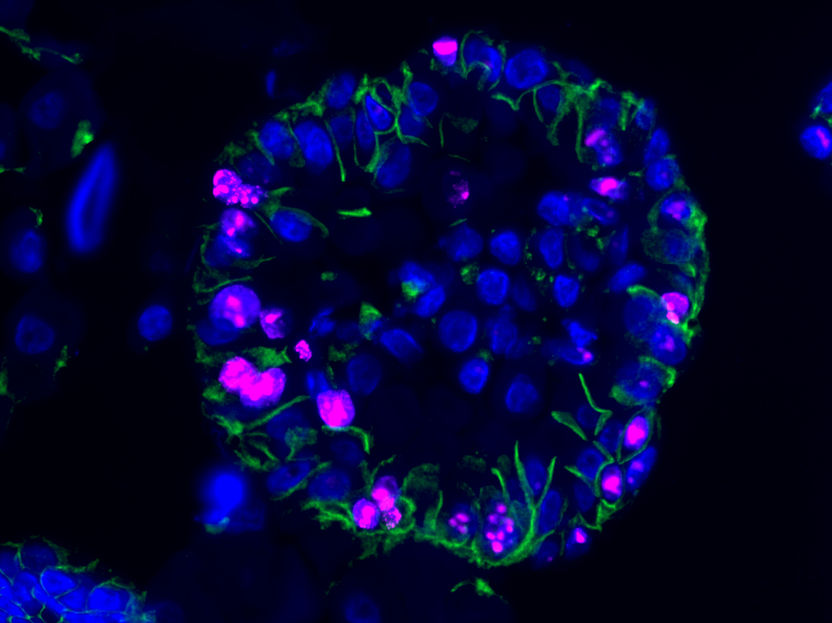
Organoides de ccRCC humanos bajo el microscopio, etiquetados con marcadores fluorescentes. Los científicos extrajeron células madre de cáncer de los pacientes y las usaron para cultivar estas versiones en miniatura de los tumores de riñón en el laboratorio. La estructura de los organoides se asemeja a los tumores de los pacientes y contiene los mismos tipos de células.
AG W. Birchmeier, MDC
No todas las células cancerosas son iguales. Los tumores contienen potentes células madre cancerosas que producen metástasis y pueden regenerar la enfermedad si escapan a un tratamiento. Esto los convierte en objetivos vitales para las terapias, si los científicos pueden aislarlos y probar sus debilidades. Pero las células son a menudo tan raras que para muchos tipos de cáncer, todavía no se han encontrado.
El laboratorio del profesor Walter Birchmeier del Centro Max Delbrück de Medicina Molecular de la Asociación Helmholtz (MDC), en colaboración con el Departamento de Urología de la Charité, ha descubierto ahora células madre cancerosas responsables de la forma más común de cáncer de riñón: el carcinoma de células renales de células claras, o ccRCC. En una colaboración en todo Berlín, los científicos encontraron una debilidad. Las células dependen de dos señales bioquímicas críticas. El bloqueo de ambos impide el crecimiento de tumores en varios modelos de laboratorio de la enfermedad, lo que sugiere un nuevo y prometedor enfoque para tratar a los pacientes humanos. La labor también pone de relieve la importancia permanente de los ratones en las investigaciones médicas. El estudio aparece en el número actual de Nature Communications e incluye a autores del MDC, el Departamento de Urología de la Charité - Universitätsmedizin Berlin, el Instituto de Salud de Berlín (BIH ), la Unidad de Cribado del Instituto Leibniz FMP, la compañía EPO, y otros socios.
Dos debilidades bioquímicas
La identificación de células madre de cáncer ccRCC fue crucial para el proyecto. La Dra. Annika Fendler, postdoctora del grupo Birchmeier y miembro del Departamento de Urología de Charité, fue la primera autora del artículo. Identificó tres proteínas en la superficie de las células que permitieron marcarlas y luego aislarlas. Esto permitió al Dr. Hans-Peter Rahn aislar las células usando la clasificación de células activadas por fluorescencia (FACS). Los científicos descubrieron que las células madre del cáncer representaban sólo un dos por ciento del total de los tumores humanos.
"Nuestro análisis de estas células muestra que dependen de las señales que se transmiten a través de dos redes bioquímicas llamadas WNT y NOTCH", dice Fendler. Debido a que se sabía que estas redes jugaban un papel en otros tipos de cáncer, el laboratorio ha aprendido a desbaratarlas. Ya habían desarrollado un potente inhibidor de las señales de WNT con el FMP, su instituto asociado en el campus de Berlín-Buch.
Anteriormente no se sospechaba que el WNT y el NOTCH tuvieran un papel en los tumores renales; las mutaciones en estas redes rara vez se encuentran en la enfermedad. Sin embargo, ambas señales están vinculadas a un gen supresor de tumores llamado VHL, que está fuertemente asociado con el ccRCC. Los nuevos hallazgos sugirieron que el bloqueo de las señales WNT, NOTCH o ambas, podría dirigirse a las células madre del cáncer e interferir con los componentes más agresivos de los tumores.
En la clínica, los inhibidores contra las diversas vías bioquímicas están reemplazando cada vez más a la quimioterapia en los tratamientos para pacientes con cáncer. "Pero tienes que saber qué caminos tomar como objetivo", dice Fendler, "y no se sabía lo suficiente sobre la biología del ccRCC".
La promesa de múltiples sistemas modelo
Las pruebas iniciales de los nuevos inhibidores eran prometedoras. "Sorprendentemente, tres cuartas partes de los cultivos celulares derivados de los pacientes respondieron al menos a un tipo de inhibidor, y el 50 por ciento del resto se inhibieron en presencia de los dos inhibidores", dice Birchmeier.
Pero aquí el laboratorio se enfrentó a uno de los principales retos de la investigación del cáncer. "Lo que aprendemos en el laboratorio suele ser muy difícil de traducir al contexto real de un paciente", dice Birchmeier. "Los cultivos de líneas celulares regulares y los modelos animales obtenidos de otros laboratorios no reflejan la complejidad de una enfermedad en el cuerpo de una persona". Una solución es desarrollar más tipos de modelos que estén más cerca de la enfermedad humana.
Birchmeier y sus colegas ya eran expertos en extraer células madre de pacientes con cáncer, cultivarlas y desafiarlas con una enorme paleta de drogas. En colaboración con la empresa EPO en el campus de Berlín-Buch, también han transplantado células madre cancerígenas de pacientes a ratones, que desarrollan tumores prácticamente idénticos a los de sus homólogos humanos. Estos animales son esenciales en la búsqueda de terapias: lo que cura un tumor humano en ratones también podría funcionar en un paciente. En el proyecto actual, la EPO inyectó inhibidores de WNT y NOTCH, solos y en combinación, en ratones portadores de tumores y observó lo que sucedió. Bloquear ambas señales resultó ser la estrategia más efectiva. ¿Pero funcionaría igual de bien en los humanos?
Un nuevo tipo de modelo
Muy recientemente los científicos han aprendido a utilizar las células de los pacientes para generar organoides: versiones en miniatura de los órganos, que contienen muchos tipos de células. Están compuestos de tejido humano, pero pueden ser usados sin los problemas éticos de probar drogas en pacientes humanos. Ya se habían creado órganos para los riñones sanos, varios órganos y tumores como el cáncer de colon.
"Otros grupos habían intentado con ccRCC, pero habían tenido menos éxito", dice Fendler. "El tejido no creció muy bien o no produjo organoides. Ambos factores son importantes para desarrollar modelos de pruebas y tratamientos de drogas. Un paciente con la enfermedad necesita modelos rápidos y fiables en los que se puedan probar las respuestas al tratamiento".
Diferentes modelos, resultados similares
"El hallazgo más crucial del estudio", dice Birchmeier, "es haber identificado los papeles esenciales de los sistemas de señalización WNT y NOTCH en el ccRCC, y mostrar que su inhibición tiene un impacto en los tumores". Sigue habiendo sutiles diferencias entre los sistemas modelo que aún deben explorarse; por el momento, todavía se necesitan estudios de ratones.
Mientras tanto, el trabajo proporciona nuevos e importantes sistemas experimentales para los científicos que trabajan en la enfermedad. Annika Fendler se ha trasladado al Instituto Francis Crick de Londres, donde sigue trabajando en modelos de cáncer de riñón. En última instancia, los científicos esperan que la estrategia desarrollada en los modelos dé el salto a la clínica, en terapias diseñadas a medida que se dirigen a las células más peligrosas de los tumores.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.