T-Zellen gegen Krebs: Erziehung oder Zerstörung?
Anzeigen
Trotz der kosten- und zeitintensiven Behandlung von Tumorpatienten ist Krebs nach den Erkrankungen des Herz-Kreislaufsystems die zweithäufigste Todesursache in den Ländern der industrialisierten Welt. Zytotoxische Therapien, wie z. B. die Chemotherapie und die Strahlentherapie, stellen neben der chirurgischen Entfernung des (Primär-)Tumors die Säulen der Krebstherapie dar. Die Behandlung von Krebszellen mit Chemotherapeutika führt zur Aktivierung von zellulären "Selbstmordprogrammen", das heisst zur Induktion der Apoptose. Zytotoxische Behandlungen sind jedoch häufig mit belastenden Nebeneffekten wie z. B. neurosensorischen Ausfällen, Fieber und Anämien behaftet.
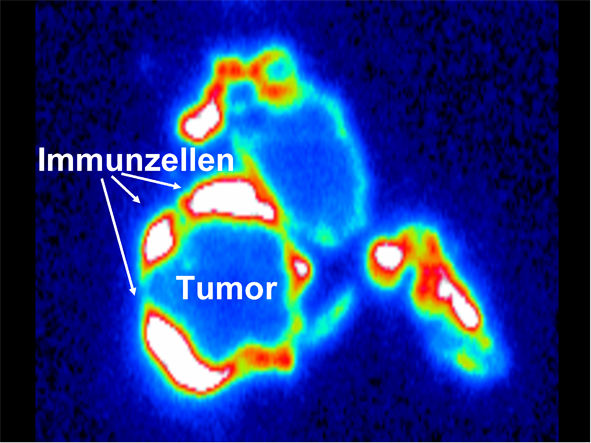
T Helferzellen belagern einen endogenen Tumor; modifiziert nach Wieder et al., (2008) Cell Cycle2974-2977.
AG Prof. Röcken
Weiterhin überleben im Falle einer ausgedehnten Metastasenbildung trotz aktueller, meist gewebszerstörender Therapieansätze nur ein Bruchteil der Betroffenen die folgenden fünf Jahre; z. B. liegen die Fünfjahresüberlebensraten von Lungen- und Bauchspeicheldrüsenkrebs unterhalb von 10%.
Es besteht somit ein dringender Bedarf an verbesserten und alternativen Therapien zur Krebsbekämpfung. Eine dieser Möglichkeiten stellt die Immuntherapie dar, bei der das körpereigene Abwehrsystem zur Bekämpfung von Krebszellen eingesetzt wird. Neben dem Einsatz von Vakzinen, welcher zu einer T-Zell-vermittelten Immunantwort führen kann, wurde in der Zwischenzeit bereits an einigen Patienten ein adoptiver Transfer von Immunzellen, in diesem Fall von Tumorantigen-spezifischen T-Helferzellen, erfolgreich praktiziert.
In dem von der Wilhelm Sander-Stiftung geförderten Projekt sucht ein Forschungsteam um Prof. Dr. Martin Röcken vom Lehrstuhl für Dermatologie der Universität Tübingen nach Möglichkeiten, endogen wachsende Tumore mittels adoptivem Transfer von T-Zellen einzudämmen. Als in vivo Modell eines endogen wachsenden Tumors werden RIP1-Tag2 Mäuse verwendet, die das T-Antigen (Tag) des Simian Virus 40 (SV40) unter der Kontrolle des Insulinpromoters (RIP1) exprimieren. Dies führt zu einer gewebsspezifischen Expression von Tag in allen Insulin-produzierenden beta-Zellen des endokrinen Pankreas. Beginnend mit der Entwicklung von 2-3 Adenomen, die sich danach zu Inselzellkarzinomen transformieren, sterben die Mäuse nach 14-16 Wochen an einer Hypoglykämie. Überraschenderweise erwiesen sich in diesen Untersuchungen T-Helferzellen als die bislang wirksamste Therapie gegen diesen sehr aggressiven Tumor, wobei die tumoreindämmende Wirkung der T-Helferzellen nicht auf der Zerstörung des Gewebes zu beruhen scheint.
Mit neuen experimentellen Ansätzen untersuchen Prof. Dr. Röcken und Mitarbeiter, inwieweit eine T-Helferzellen-basierte Therapie bei endogen wachsenden Tumoren vom Zytokinnetzwerk, insbesondere dem Th1 Zytokin IFN-gamma, abhängt, und wie tumorspezifische Th1-Lymphozyten die physiologischen und biochemischen Merkmale endogen wachsender Tumore beeinflussen, ohne sie zu zerstören. Beide Fragestellungen werden sowohl an isolierten Tumorzellen (beta-Insulinomzellen) als auch an Gewebsschnitten von Mäusen vor, während und nach einer Therapie mit Tumorantigen-spezifischen Th1-Lymphozyten durchgeführt. Von den Untersuchungen erwarten die Forscher neue Erkenntnisse über die Wirksamkeit und den Mechanismus einer T-Zell-basierten Immuntherapie. Dies wird dann in absehbarer Zeit die Voraussetzungen für die Einführung alternativer, zellulärer Therapien zur Tumorbekämpfung beim Menschen schaffen, die möglicherweise mit geringeren Nebenwirkungen behaftet sind.
Die Wilhelm Sander-Stiftung fördert die Fortsetzung dieses Forschungsprojekt mit weiteren über 160.000 €, nachdem bislang bereits über 150.000 € Fördermittel geflossen sind.