Von der Mikroskopie zur Nanoskopie: Leibniz-Preis für Professor Stefan Hell
Die Deutsche Forschungsgemeinschaft (DFG) verlieh am 11. Februar die Leibnizpreise für das Jahr 2008. Einer der Preisträger ist Professor Stefan Hell, Direktor am Max-Planck-Institut für Biophysikalische Chemie in Göttingen. Einen Teil des Preisgeldes in Höhe von 2,5 Millionen Euro wird der Physiker auch im Deutschen Krebsforschungszentrum einsetzen, wo er die Kooperationsabteilung "Hochauflösende Optische Mikroskopie" leitet.
Bis vor wenigen Jahren galt für die Lichtmikroskopie die magische Auflösungsgrenze von 200 Nanometern, die Ernst Abbe bereits im Jahr 1873 in seinem berühmten Gesetz formulierte: Mindestens die Hälfte der Wellenlänge des sichtbaren Lichtes müssten zwei Punkte in der Brennebene des Objektivs auseinander liegen, um voneinander unterschieden zu werden. Erst 120 Jahre später, Anfang der 1990er Jahre, gelang es dem Physiker Stefan Hell, diese magische Grenze zu durchbrechen und den Grundstein für die Lichtmikroskopie mit Auflösungen auf der Nanoskala - der Lichtnanoskopie - zu legen.
Auch mit Elektronen- oder Rastersondenmikroskopen lassen sich Strukturen im Nanometerbereich erkennen. Allerdings müssen die Präparate für diese Techniken in hauchdünne Scheiben geschnitten werden. Untersuchungen von intakten oder sogar lebenden Zellen sind so unmöglich. Das vermag nur fokussiertes Licht.
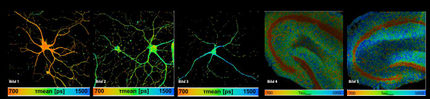
Als ersten Schritt erfand Stefan Hell 1990 das 4Pi-Mikroskop, bei dem das Licht statt von einer von zwei Seiten gleichzeitig auf das Objekt fällt. Damit konnte die Auflösung bereits um das Vier- bis Siebenfache gesteigert werden. Mit der "Stimulated Emission Depletion" (STED-)Mikroskopie, einem Verfahren, das die Eigenschaften der Fluoreszenz-Farbstoffe ausnützt, die man ohnehin zum Anfärben von Proteinen oder DNA verwendet, ließ sich die Auflösung auch in der Brennebene dramatisch erhöhen und somit Abbes Beugungsgrenze durchbrechen: Damit lassen sich biologische Strukturen erkennen, die bis zu 2000-mal feiner sind als ein menschliches Haar (20 bis 50 Nanometer).
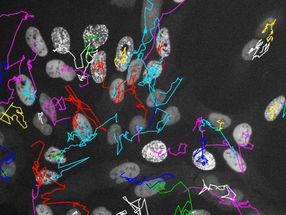
Im Krebsforschungszentrum arbeiten Hell und seine Mitarbeiter an der Entwicklung besonders leistungsfähiger Varianten dieser neuen Verfahren und setzen sie in der biologischen und medizinischen Grundlagenforschung ein. So plant Hell mit einem Teil des Leibniz-Preisgeldes einen weiteren Quantensprung der Lichtnanoskopie: die Kombination aus STED- und 4Pi-Mikroskopie in lebenden Zellen. Damit soll die Auflösung in allen drei Raumrichtungen weiter verbessert werden, um besonders detailreiche Bilder aus dem Inneren einer lebenden Zelle zu gewinnen. Durch besonders schnelle Aufnahmetechniken sollen so physiologische Prozesse in der lebenden Zelle mit hoher Auflösung sichtbar gemacht werden, etwa das Freisetzen von Botenstoffen an Nervenenden oder aber die Unterschiede in der Genaktivität. Viele weitere Fragen der biomedizinischen Forschung, so erwarten die Forscher, werden sich mit diesen Aufnahmen klären lassen.
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.