TransMIT-Patent für Alzheimer-Wirkstoff erweist sich als äußerst viel versprechend
Gießen. Der 2002 von der Gießener TransMIT GmbH zum Patent angemeldete Wirkstoff des Marburger Professors Dr. Thomas Schrader und seines Düsseldorfer Amtskollegen Dr. Detlev Riesner erweist sich während der in vitro-Testphase an lebenden Nervenzellen als äußerst viel versprechend und soll nun in vivo an transgenen Mäusen getestet werden.
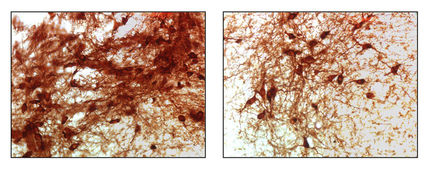
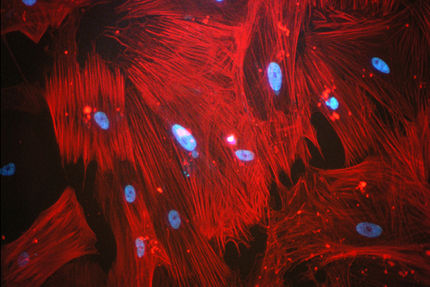
Ein künstliches, am Computer maßgeschneidertes Molekül soll zukünftig die bei Alzheimer- sowie Creutzfeld-Jacob-Erkrankungen und BSE abnormal veränderten Eiweiße an ihrer Verklumpung hindern und so einem Absterben der Neuronen und dem schrittweisen Funktionsverlust des Gehirns entgegenwirken.
Unter Einfluss neurodegenerativer Erkrankungen bilden die betroffenen Eiweißmoleküle ihre ursprünglich vorwiegend ungeordnete Struktur in eine Beta-Faltblatt-Struktur um. Als Ziehharmonika-förmige Beta-Amyloid-Peptide neigen sie aufgrund ihrer klebrigen Oberfläche zur Bildung von Ablagerungen im Gehirn, den so genannten Plaques. Werden die Eiweißmoleküle nicht ausreichend und schnell genug abgebaut oder ausgeschieden, verbinden sie sich zu Beta-Amyloid-Fibrillen und anschließend zu Amyloid-Plaques, die die Sauerstoffversorgung und damit die Funktion der Nervenzellen beeinträchtigen.
Die von den Wissenschaftlern entwickelten Wirkstoffe aus der Substanzgruppe der Acylaminopyrazole lagern sich an die Beta-Amyloid- Peptidstränge an und verhindern ein weiteres Verklumpen.
Das Besondere der Wirkungsweise liegt dabei darin, dass die künstlich hergestellten Moleküle das Wasserstoffbrückenmuster der krankhaften Alzheimer-Eiweiße nachahmen. In komplementärer Anordnung bilden sie zu jedem Wasserstoffbrücken-Donor und -Akzeptor eine H-Brücke aus und legen sich wie Kappen auf alle Carboxyl- und Stickstoff-Wasserstoff-Gruppen der Peptidbindungen. Der Beta-Amyloid-Peptidstrang wird so entlang seiner beiden klebrigen Außenseiten verkappt und an einer weiteren Aggregation mit benachbarten Polypeptidketten gehindert. Der Abbau der solcherart unschädlich gemachten Beta-Amyloid-Peptidstränge erfolgt anschließend über natürliche, körpereigene Mechanismen.
Die in Kooperation mit der im österreichischen Graz ansässigen JSW-Research Forschungslabor GmbH durchgeführten in vitro-Tests sind sehr erfolgreich verlaufen und geben klare Hinweise für die Substanzauswahl der nun von Frühsommer bis Oktober 2004 vorgesehenen in vivo-Testreihe. Diese wird mit transgenen "Alzheimer"-Mäusen erfolgen, die im Alter von sechs bis acht Monaten zerebrale Beta-Amyloid-Ablagerungen und in Folge dessen Gedächtnisstörungen aufweisen.
Die Zahl der in Deutschland mittelschwer und schwer Demenzerkrankten liegt bei gut 1 Million - mit einem prognostizierten Anstieg bis 2050 auf etwa 2 Millionen. In Europa leiden rund drei Prozent der über 60-jährigen an Alzheimer. Werden sich die positiven Befunde im Tiermodell reproduzieren, so gehen die Kooperationspartner davon aus, bereits in vier bis fünf Jahren ein wirksames Medikament zur Behandlung und Heilung von Alzheimer-Erkrankungen vorlegen zu können.
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
Pharmaceutical Substances von Thieme Verlag
Entdecken Sie industrielle Synthesewege für 2.600 APIs
Ihr Recherchetool für Synthesen, Patente und Anwendungen – Pharmaceutical Substances

KNAUER IJM NanoScaler von KNAUER
Effiziente Formulierung von Lipid-Nanopartikeln für RNA-basierte Therapien
Optimieren Sie die Wirkstoffverkapselung von 1 ml bis zu Hunderten von Millilitern mit minimalem Wirkstoffeinsatz

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.